Clear Sky Science · it
Identificazione di RBX1 come regolatore della trascrizione di LIPT1 e del suo ruolo nella morte cellulare indotta dal rame nelle cellule di GBM
Perché il rame e i tumori cerebrali sono importanti
Il glioblastoma multiforme è una delle forme più letali di tumore cerebrale: la maggior parte dei pazienti sopravvive solo per un breve periodo dopo la diagnosi, nonostante interventi chirurgici aggressivi, radioterapia e chemioterapia. Questo studio esplora un alleato inaspettato contro questi tumori: il metallo rame. I ricercatori indagano una forma di morte cellulare di recente riconoscimento scatenata dal rame e identificano una via molecolare che potrebbe consentire ai clinici di sfruttare questo processo per indebolire i tumori e, potenzialmente, potenziare l’attacco del sistema immunitario contro le cellule cancerose.
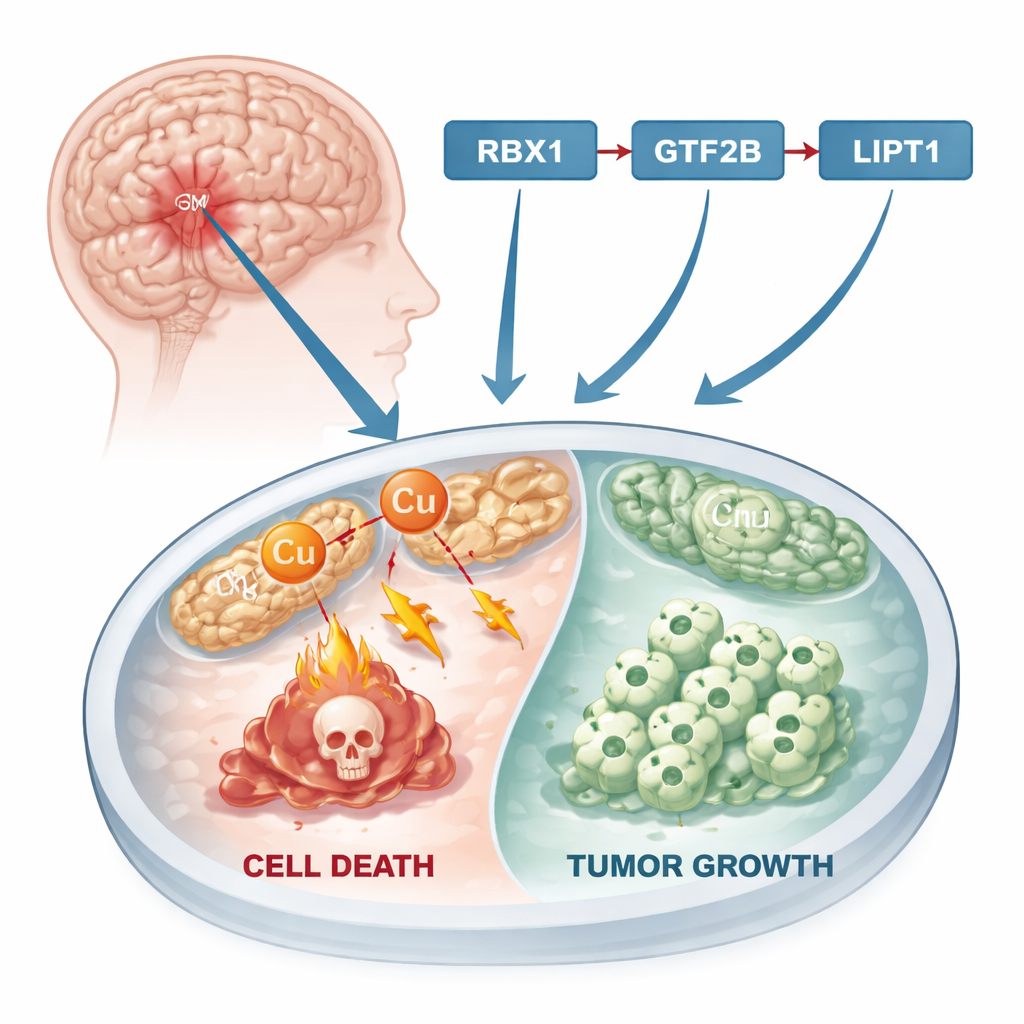
Un nuovo modo per le cellule di morire
Per decenni la ricerca sul cancro si è concentrata su forme note di morte cellulare come l’apoptosi, in cui le cellule danneggiate si spengono silenziosamente. Recentemente gli scienziati hanno scoperto una via diversa chiamata morte cellulare indotta dal rame, o “cuprotosi”. In questo processo, un eccesso di rame si accumula nelle “fabbriche energetiche” della cellula, i mitocondri. Lì il rame altera proteine chiave, provocando la formazione di aggregati tossici che alla fine uccidono la cellula. Poiché molti tumori presentano un metabolismo dei metalli alterato e livelli di rame superiori rispetto ai tessuti normali, la cuprotosi offre un possibile punto di pressione: se i ricercatori riuscissero a spingere le cellule tumorali verso questa morte mediata dal rame, potrebbero rallentare o arrestare la crescita del cancro.
In luce un gene chiave nel glioblastoma
Gli autori hanno iniziato analizzando un gruppo di geni già noti per essere coinvolti nella cuprotosi e hanno valutato il loro comportamento nei campioni di glioblastoma rispetto al tessuto cerebrale normale. Un gene in particolare, chiamato LIPT1, è emerso come rilevante. Risultava più attivo nel tessuto di glioblastoma e in diverse linee cellulari di glioblastoma rispetto alle cellule cerebrali normali. In modo significativo, i pazienti i cui tumori presentavano un’attività più elevata di LIPT1 tendevano a rimanere liberi da ricadute più a lungo dopo il trattamento. Livelli alti di LIPT1 erano anche associati a una maggiore presenza di cellule CD8 T, i principali effettori immunitari contro il cancro, suggerendo che questo gene potrebbe rendere l’ambiente tumorale più vulnerabile all’attacco immunitario.
Cosa succede quando l’interruttore della morte da rame viene attenuato
Per verificare se LIPT1 influenzi davvero la morte cellulare indotta dal rame, il gruppo ha esposto cellule di glioblastoma a una combinazione farmacologica che trasporta rame e che induce in modo affidabile la cuprotosi. Hanno quindi usato strumenti genetici per ridurre i livelli di LIPT1. Quando LIPT1 è stato soppresso, le cellule tumorali sono diventate più resistenti alla uccisione da rame, hanno mostrato una maggiore sopravvivenza e capacità aumentata di migrare e invadere — comportamenti associati a un cancro più aggressivo. In colture miste di cellule tumorali e cellule CD8 umane, la riduzione di LIPT1 ha inoltre diminuito il rilascio di molecole di segnalazione immunitaria e ha reso le cellule cancerose più difficili da eliminare per i linfociti T. Nel complesso, questi esperimenti indicano che LIPT1 aumenta la sensibilità alla morte indotta dal rame e sostiene l’attività immunitaria anti-tumorale.
Seguendo la catena di comando fino a RBX1
La sfida successiva è stata capire perché LIPT1 risulti aumentato nel glioblastoma. Combinando diversi grandi database di geni e proteine, i ricercatori hanno identificato un fattore di trascrizione — una specie di interruttore maestro dell’attività genica — chiamato GTF2B che si lega vicino al gene LIPT1 e probabilmente ne potenzia l’espressione. Hanno poi indagato cosa controlli a sua volta GTF2B. È emersa come forte candidata una seconda proteina, RBX1. RBX1 fa parte del sistema cellulare di etichettatura e smaltimento che marca altre proteine per la degradazione. Nelle cellule di glioblastoma, i livelli di RBX1 erano più bassi rispetto alle cellule cerebrali normali, mentre GTF2B e LIPT1 risultavano aumentati. Test di laboratorio hanno mostrato che RBX1 può attaccare piccoli “tag distruggimi” a GTF2B, portandone alla degradazione; quando RBX1 veniva incrementato, i livelli di GTF2B e l’attività di LIPT1 diminuivano, e bloccare il macchinismo di degradazione cellulare invertiva questo effetto.
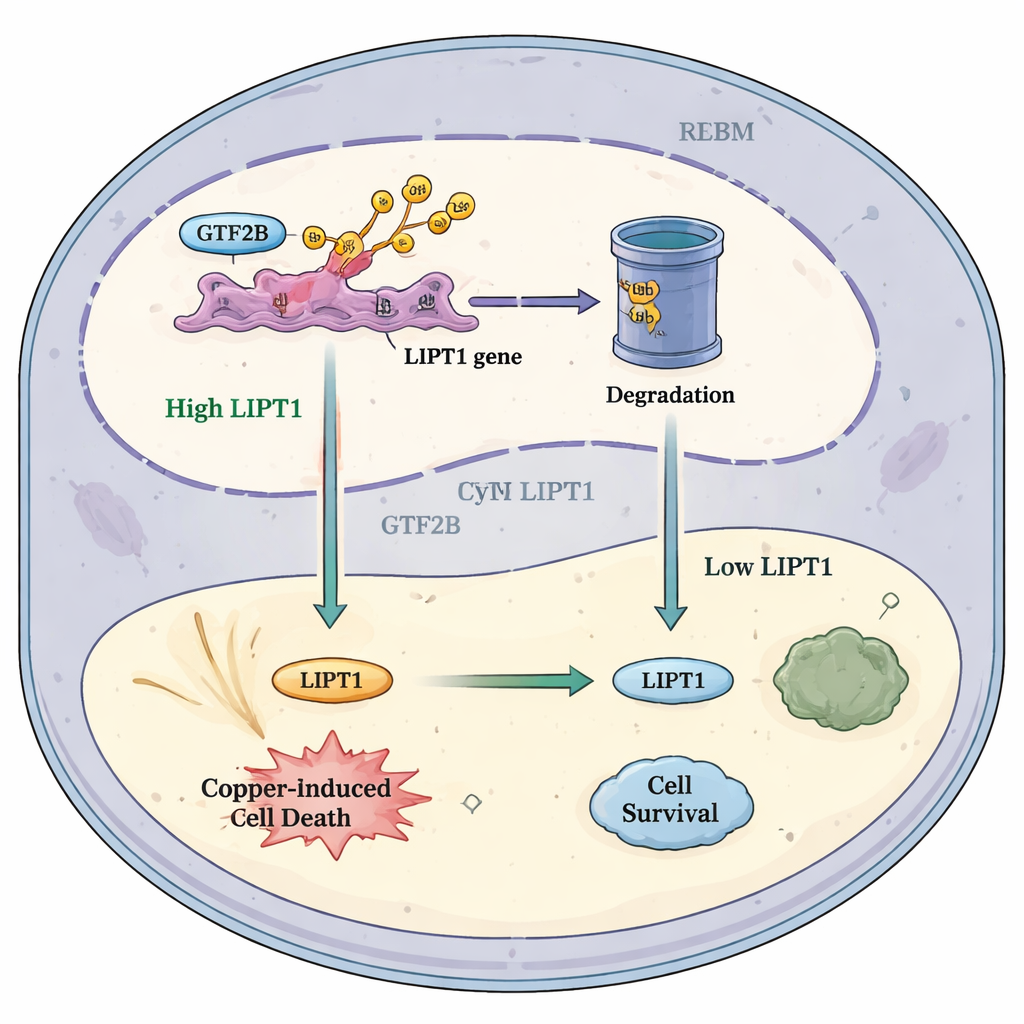
Come questa via potrebbe aiutare i trattamenti futuri
Mettere insieme questi risultati porta gli autori a proporre un modello semplice: in condizioni sane, RBX1 mantiene GTF2B sotto controllo, limitando quanto intensamente attiva il gene LIPT1. Nel glioblastoma, la riduzione di RBX1 porta a una minore degradazione di GTF2B. L’eccesso di GTF2B aumenta quindi LIPT1, accrescendo la sensibilità delle cellule tumorali alla morte indotta dal rame e richiamando più cellule immunitarie anti-cancro. Questo modello suggerisce che modulare con attenzione la via RBX1–GTF2B–LIPT1, possibilmente in combinazione con farmaci che mirano il rame e con immunoterapie, potrebbe spostare l’equilibrio all’interno dei tumori cerebrali verso l’autodistruzione. Pur essendo necessario ancora molto lavoro prima che questa idea possa arrivare ai pazienti, lo studio evidenzia un’interessante convergenza tra biologia dei metalli, regolazione genica e immunologia del cancro che potrebbe aprire nuove vie terapeutiche per uno dei tumori più ostinati.
Citazione: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Parole chiave: glioblastoma, morte cellulare indotta dal rame, LIPT1, immunologia tumorale, via RBX1