Clear Sky Science · it
Integrazione di machine learning e modellazione basata sulla fisica per la progettazione predittiva di nanocompositi caricati con gemcitabina
Medicinali oncologici più intelligenti progettati su misura
Farmaci antitumorali come la gemcitabina possono salvare vite, ma spesso si comportano più come strumenti grezzi che come strumenti di precisione: si degradano rapidamente, non raggiungono sempre il bersaglio e provocano effetti collaterali severi. Questo studio esplora come i computer possano aiutare gli scienziati a "pre-testare" nuovi vettori di farmaco in scala nanometrica sullo schermo, invece che solo in laboratorio, per rendere i trattamenti con gemcitabina più efficaci, più duraturi e potenzialmente più sicuri per i pazienti.
Perché i vettori microscopici sono importanti
La chemioterapia tradizionale inonda il corpo con molecole di farmaco che circolano ovunque, non solo nei tumori. I nanocompositi — particelle ingegnerizzate migliaia di volte più piccole di un granello di sabbia — offrono un modo per incapsulare la gemcitabina in modo che sia protetta nel flusso sanguigno e veicolata più direttamente alle cellule tumorali. Due valori decidono in larga misura se un progetto è utile. L'efficienza di caricamento indica quanto farmaco finisce all'interno di ciascuna particella, mentre l'efficienza di incapsulamento misura quale frazione del farmaco iniziale viene effettivamente intrappolata anziché sprecata. Valori elevati per entrambi significano meno iniezioni, meno materiale vettore e una maggiore probabilità di colpire il tumore con forza senza sovraccaricare il resto del corpo.
Dal tentativo ed errore alla progettazione guidata dai dati
Progettare questi nanovettori manualmente è come cercare di sintonizzare una radio con centinaia di manopole — dimensione delle particelle, carica superficiale, materiali, rivestimenti e metodi di preparazione interagiscono tutti in modi complessi. Finora i ricercatori cambiavano perlopiù una o due impostazioni alla volta e ne misuravano il risultato, un ciclo lento e costoso che svela soltanto una piccola porzione del quadro completo. In questo lavoro, gli autori hanno raccolto 59 ricette di nanovettori per gemcitabina accuratamente valutate dalla letteratura scientifica e le hanno arricchite con esempi addizionali basati sulla fisica generati al computer. Questo dataset combinato ha permesso di testare diverse tecniche di machine learning — programmi informatici che apprendono pattern dai dati — per prevedere le efficienze di caricamento e incapsulamento a partire solo dalle scelte di progettazione.
Lasciare che la fisica guidi gli algoritmi
La maggior parte dei sistemi di machine learning sono potenti adattatori di curva: riescono a individuare pattern ma non sanno quando una risposta viola le leggi della natura. Per evitare predizioni irrealistiche, i ricercatori hanno costruito un metodo ibrido che unisce i dati a regole fisiche di base su come le molecole di farmaco si muovono, si legano e raggiungono l'equilibrio in un sistema chiuso. Nel loro quadro, qualunque previsione che implichi, per esempio, la creazione di più farmaco di quello inizialmente aggiunto, o che ignori come le molecole diffondono attraverso un materiale, viene penalizzata durante l'addestramento. Questo approccio "informato dalla fisica" indirizza il modello verso risposte che hanno senso chimico e fisico, specialmente in regioni dello spazio di progettazione dove le misure sperimentali sono scarse.
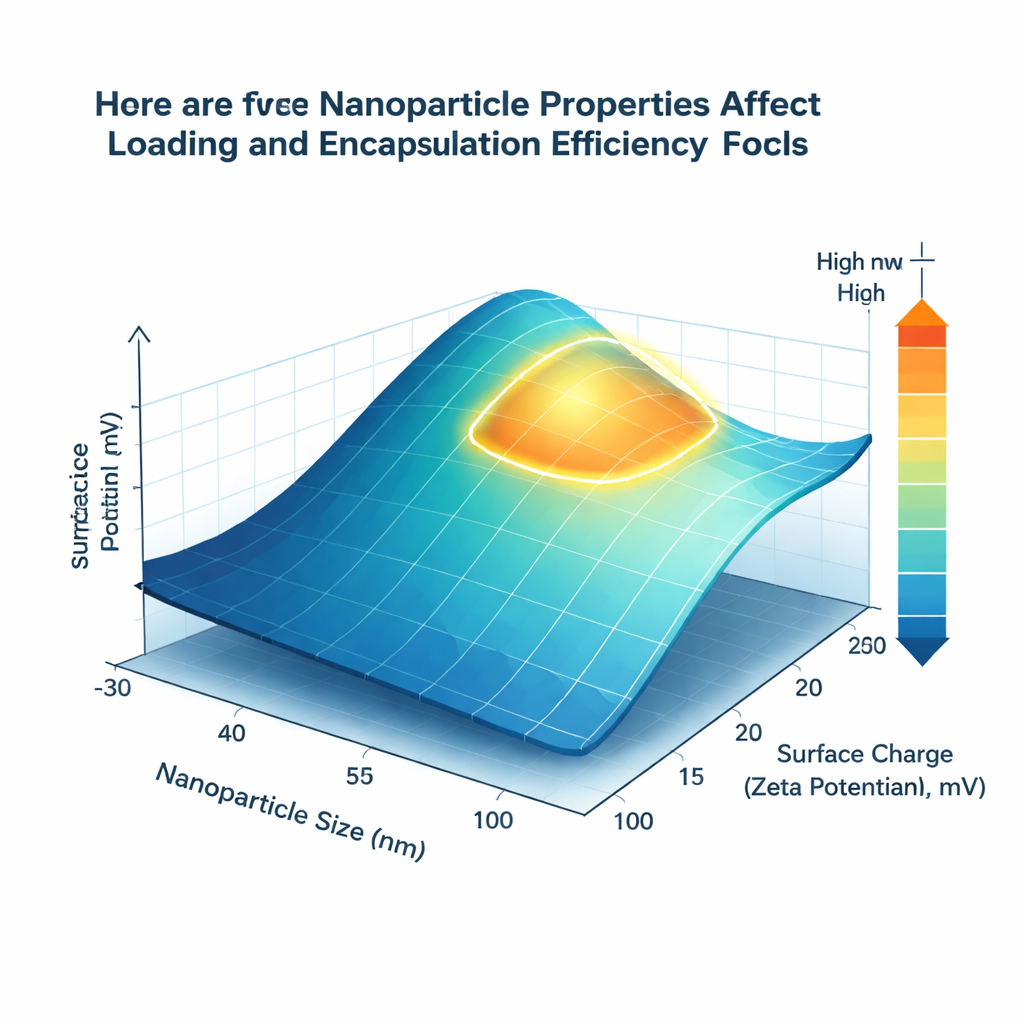
Cosa hanno scoperto i modelli
Tra le tecniche testate, un algoritmo ensemble avanzato chiamato XGBoost ha fornito le previsioni più accurate, rispecchiando da vicino i risultati sperimentali segnalati per entrambe le efficienze chiave. Ma oltre all'accuratezza, il team cercava regole di progettazione comprensibili. Usando un metodo chiamato SHAP, che classifica quanto ciascun fattore spinge la previsione verso l'alto o verso il basso, hanno osservato che dimensione delle particelle e carica superficiale dominano costantemente le prestazioni. Nanovettori con diametro compreso approssimativamente tra 80 e 150 nanometri offrivano il miglior equilibrio tra area superficiale e volume interno, aumentando sia il caricamento sia l'incapsulamento. Una carica superficiale lievemente positiva, nell'intervallo di +15 a +25 millivolt, risultava correlata a un migliore intrappolamento della gemcitabina, probabilmente perché le superfici dei vettori cariche positivamente interagiscono favorevolmente con i gruppi negativi del farmaco.
Una mappa digitale per i trattamenti oncologici futuri
Il risultato finale non è un medicinale pronto, ma uno strumento di pianificazione potente. Lo studio fornisce una sorta di "mappa di progettazione" che indica ai ricercatori le ricette di nanovettori più promettenti per trattenere e proteggere bene la gemcitabina, evitando milioni di combinazioni poco promettenti. Gli autori sottolineano che le loro previsioni devono ancora essere confermate con nuovi studi di laboratorio e su modelli animali, e che il loro dataset — sebbene assemblato con cura — è di dimensioni modeste. Nonostante ciò, questo framework di machine learning consapevole della fisica mostra come i computer possano aiutare a restringere la ricerca di vettori per farmaci oncologici migliori, riducendo i costi e accelerando il percorso dalle idee a terapie più precise e più compatibili per i pazienti.
Citazione: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
Parole chiave: nanomedicina, gemcitabina, consegna del farmaco, apprendimento automatico, nanoparticelle