Clear Sky Science · it
MCT1 come regolatore critico della segnalazione insulinica, dell’omeostasi energetica e della funzione dei podociti
Perché contano le scelte energetiche delle cellule renali
I nostri reni filtrano silenziosamente centinaia di litri di sangue ogni giorno, e buona parte di quel lavoro dipende da piccole cellule chiamate podociti che avvolgono i filtri renali. Queste cellule devono rimodellarsi continuamente per mantenere le proteine nel sangue e i rifiuti nelle urine. Questo studio esplora come i podociti ottengono l’energia di cui hanno bisogno, cosa succede quando una delle loro principali “porte del carburante” viene bloccata e perché ciò potrebbe essere rilevante per condizioni comuni come il diabete e le malattie renali. 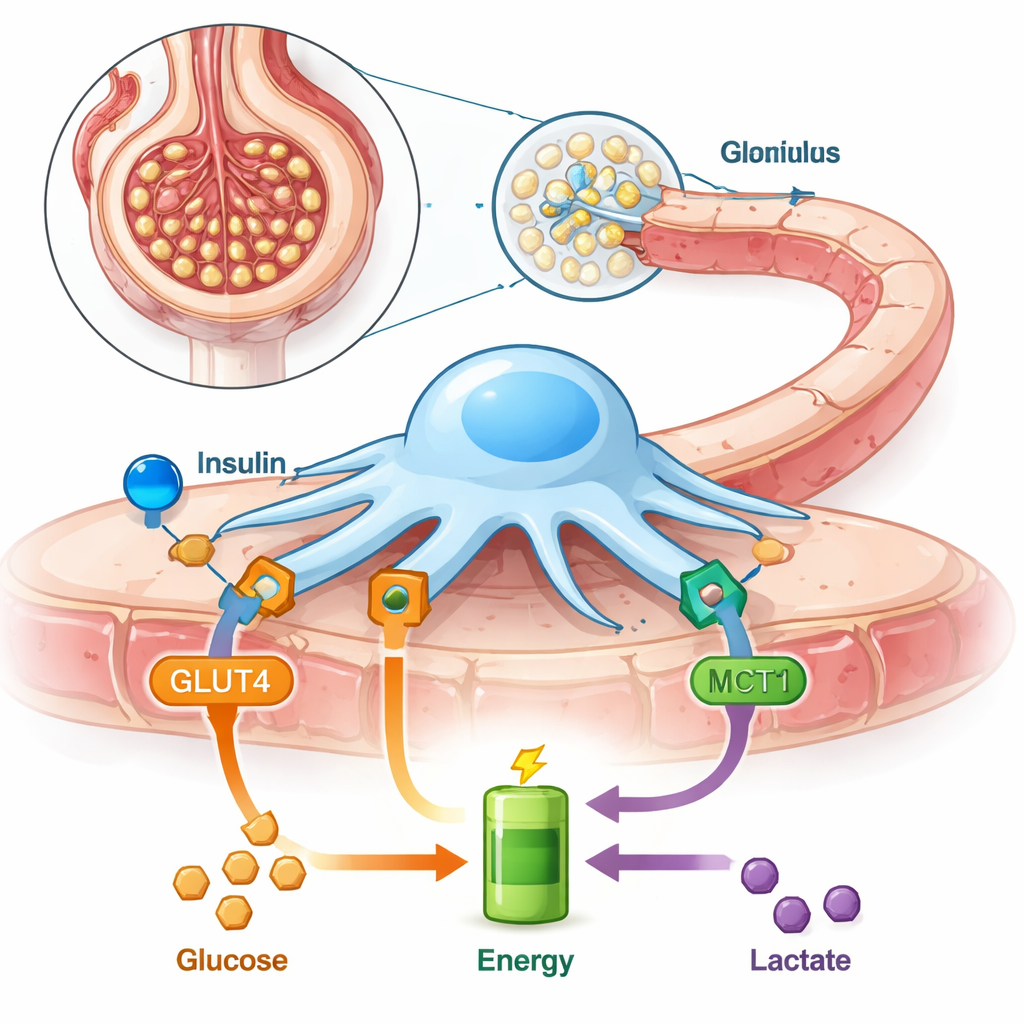
Le cellule guardiane del filtro
I podociti si trovano sul lato esterno di ogni filtro renale, estendendo sottili prolungamenti a forma di piede che si interbloccano per formare una barriera finale prima che l’urina venga prodotta. Poiché si adattano costantemente nella forma, consumano molta energia. Diversamente da molte altre cellule, i podociti dipendono in larga misura dalla degradazione dello zucchero senza ossigeno (una via chiamata glicolisi) e sono particolarmente sensibili all’insulina, che segnala loro di introdurre più glucosio dal sangue tramite un trasportatore chiamato GLUT4. Gli autori avevano dimostrato in precedenza che i podociti possono anche utilizzare il lattato, una piccola molecola spesso liquidata come “rifiuto”, suggerendo che queste cellule sono più flessibili di quanto si pensasse.
La porta del lattato: MCT1
Il lattato entra ed esce dalle cellule attraverso proteine trasportatrici speciali. Una delle più importanti è il trasportatore monocarboxilato 1 (MCT1), che può portare il lattato nelle cellule per essere utilizzato come fonte energetica. In questo studio, i ricercatori hanno usato podociti di ratto coltivati in vitro e hanno bloccato MCT1 con un inibitore chimico. Hanno quindi esaminato come questo influisse sulla capacità dell’insulina di stimolare l’assorbimento di glucosio, sulla quantità di energia che le cellule potevano produrre, sull’aspetto del loro impalcatura interna e su quanto la barriera filtrante diventasse “permeabile” a una grande proteina ematica chiamata albumina. Hanno anche testato filtri renali interi di ratto (glomeruli isolati) per vedere come il lattato e il blocco di MCT1 modificassero la perdita di proteine in un sistema più intatto.
Quando la porta del carburante si chiude
Il blocco di MCT1 ha avuto diversi effetti notevoli. Innanzitutto, ha ridotto la quantità di glucosio assorbita dai podociti, sia a riposo sia dopo la stimolazione con insulina, e ha indebolito un interruttore chiave nella via insulinica (una proteina chiamata Akt) senza alterare il recettore dell’insulina stesso. Allo stesso tempo, il normale spostamento del trasportatore GLUT4 verso la superficie cellulare è risultato attenuato. Le misurazioni del metabolismo cellulare hanno mostrato che la produzione energetica totale è diminuita quando MCT1 è stato bloccato, e le cellule hanno spostato il loro metabolismo lontano dalla glicolisi verso un maggior consumo ossidativo nei mitocondri. Anche quando venivano aggiunti insulina o lattato, questo deficit energetico non veniva completamente compensato, suggerendo che MCT1 è centrale per l’equilibrio delle fonti energetiche nei podociti. 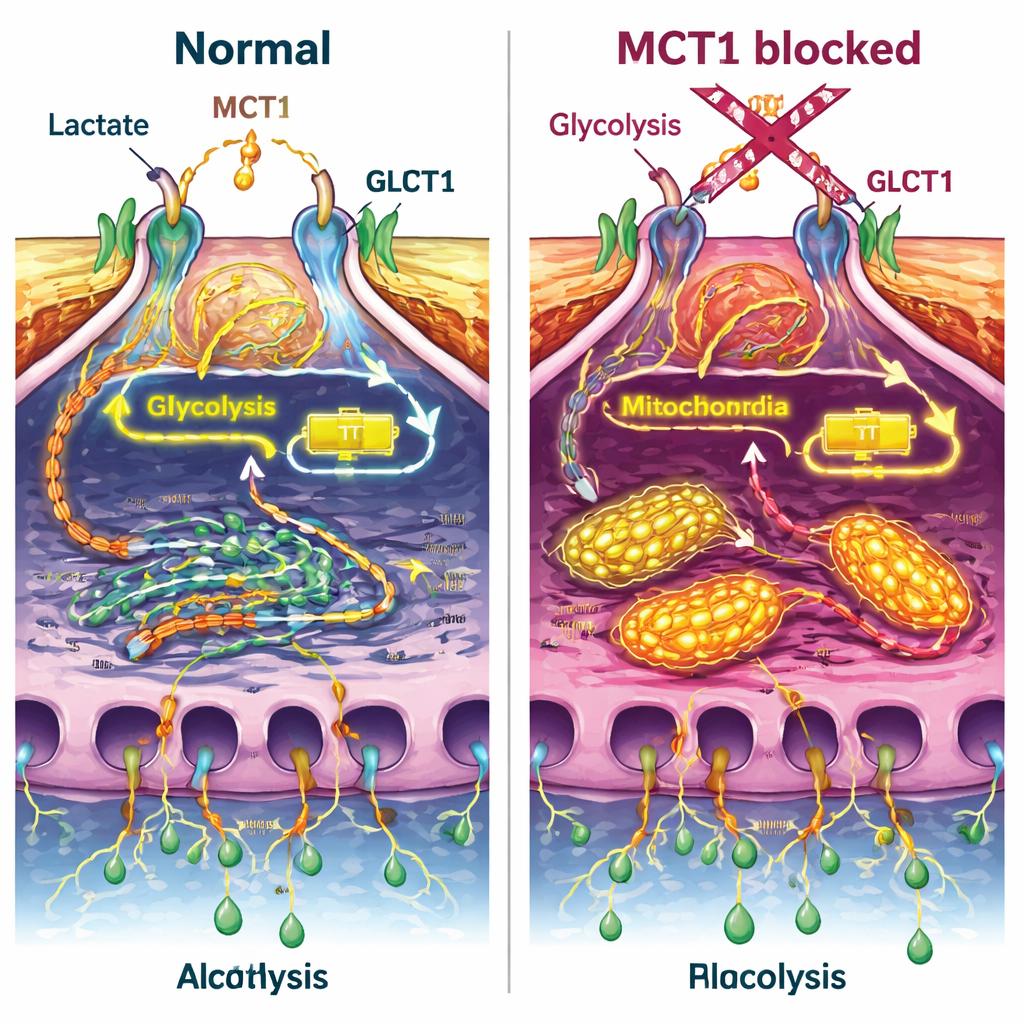
Filtri che perdono e impalcature sotto stress
I cambiamenti energetici erano strettamente collegati al danno fisico. Quando MCT1 è stato bloccato, gli strati di podociti in coltura hanno lasciato passare più albumina, un effetto simile a quello osservato con l’insulina da sola. Anche il lattato di per sé ha aumentato la permeabilità della barriera, e la combinazione di lattato o insulina con il blocco di MCT1 ha mantenuto elevata la permeabilità. All’interno delle cellule, le fibre di actina che formano la loro struttura sono diventate più aggrovigliate e disorganizzate, un modello associato alla perdita dei sottili pedicelli che compongono il filtro. Un’altra proteina chiave, la nefrina, che aiuta a tenere insieme il filtro e supporta anche l’azione dell’insulina, è risultata ridotta o mal localizzata quando MCT1 è stato inibito. Nei filtri renali isolati di ratto, l’aggiunta di lattato ha rapidamente aumentato la perdita di albumina, e il blocco di MCT1 ha prodotto un aumento simile, a sostegno dell’idea che un alterato trattamento del lattato indebolisca direttamente la barriera.
Implicazioni per il diabete e la salute renale
Gli autori propongono che il corretto movimento del lattato attraverso MCT1 sia essenziale perché i podociti mantengano il loro programma energetico preferito, rispondano all’insulina e conservino una barriera di filtrazione serrata. Quando questa “porta” del lattato viene alterata—per blocco di MCT1 o per iperglicemia cronica che modifica l’equilibrio del lattato—i podociti perdono flessibilità metabolica, consumano meno glucosio, dipendono eccessivamente dai mitocondri e diventano strutturalmente instabili e più permeabili. Per le persone, questo lavoro suggerisce che cambiamenti sottili nel modo in cui le cellule renali gestiscono il lattato potrebbero contribuire alla resistenza all’insulina e ai danni renali precoci molto prima che la funzione renale complessiva risulti anomala. Comprendere e, in prospettiva, mirare a questo sistema di trasporto del lattato potrebbe aprire nuove strade per proteggere i filtri renali nel diabete e in altre malattie metaboliche.
Citazione: Szrejder, M., Audzeyenka, I., Rachubik, P. et al. MCT1 as a critical regulator of insulin signaling, energy homeostasis and podocyte function. Sci Rep 16, 5906 (2026). https://doi.org/10.1038/s41598-026-37093-x
Parole chiave: podociti renali, metabolismo del lattato, resistenza all’insulina, barriera di filtrazione glomerulare, trasportatore MCT1