Clear Sky Science · it
Un quadro unificato multimodale basato su transformer per la previsione della recidiva del cancro al seno e l’analisi di sopravvivenza
Perché è importante prevedere il ritorno del cancro
Per molte donne, il termine del trattamento per il cancro al seno porta sollievo ma lascia anche una domanda persistente: la malattia tornerà, e se sì, quando e con quale gravità? I piani di follow‑up odierni si basano spesso su medie generali piuttosto che sul mix unico di fattori che caratterizza ogni paziente. Questo studio presenta un nuovo sistema di intelligenza artificiale che mira a offrire ai medici una visione più chiara e personalizzata sia del rischio di recidiva del cancro al seno sia della durata probabile del periodo libero da malattia.
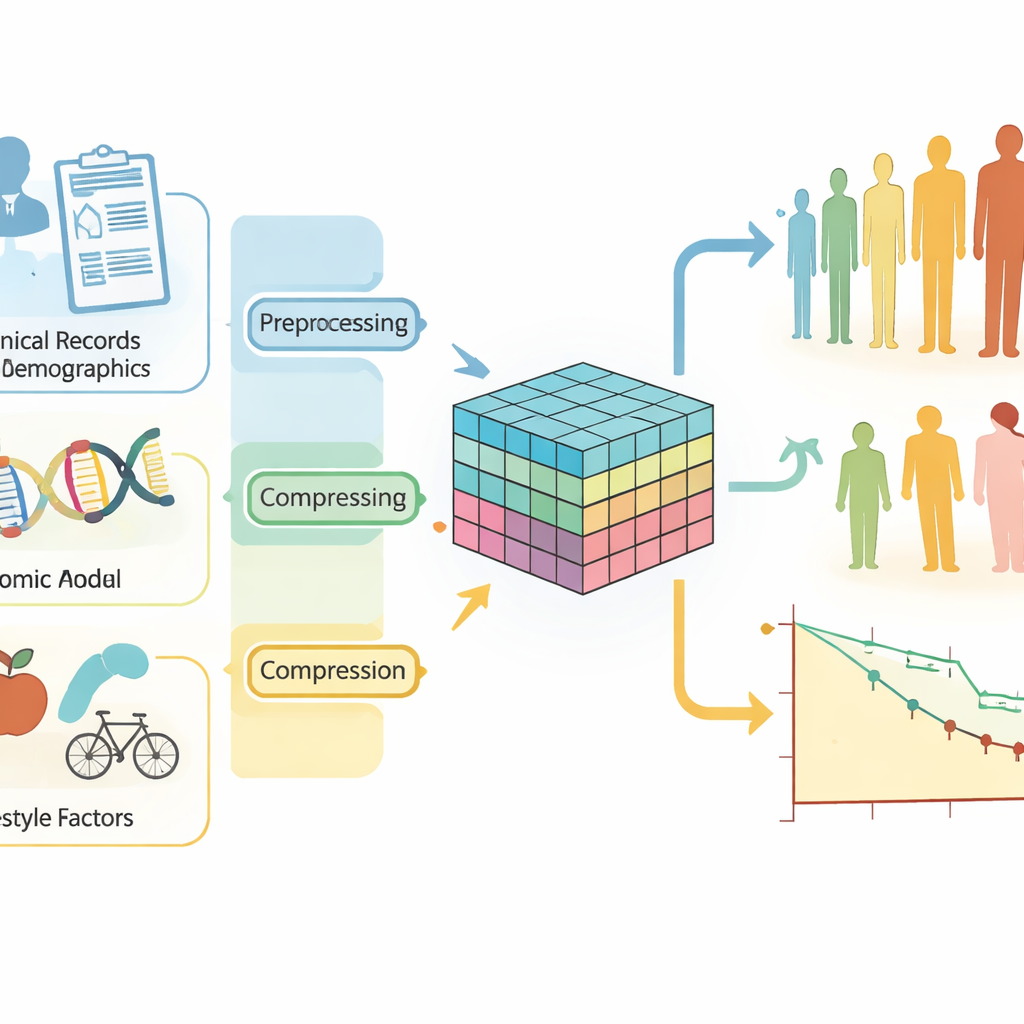
Mettere insieme molte tipologie di dati del paziente
La recidiva del cancro al seno non è un risultato unico. Può manifestarsi come un nuovo tumore nello stesso seno, una diffusione ai linfonodi vicini o metastasi a distanza in organi come polmoni o ossa. Ogni pattern comporta implicazioni diverse per trattamento e sopravvivenza. Allo stesso tempo, il rischio è modellato da molte influenze intrecciate: caratteristiche del tumore, attività genica, età, stato menopausale, peso corporeo, fumo e altro. Gli strumenti statistici tradizionali faticano di fronte a questo mix di informazioni cliniche, genetiche e legate allo stile di vita. Tipicamente assumono relazioni semplici e lineari e spesso si basano su punteggi di rischio costruiti a mano che non riescono a catturare la reale complessità dei dati oncologici moderni.
Un modello intelligente unificato invece di strumenti separati
I ricercatori hanno progettato un unico framework di deep learning che affronta due compiti contemporaneamente: predice quale delle quattro tipologie di recidiva è più probabile per una paziente e stima il momento in cui quell’evento potrebbe verificarsi mediante analisi di sopravvivenza. Invece di costruire modelli separati per “tornerà?” e “quando tornerà?”, il sistema apprende entrambe le risposte insieme. Sotto il cofano utilizza un’architettura transformer—la stessa famiglia di modelli alla base di molti strumenti linguistici all’avanguardia—per scoprire pattern sottili e interazioni a lungo raggio nei dati. Questo approccio unificato intende rispecchiare il modo di ragionare degli oncologi, che valutano molteplici indizi simultaneamente invece di eseguire calcoli isolati.
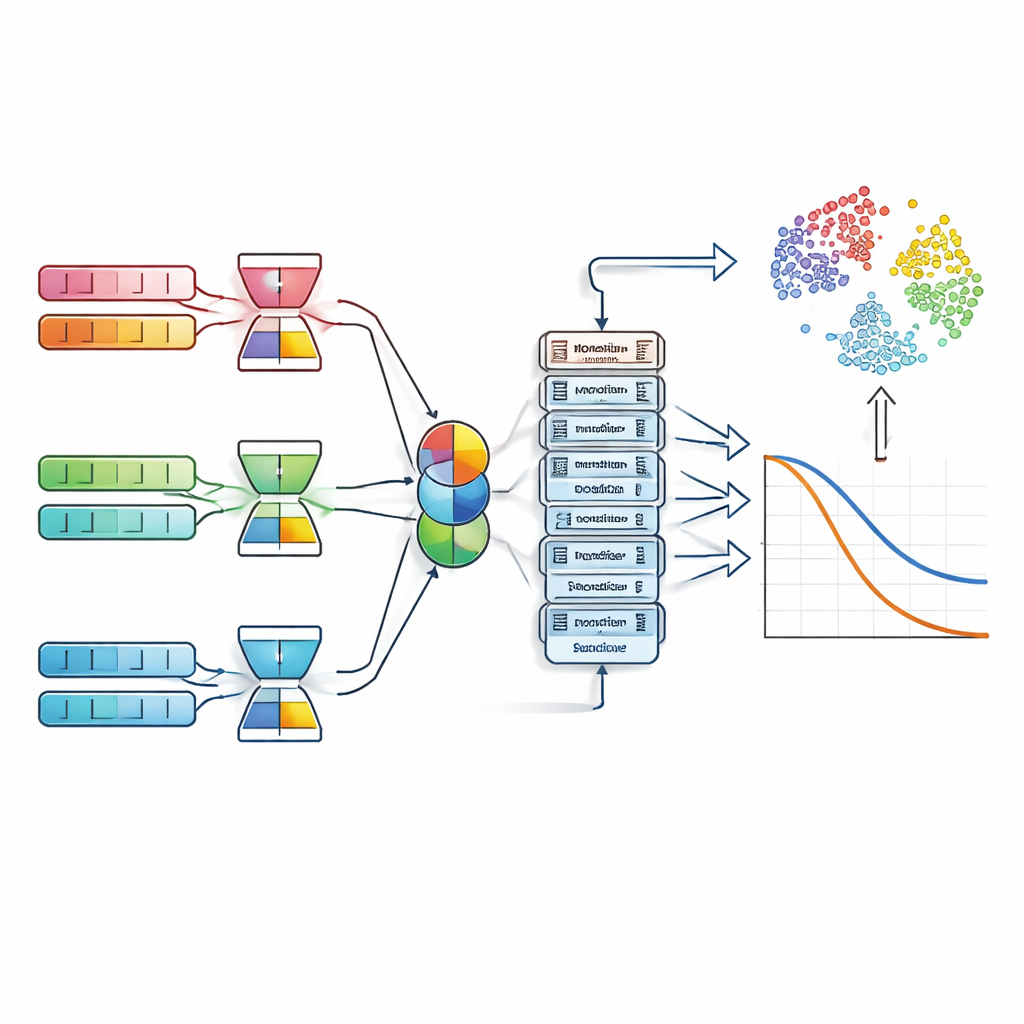
Come il sistema individua i pattern nei dati sanitari
Per alimentare il modello, il team ha assemblato un’ampia raccolta multicentrica di cartelle cliniche del cancro al seno provenienti da cinque fonti note. Queste comprendono migliaia di pazienti con misure cliniche dettagliate, profili di espressione genica, informazioni demografiche e indicatori dello stile di vita. Poiché tali dati possono essere rumorosi e ad alta dimensionalità—soprattutto le decine di migliaia di misure di attività genica—il sistema passa inizialmente ogni tipo di dato attraverso un “autoencoder denoising”. Questo passaggio comprime ogni modalità in una rappresentazione più pulita e compatta che conserva segnali biologici importanti filtrando l’alone casuale.
Apprendere cosa conta di più per ogni paziente
Dopo la compressione, il modello non si limita a incollare tutte le caratteristiche insieme. Applica invece un meccanismo di attenzione per modalità che apprende quanto peso assegnare alle informazioni cliniche, genetiche o legate allo stile di vita per ciascuna persona. Per alcune pazienti possono prevalere la dimensione del tumore e lo stato dei recettori ormonali; per altre, un particolare schema genico o la storia di fumo possono essere più indicativi. Questi segnali pesati vengono fusi in un profilo paziente unico e processati da strati transformer impilati, che utilizzano l’auto‑attenzione per modellare come i diversi fattori di rischio interagiscono. Da questa rappresentazione condivisa, un ramo predice il tipo di recidiva, mentre un altro stima un punteggio di rischio continuo che può essere tradotto in curve di sopravvivenza a cinque e dieci anni.
Prestazioni, validazione e interpretabilità
Nei test condotti sulle cinque banche dati, il sistema unificato ha sistematicamente superato metodi standard come regressione logistica, support vector machine, random forest, modelli di sopravvivenza di Cox classici e reti neurali più semplici. Ha raggiunto circa il 98–99% di accuratezza nella classificazione del tipo di recidiva e un elevato indice di concordanza—una misura consolidata di quanto bene l’ordine di sopravvivenza previsto corrisponda alla realtà. Esperimenti cross‑dataset, in cui il modello è stato addestrato su una coorte e testato su un’altra, hanno dimostrato che generalizza meglio rispetto ad approcci concorrenti. Per evitare che diventasse una “scatola nera” misteriosa, gli autori hanno anche impiegato strumenti di spiegazione che evidenziano quali caratteristiche hanno influenzato maggiormente ogni previsione. Dimensione del tumore, stato HER2, fumo, stato menopausale, età alla diagnosi e mutazioni BRCA1 sono emerse come particolarmente importanti, in linea con la comprensione medica attuale.
Cosa significa per pazienti e medici
Il messaggio principale dello studio è che un singolo sistema di IA, progettato con cura, può integrare molteplici filoni di informazione per offrire un quadro più ricco e affidabile del rischio di recidiva del cancro al seno e della sopravvivenza. Pur necessitando ancora di test prospettici in contesti clinici reali, il framework potrebbe un giorno aiutare i medici a personalizzare i piani di sorveglianza, scegliere i trattamenti e informare le pazienti con maggiore sicurezza. Per le pazienti, questo potrebbe tradursi in programmi di follow‑up più aderenti al loro vero livello di rischio—riducendo ansia e accertamenti inutili per alcune, e segnalando altre che potrebbero beneficiare di monitoraggi più ravvicinati o di terapie più aggressive.
Citazione: Malik, S., Patro, S.G.K., Al-Nussairi, A.K.J. et al. A unified multi modal transformer framework for breast cancer recurrence prediction and survival analysis. Sci Rep 16, 8334 (2026). https://doi.org/10.1038/s41598-026-37046-4
Parole chiave: recidiva del cancro al seno, predizione della sopravvivenza, apprendimento profondo multimodale, modello transformer, oncologia personalizzata