Clear Sky Science · it
Potenziali biomarcatori per l’infiammazione parodontale precoce: indagine su cellule B CD5+, citochine salivari e microbioma orale
Perché le tue gengive sono importanti per tutto il corpo
Le gengive che sanguinano sono facili da ignorare, ma l’infiammazione che le causa può erodere silenziosamente l’osso che sostiene i denti ed è collegata a malattie cardiache, diabete e altre patologie. Questo studio si è chiesto se i segnali d’allarme precoci di tale danno possano essere rilevati in un campione di uso quotidiano — la saliva — insieme ad alcune cellule immunitarie nel sangue e al mix di batteri che si annidano sotto il margine gengivale. Individuare marcatori precoci affidabili potrebbe aiutare i dentisti a segnalare i pazienti ad alto rischio molto prima che si verifichi una perdita dentale irreversibile.
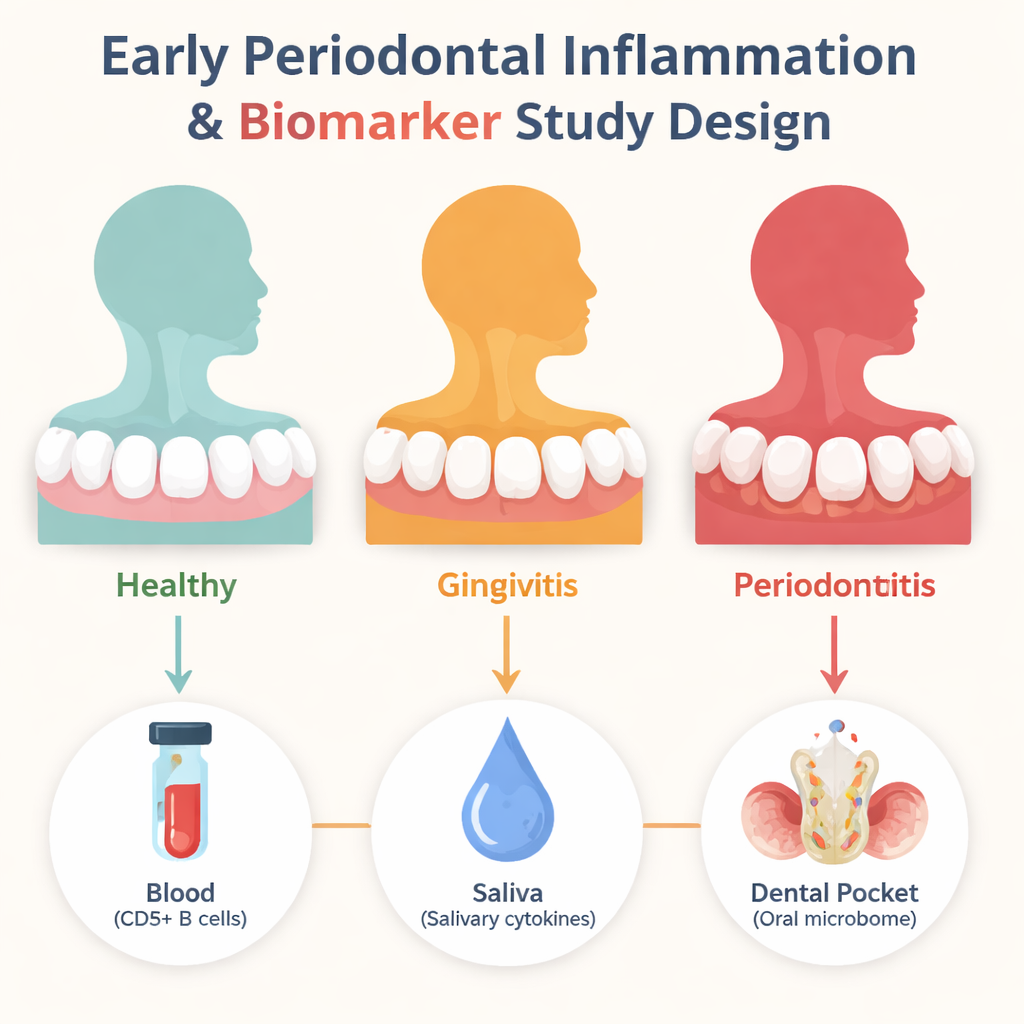
Alla ricerca dei primi segnali d’allarme
I ricercatori si sono concentrati su tre tipi di indizi. In primo luogo, hanno esaminato un gruppo speciale di cellule immunitarie nel sangue chiamate cellule B CD5-positive, che nelle fasi avanzate della malattia parodontale e nell’artrite reumatoide sono state associate alla perdita ossea e a risposte autoimmuni. In secondo luogo, hanno misurato dozzine di proteine segnalatrici, o citochine, nella saliva che fungono da allarmi chimici quando i tessuti sono irritati. In terzo luogo, hanno sequenziato il DNA batterico del fluido prelevato dalle tasche gengivali per vedere come il microbioma orale cambia quando la salute evolve in gengivite e poi in parodontite moderata. Sessanta adulti non fumatori sono stati raggruppati con cura come sani, affetti da gengivite o da parodontite cronica moderata in base alla profondità delle tasche gengivali, al sanguinamento e ai punteggi di placca.
Le cellule immunitarie nel sangue restano tranquille
Alla luce di studi precedenti sulla malattia avanzata, il team si aspettava che le persone con parodontite potessero già mostrare livelli elevati di cellule B CD5-positive nel sangue, a indicare una reazione sistemica all’infezione cronica gengivale. Sorprendentemente, il conteggio totale di queste cellule è risultato sostanzialmente lo stesso nei tre gruppi, intorno a un quinto di tutte le cellule B. Anche quando gli scienziati le hanno suddivise in stadi di sviluppo — immature, naive e diversi tipi di cellule della memoria — non è emerso alcuno schema chiaro con significatività statistica. Alcune cellule della memoria, in particolare quelle legate a risposte durature, tendevano a essere meno numerose nelle persone con malattia, suggerendo che potrebbero lasciare il sangue per accumularsi nel tessuto gengivale infiammato, ma saranno necessari studi più ampi per confermare questa sfumata tendenza.
Saliva e batteri raccontano una storia più chiara
Al contrario, la saliva e la comunità batterica sotto le gengive riflettevano chiaramente lo stadio della malattia. Le persone con parodontite avevano circa il doppio del livello mediano della chemochina IL-8 nella saliva rispetto ai partecipanti sani o con gengivite, e avevano molta più probabilità di presentare livelli rilevabili di IL-17A oltre a segni di attività di IL-6 e IL-1β. Queste molecole richiamano cellule immunitarie e promuovono processi di riassorbimento osseo, quindi il loro aumento suggerisce che circuiti infiammatori sono già attivi anche nella malattia moderata. Allo stesso tempo, il sequenziamento del DNA ha mostrato che le bocche sane erano dominate da batteri innocui e amanti dell’ossigeno come Rothia e Streptococcus. Con la gengivite e soprattutto con la parodontite, l’equilibrio è passato verso specie gram-negative, abitudinarie in ambienti poveri di ossigeno, tra cui Tannerella, Fusobacterium, Treponema e Fretibacterium, note o emergenti responsabili della degradazione gengivale.
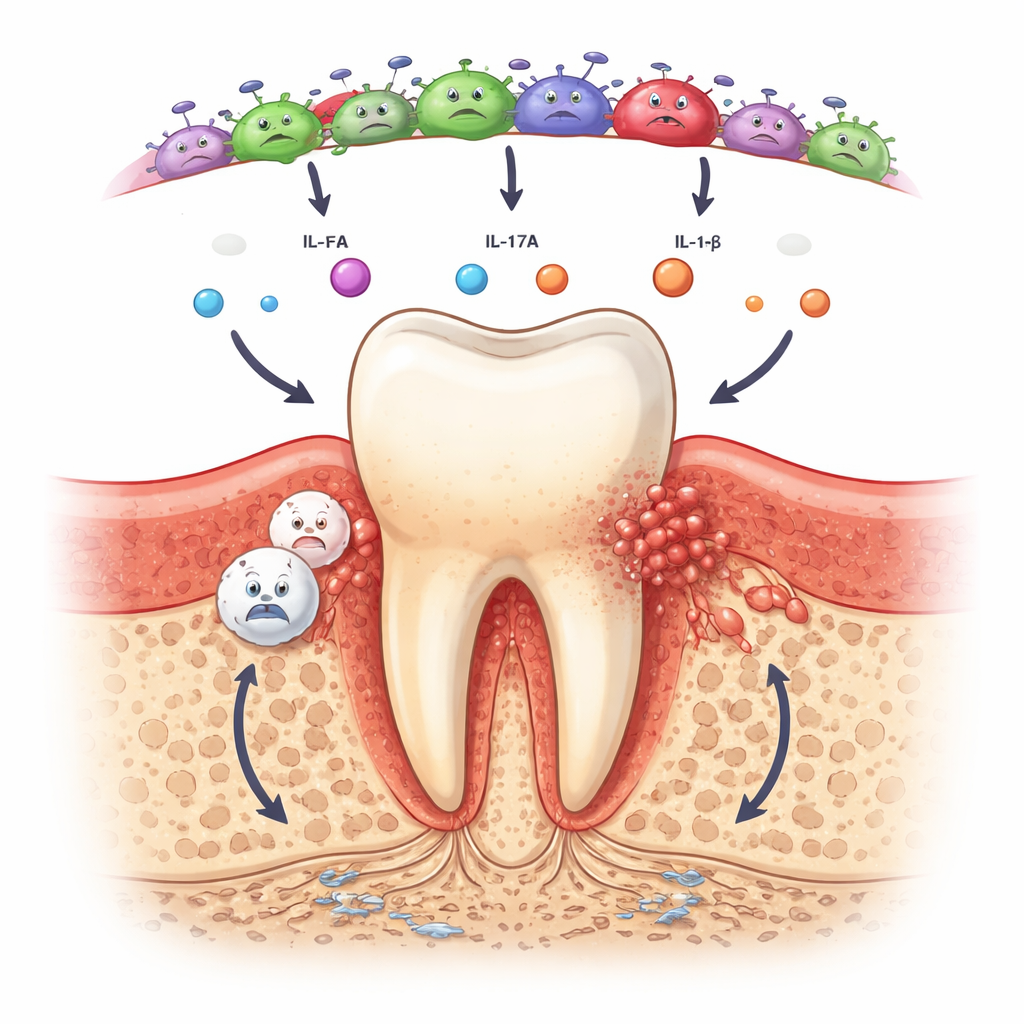
Primi indizi di un profilo ad alto rischio
Combinando statistica e apprendimento automatico, il team ha identificato gruppi batterici che separavano al meglio siti sani da siti malati. Due ceppi di Tannerella forsythia e diverse specie di Fretibacterium sono emersi come particolarmente informativi, mentre una specie di Rothia segnalava gengive più sane. Un risultato intrigante è venuto dal gruppo con gengivite: i livelli di IL-8 nella saliva seguivano da vicino l’abbondanza di un genere batterico chiamato Megasphaera. Questo legame non è apparso nelle bocche sane né nella parodontite conclamata, suggerendo che Megasphaera insieme a IL-8 potrebbe fungere da indicatore di primo stadio quando il danno è ancora limitato e potenzialmente reversibile. Tuttavia, la dimensione del campione era modesta e gli autori sottolineano che tali pattern devono essere testati in studi più ampi e a lungo termine prima di poter guidare la pratica clinica.
Cosa significa per i pazienti
Per chi è preoccupato per le proprie gengive, il messaggio principale è che il corpo invia segnali biochimici precoci di allarme, ma questi si manifestano più nella saliva locale e nel microbioma gengivale che nelle cellule immunitarie circolanti quando la malattia è ancora moderata. I normali esami del sangue per le cellule B CD5-positive probabilmente non segnaleranno una parodontite precoce. L’approccio più promettente potrebbe essere invece un pannello combinato saliva–microbioma che monitora diverse citochine — in particolare IL-8 e IL-17A — insieme a specie batteriche chiave come Tannerella, Fretibacterium e Megasphaera. Se convalidato, un test semplice basato sulla bocca potrebbe aiutare i dentisti a individuare prima i pazienti ad alto rischio, personalizzare pulizie e terapie e forse prevenire sia la perdita dei denti sia alcuni dei problemi di salute più ampi legati all’infiammazione gengivale cronica.
Citazione: Gottschalk, E.C., Chabanovska, O., Vasudevan, P. et al. Potential biomarkers for early periodontal inflammation: investigating CD5+ B cells, salivary cytokines and oral microbiome. Sci Rep 16, 7192 (2026). https://doi.org/10.1038/s41598-026-37044-6
Parole chiave: malattia gengivale, microbioma orale, biomarcatori salivari, parodontite, infiammazione