Clear Sky Science · it
Predizione con apprendimento automatico della trasformazione emorragica dopo trombectomia tramite DSA quantitativa
Perché questo è importante per i pazienti con ictus
Quando una persona subisce un ictus grave, i medici talvolta possono rimuovere il coagulo dall’arteria principale del cervello con un dispositivo molto piccolo in una procedura chiamata trombectomia meccanica. Questo ha rivoluzionato l’assistenza per l’ictus, ma molti pazienti continuano ad avere esiti sfavorevoli perché alcuni sviluppano nuovi sanguinamenti nel cervello. Lo studio descritto in questo articolo pone una domanda semplice ma cruciale: possiamo usare le informazioni che i medici già raccolgono in sala operatoria, insieme alle moderne tecniche di apprendimento automatico, per prevedere quali pazienti hanno più probabilità di sanguinare e necessitare di protezione aggiuntiva?
Guardare oltre “arteria aperta o chiusa”
Oggi il successo dopo la trombectomia viene solitamente valutato in base a se l’arteria occlusa appare di nuovo aperta all’angiografia, una specie di filmato in tempo reale dei vasi sanguigni. Ma questa valutazione grossolana non rivela che cosa accade nei piccoli vasi a valle del cervello, dove si verificano realmente i danni e i sanguinamenti. Alcuni pazienti con una perfetta riapertura dei grandi vasi sviluppano comunque emorragie cerebrali gravi, una complicanza chiamata trasformazione emorragica. Gli autori hanno ipotizzato che misurazioni più dettagliate del flusso di sangue in questi piccoli vasi, ricavate dallo stesso angiogramma, potessero contenere indizi nascosti su chi è a rischio.
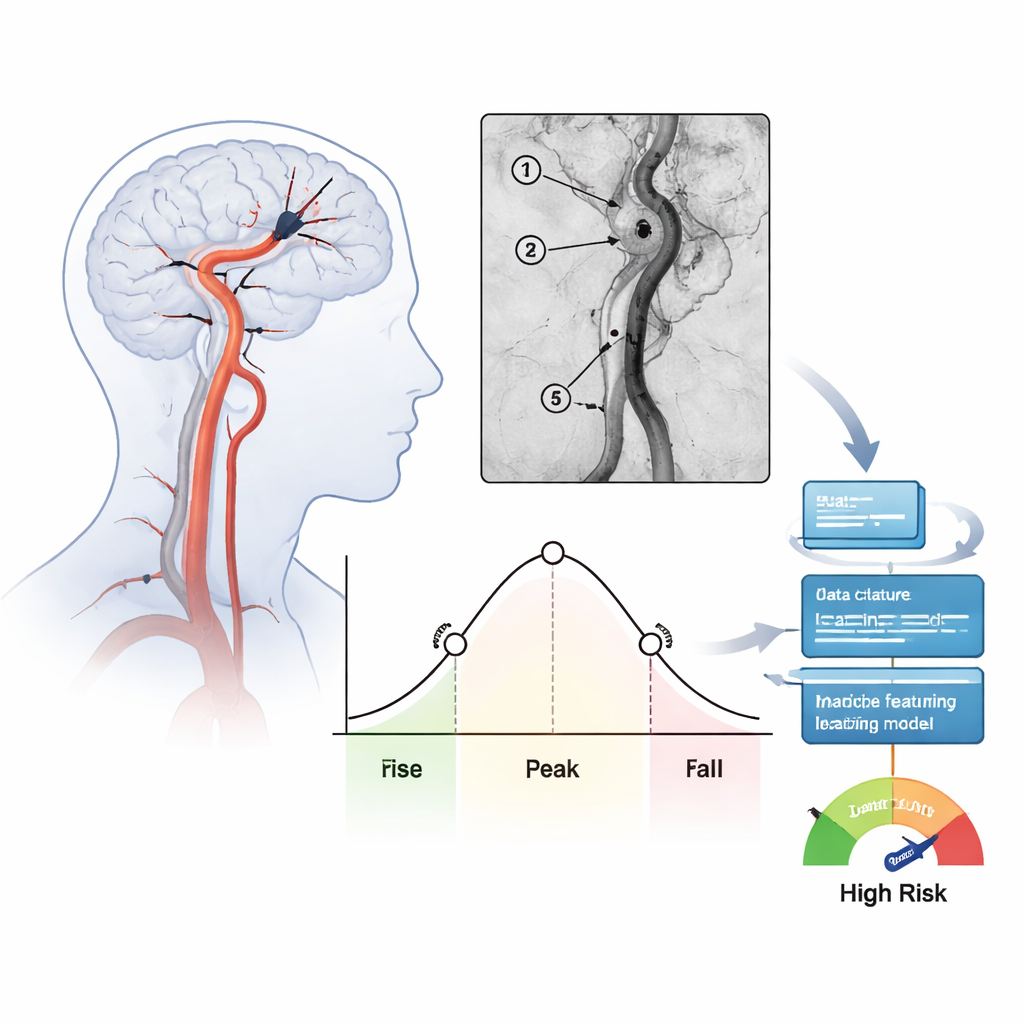
Trasformare i filmati angiografici in numeri
Il gruppo ha studiato 171 persone trattate per ictus severi nella parte anteriore del cervello in un anno, in un unico ospedale. Dopo che i medici hanno rimosso il coagulo e ripristinato il flusso, hanno registrato le viste angiografiche standard e poi analizzato come il mezzo di contrasto iniettato si affacciava e defluiva in diversi punti chiave lungo l’arteria trattata. Per ogni regione hanno calcolato misure temporali come il tempo medio di transito e l’ampiezza della principale ondata di contrasto (full width at half maximum). Questi numeri sintetizzano se il sangue scorre lentamente e in modo uniforme o passa velocemente in un impulso concentrato. In totale sono state estratte 39 caratteristiche di flusso per ogni paziente e verificate la consistenza tra valutatori indipendenti.
Insegnare al computer a riconoscere i modelli a rischio
I ricercatori hanno quindi utilizzato un insieme di metodi comuni di apprendimento automatico per verificare se queste caratteristiche di flusso, da sole o combinate con dati clinici di base come età e gravità dell’ictus, potessero distinguere i pazienti che in seguito hanno sviluppato sanguinamento cerebrale da quelli che non l’hanno fatto. Per evitare l’overfitting, hanno prima applicato cinque diverse tecniche di selezione delle caratteristiche per scegliere le misure più informative, e hanno ripetutamente suddiviso i dati in gruppi di addestramento e di test con validazione incrociata. Tra le molte combinazioni testate, un modello relativamente semplice — regressione logistica, ottimizzata con un filtro di caratteristiche “Elastic Net” — ha dato le migliori prestazioni. Quando si è basato solo sulle misure di flusso derivanti dall’angiografia, ha separato correttamente pazienti con e senza emorragia con un’area media sotto la curva ROC di circa 0,81. Con l’aggiunta di fattori clinici, la performance è salita a circa 0,86, suggerendo che il modello potrebbe diventare un utile ausilio decisionale.
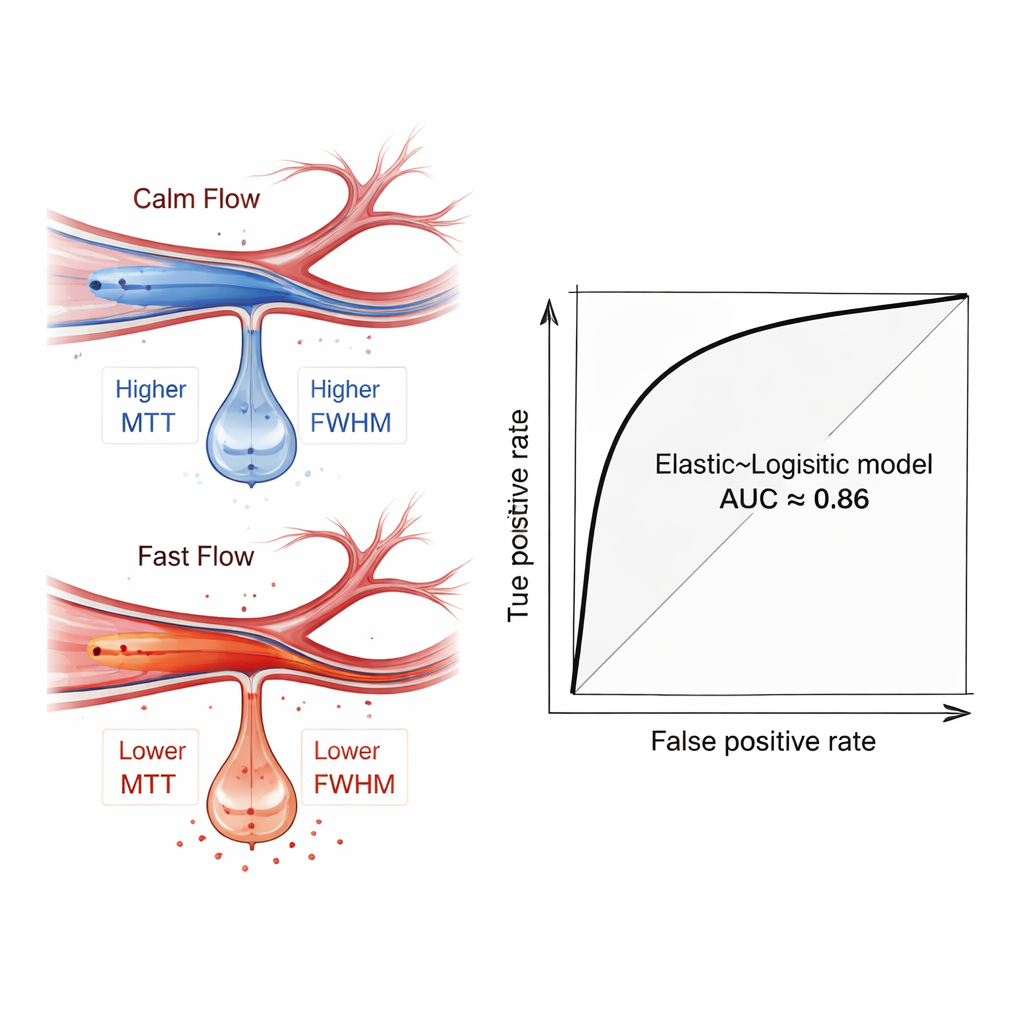
Cosa hanno rivelato i segnali del flusso sanguigno
Analizzando i modelli addestrati, gli autori hanno usato una tecnica di interpretabilità chiamata SHAP per vedere quali caratteristiche erano più importanti. Le misure che catturavano quanto fosse prolungato e quanto fosse disperso l’impulso di flusso — specialmente in un ramo più distante dell’arteria cerebrale media — sono emerse come predittori chiave. I pazienti che in seguito hanno sanguinato tendevano a mostrare un flusso più rapido e più concentrato in questi vasi distali, riflesso da tempi di transito inferiori e picchi più stretti. Questo schema è un’impronta emodinamica di “iperperfusione”, uno stato in cui tessuto cerebrale fragile, improvvisamente irrorato da sangue ad alta velocità dopo essere stato privato, è più propenso a perdere fluidi e sanguinare. È importante sottolineare che questo segnale è emerso anche quando semplici confronti di gruppo non mostravano differenze statistiche marcate, sottolineando il valore di un’analisi multicaratteristica e guidata dalla macchina.
Come questo potrebbe cambiare la cura al letto del paziente
Poiché il metodo utilizza immagini già acquisite durante la trombectomia, non richiede esami aggiuntivi, altro mezzo di contrasto o radiazioni. Una volta tracciate le regioni di interesse — un passaggio che attualmente richiede pochi minuti — il computer può calcolare automaticamente le misure di flusso e generare una stima personalizzata del rischio di sanguinamento. In linea di principio, questo potrebbe aiutare i medici a personalizzare gli obiettivi pressori, decidere quanto aggressivamente usare farmaci anticoagulanti e programmare TC più precoci per i pazienti segnalati ad alto rischio. Gli autori avvertono che il loro studio è retrospettivo e proveniente da un singolo centro, quindi sono necessari trial più ampi e multicentrici prima che lo strumento possa guidare la pratica clinica di routine. Tuttavia, offre una chiara prova di concetto: trasformando gli angiogrammi dell’ictus in ricchi dati numerici e lasciando che l’apprendimento automatico li analizzi, possiamo andare oltre la semplice domanda “L’arteria è aperta?” verso “La microcircolazione cerebrale è sicura?” — uno spostamento che potrebbe in ultima analisi risparmiare a più pazienti sanguinamenti pericolosi dopo il trattamento.
Citazione: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Parole chiave: ictus, trombectomia meccanica, emorragia cerebrale, apprendimento automatico, angiografia