Clear Sky Science · it
Impatto dei trattamenti sistemici specifici per le neoplasie neuroendocrine sull’espressione e la funzione di CXCR4 nelle cellule dei tumori neuroendocrini
Perché è importante per la cura del cancro in futuro
Quando alcuni rari tumori dell’intestino e del pancreas diventano più aggressivi, spesso smettono di rispondere ai trattamenti mirati standard. Medici e ricercatori hanno urgente bisogno di nuovi modi per visualizzare e colpire questi tumori più difficili. Questo studio pone una domanda pratica dalle grandi implicazioni: i chemioterapici e i farmaci mirati che i pazienti già ricevono modificano un marcatore tumorale chiave chiamato CXCR4, che è in sviluppo sia come “segnalatore” diagnostico sia come bersaglio terapeutico?
Un bersaglio che cambia nelle cellule tumorali aggressive
Le neoplasie neuroendocrine sono tumori rari che originano da cellule produttrici di ormoni, più frequentemente nell’intestino e nel pancreas. Nelle loro forme iniziali e più ordinate, questi tumori di solito esprimono sulla superficie un recettore chiamato recettore della somatostatina 2, che i medici possono visualizzare e trattare con farmaci radioattivi specializzati. Quando la malattia diventa più aggressiva, questi tumori tendono a perdere quel marcatore, rendendoli più difficili da rilevare e colpire. Allo stesso tempo, molti attivano un altro marcatore di superficie, un recettore chiamato CXCR4, associato a crescita più rapida, diffusione a organi distanti e peggiore sopravvivenza. Poiché CXCR4 può essere visualizzato con un tracciante PET e potenzialmente attaccato con farmaci radioattivi o a base di anticorpi, è emerso come un promettente bersaglio “di riserva” quando le opzioni standard falliscono.
Testare farmaci del mondo reale in modelli cellulari tumorali
I ricercatori hanno voluto sapere come i farmaci già usati per trattare i tumori neuroendocrini di alto grado influenzino lo stesso CXCR4. Se queste medicine riducessero involontariamente CXCR4, potrebbero indebolire future strategie diagnostiche o terapeutiche mirate a CXCR4—ma potrebbero anche contribuire a frenare l’aggressività del tumore. Il gruppo ha lavorato con tre diverse linee cellulari umane che rappresentano forme aggressive della malattia, inclusa una linea ibrida che imita da vicino i tumori particolarmente difficili da trattare. Hanno esposto queste cellule a sei agenti comuni: le chemioterapie cisplatino, etoposide, streptozotocina, 5‑fluorouracile, il farmaco orale temozolomide e l’inibitore mirato mTOR everolimus. Dopo il trattamento, hanno misurato CXCR4 a livello genetico e proteico e testato quanto bene le cellule riuscissero ancora ad assorbire un tracciante PET che cerca CXCR4.
Alcuni farmaci attenuano il segnale CXCR4
I risultati hanno mostrato che non tutti i farmaci antitumorali sono uguali rispetto a questo recettore. Il cisplatino ha chiaramente ridotto l’attività genetica di CXCR4 in due delle tre linee cellulari e ha significativamente ridotto l’assorbimento del tracciante in due, il che significa che c’erano meno recettori funzionanti a cui il tracciante potesse legarsi. Anche temozolomide ed everolimus hanno abbassato i livelli genetici e proteici di CXCR4 in diversi tipi cellulari, sebbene ciò non si sia sempre tradotto in una diminuzione statisticamente chiara dell’assorbimento del tracciante. Invece etoposide e streptozotocina hanno avuto poco effetto su CXCR4, mentre il 5‑fluorouracile ha prodotto cambiamenti modesti che non hanno alterato fortemente il legame del tracciante. Nel complesso, il quadro suggerisce che cisplatino, temozolomide ed everolimus possono tutti attenuare CXCR4 in queste cellule tumorali aggressive, mentre gli altri agenti lo lasciano per lo più invariato.
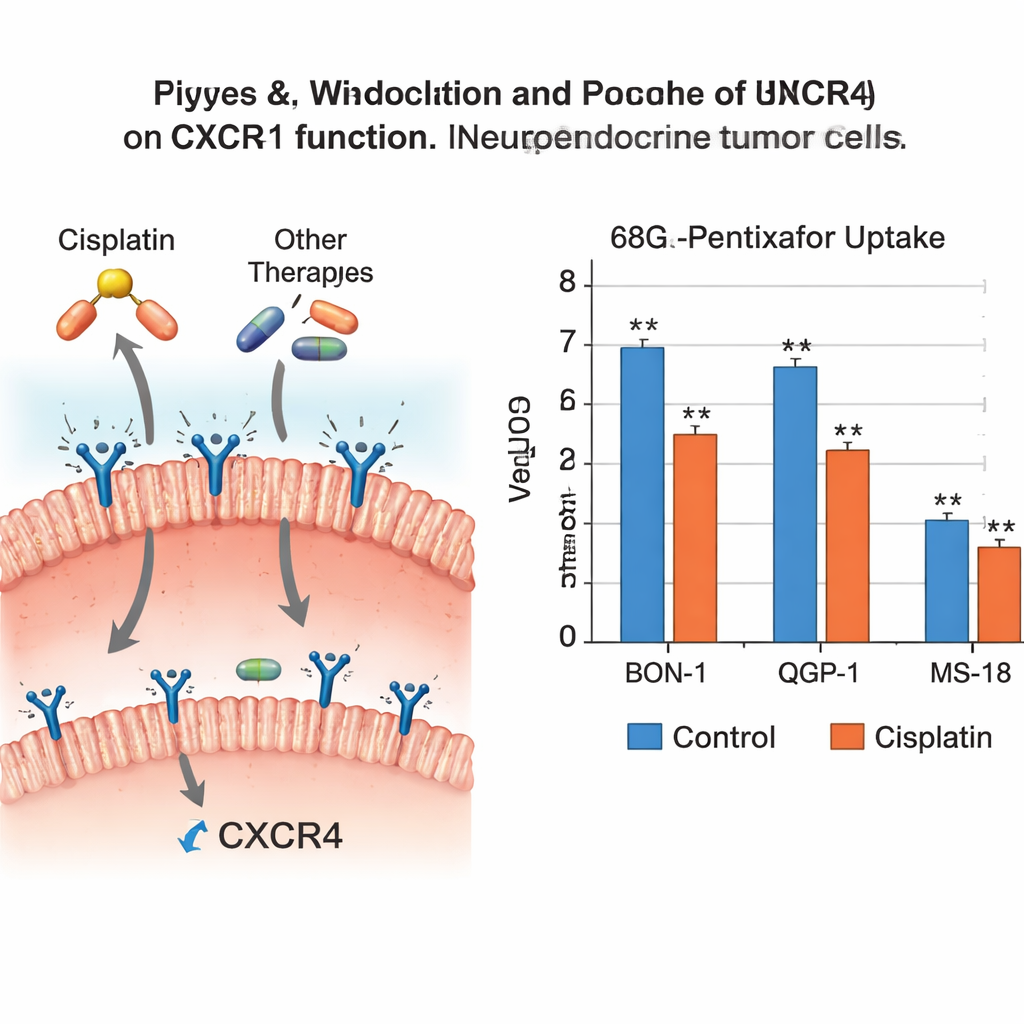
Cosa significa per le scansioni e il timing dei trattamenti
Questi risultati portano un duplice messaggio per la cura futura dei pazienti. Da un lato, l’attenuazione di CXCR4 può far parte del modo in cui farmaci come cisplatino, temozolomide ed everolimus rallentano la diffusione tumorale, perché un’elevata espressione di CXCR4 è legata a invasività e metastasi. Dall’altro lato, se il CXCR4 di un tumore è soppresso dal trattamento in corso, le PET basate su CXCR4 potrebbero sottostimare l’estensione della malattia e le terapie radioattive mirate a CXCR4 potrebbero avere meno siti di aggancio disponibili. Lo studio suggerisce che combinare direttamente terapie mirate a CXCR4 con questi farmaci sistemici è improbabile che migliori l’efficacia delle terapie focalizzate su CXCR4 e potrebbe persino attenuarle.
Un nuovo tassello per la terapia personalizzata
Per i non specialisti, il punto chiave è che un singolo marcatore tumorale può avere due ruoli contemporaneamente: può essere un segnale di malattia aggressiva e, allo stesso tempo, una leva utile per l’imaging e il trattamento mirato. Questa ricerca mostra che alcuni farmaci consolidati contro il cancro possono modificare discretamente quel marcatore verso l’alto o verso il basso. In pratica, ciò potrebbe influenzare quando programmare le scansioni e le terapie basate su CXCR4—idealmente quando il recettore è più abbondante—e può aiutare a spiegare perché certi trattamenti sono efficaci contro tumori neuroendocrini a crescita rapida. Pur provenendo da modelli cellulari e richiedendo conferme nei pazienti, questi risultati rappresentano un passo importante verso un sequenziamento più intelligente delle terapie per le persone con questi tumori difficili da trattare.
Citazione: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Parole chiave: tumori neuroendocrini, CXCR4, cisplatino, everolimus, imaging mirato