Clear Sky Science · it
Sequenziamento di ampliconi con Oxford Nanopore Technologies come alternativa diagnostica per i lentivirus dei piccoli ruminanti nelle pecore
Infezioni nascoste nelle pecore di tutti i giorni
Le pecore in tutto il mondo ospitano silenziosamente virus che possono intaccare la loro salute, accorciarne la vita e costare denaro agli allevatori—spesso senza sintomi evidenti per anni. Questo studio esplora un nuovo modo per scovare quelle infezioni nascoste utilizzando una tecnologia portatile di sequenziamento del DNA, offrendo un potenziale salto qualitativo nel modo in cui proteggiamo il benessere animale, il reddito zootecnico e persino la sicurezza alimentare.
Una malattia lenta, costosa e difficile da individuare
Il lavoro si concentra sui lentivirus dei piccoli ruminanti (SRLV), un gruppo di virus che infettano pecore e capre. Nelle pecore causano la malattia Maedi-Visna, un’infezione a lunga durata che può portare a problemi respiratori, artrite, encefalopatia e infiammazione cronica della mammella. Molti animali infetti non mostrano mai segni chiari, ma il virus comunque riduce la produzione di latte, aumenta la mortalità degli agnelli e impone lo smeriglio precoce. In alcune mandrie da latte europee, incluse Spagna e Grecia, circa la metà degli animali può essere infettata, rendendo questa una delle malattie più rilevanti nelle aziende ovine intensive.
Perché i test attuali non rilevano molti animali infetti
Oggi, gli allevamenti si affidano principalmente a esami del sangue che cercano anticorpi (ELISA) o ai test genetici standard (qPCR) per decidere quali animali sono infetti e devono essere rimossi dal gregge. Ma gli SRLV mutano e ricombinano rapidamente, generando molte varianti virali leggermente diverse. Alcune varianti sono poco riconosciute dai test sierologici, e alcuni animali infetti non sviluppano risposte anticorpali robuste. La qPCR, che mira a frammenti virali brevi e molto specifici, può fallire se quelle regioni bersaglio cambiano. Di conseguenza, molti animali realmente infetti risultano negativi e restano nel gregge, diffondendo il virus in modo silenzioso.
Usare la lettura del DNA in tempo reale per trovare il virus
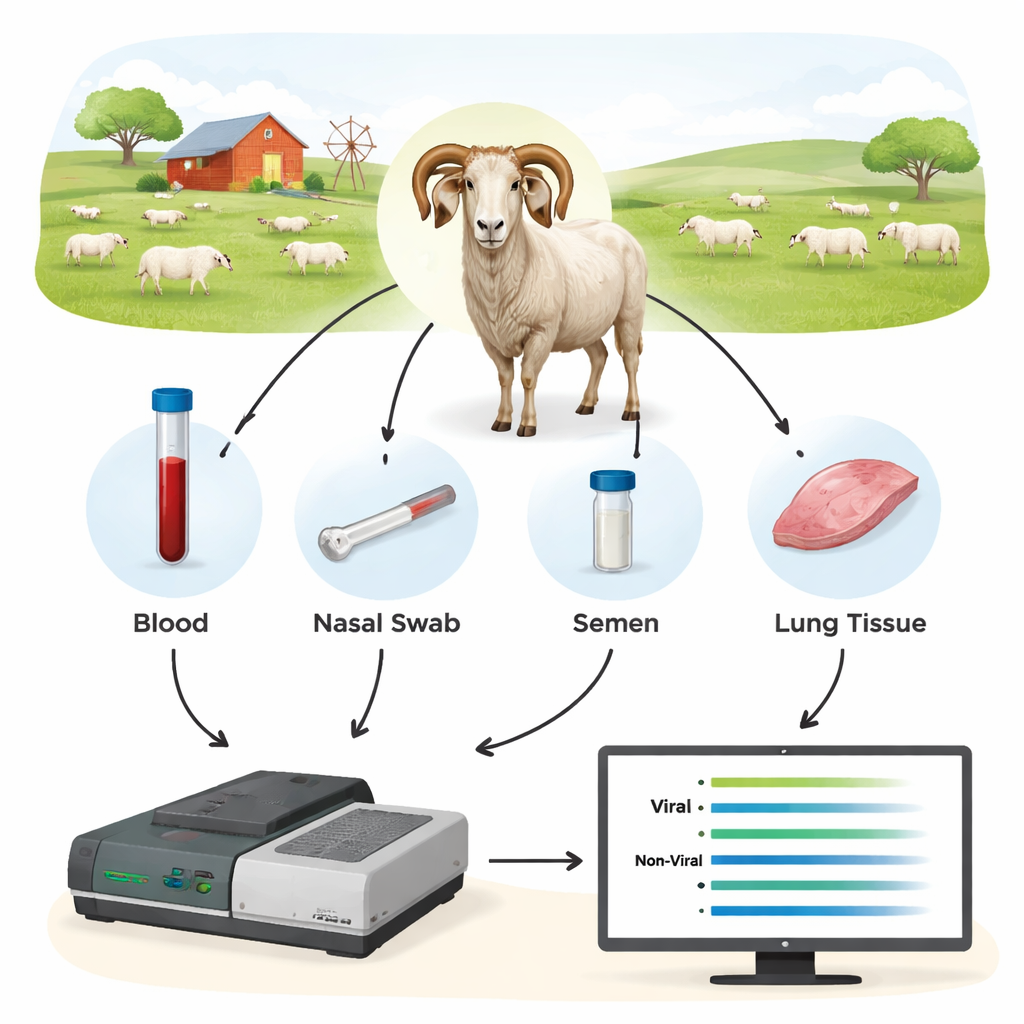
I ricercatori hanno testato un metodo di terza generazione chiamato sequenziamento Oxford Nanopore come nuovo strumento diagnostico. Invece di cercare un singolo e minuscolo frammento di DNA virale, hanno prima amplificato tratti più lunghi di geni virali chiave dai campioni degli animali e poi hanno sequenziato quei frammenti in tempo reale su un dispositivo Nanopore. Hanno raccolto sangue, tamponi nasali, seme e cellule da sangue e polmoni da 44 montoni e pecore aggiuntive, molte delle quali erano già state testate con metodi convenzionali. Concentrandosi su regioni virali relativamente conservate ma sufficientemente lunghe da rivelare la ceppa esatta, il team è riuscito sia a rilevare l’infezione sia a identificare quali tipi virali erano presenti.
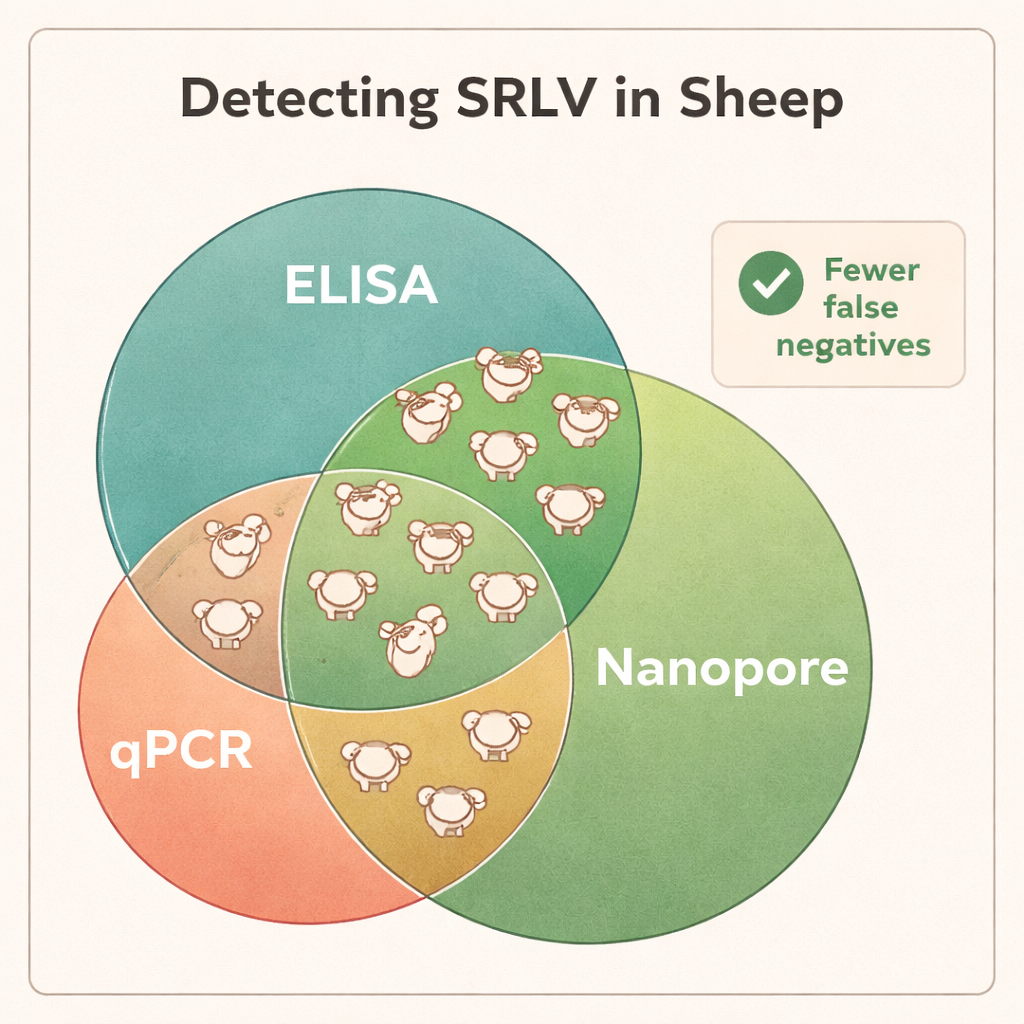
Il sangue funziona meglio—e scopre ciò che altri test perdono
Il sequenziamento ha mostrato che il DNA proveniente dal sangue intero era il materiale più affidabile per scoprire gli SRLV, anche se il virus vive principalmente in un piccolo sottoinsieme di globuli bianchi. Il tessuto polmonare di animali fortemente infetti forniva quantità molto elevate di DNA virale, ma tali campioni sono disponibili solo dopo la macellazione. Al contrario, i tamponi nasali, il seme e i globuli bianchi purificati offrivano troppo poco materiale virale per una diagnostica consistente. Quando gli scienziati hanno confrontato i risultati Nanopore con i test standard ELISA e qPCR, le differenze sono state nette: il sequenziamento Nanopore ha confermato l’infezione in tutti i montoni ELISA-positivi ma ha anche rivelato che molti animali ELISA-negativi erano in realtà infetti. Tra i diversi greggi, all’incirca il 40–45% degli animali etichettati come “negativi” dall’ELISA si è rivelato portatore del virus, e la qPCR ha mancato una frazione ancora maggiore. I dati di sequenziamento hanno inoltre messo in luce co-infezioni con diversi tipi di SRLV in alcuni montoni, informazione che i test tradizionali non forniscono facilmente.
Da risposte semplici sì/no a intuizioni più profonde
Poiché il Nanopore legge le sequenze virali reali, può andare oltre una semplice diagnosi binaria. Il team ha usato i dati per confrontare ceppi virali, costruire alberi filogenetici dei virus circolanti nei loro greggi e studiare differenze sottili nelle proteine virali che potrebbero spiegare perché alcuni animali sfuggono al rilevamento da parte dei kit ELISA standard. Hanno dimostrato che certe versioni di una proteina virale chiave, bersaglio dei test anticorpali commerciali, differiscono in modo rilevante tra animali anticorpo-positivi e anticorpo-negativi. Col tempo, tali informazioni potrebbero aiutare a perfezionare sia i test sierologici sia i programmi di allevamento volti a selezionare animali naturalmente più resistenti all’infezione.
Cosa significa questo per gli allevatori e la salute animale
Per i non specialisti, il messaggio principale è semplice: leggendo frammenti più lunghi di DNA virale direttamente, il sequenziamento Nanopore può scoprire più pecore infette, prima e con maggiore precisione, rispetto ai test di routine attuali. Inoltre indica quali ceppi virali esatti sono presenti in un gregge. Sebbene questo approccio sia ancora più complesso e costoso rispetto a un singolo esame del sangue, la tecnologia sta diventando più veloce, economica e portatile. Se integrata nei programmi di controllo, potrebbe ridurre drasticamente il numero di portatori “nascosti”, migliorare la progettazione di vaccini e test e favorire l’allevamento di animali più resistenti—rendendo l’allevamento ovino più sostenibile e umano.
Citazione: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Parole chiave: salute delle pecore, lentivirus, sequenziamento nanopore, diagnostica veterinaria, Maedi-Visna