Clear Sky Science · it
Nanoparticelle antimicrobiche ad ampio spettro con bassa tossicità per prevenire la formazione di biofilm sui dispositivi urologici
Perché gli impianti medici a volte si rivoltano contro di noi
La medicina moderna si affida a tubi di plastica e impianti per drenare l’urina, sostenere reni ostruiti e ripristinare la funzione sessuale. Tuttavia questi stessi dispositivi possono diventare calamite per i batteri, che costruiscono comunità protettive viscide chiamate biofilm. Una volta formato un biofilm, le infezioni sono difficili da trattare, spesso costringendo i medici a rimuovere o sostituire il dispositivo. Questo studio esplora un nuovo tipo di rivestimento microscopico, composto da oro e argento avvolti in un guscio di carbonio, progettato per impedire la formazione dei biofilm prima che inizino.
Il problema nascosto dei germi appiccicosi
Cateteri, stent ureterali e protesi peniene gonfiabili aiutano centinaia di migliaia di pazienti, ma offrono anche un habitat ideale per i microbi. I batteri si attaccano alla superficie del dispositivo e secernono una matrice collosa di zuccheri, proteine e grassi, formando una fortezza che li protegge dagli antibiotici e dal sistema immunitario. Di conseguenza, le infezioni correlate ai dispositivi rappresentano più di un quarto di tutte le infezioni ospedaliere e costano centinaia di milioni di dollari ogni anno. I rivestimenti protettivi attuali a base di antibiotici o semplice argento fanno fatica a prevenire i biofilm nel lungo termine e possono contribuire alla crescente resistenza agli antibiotici.
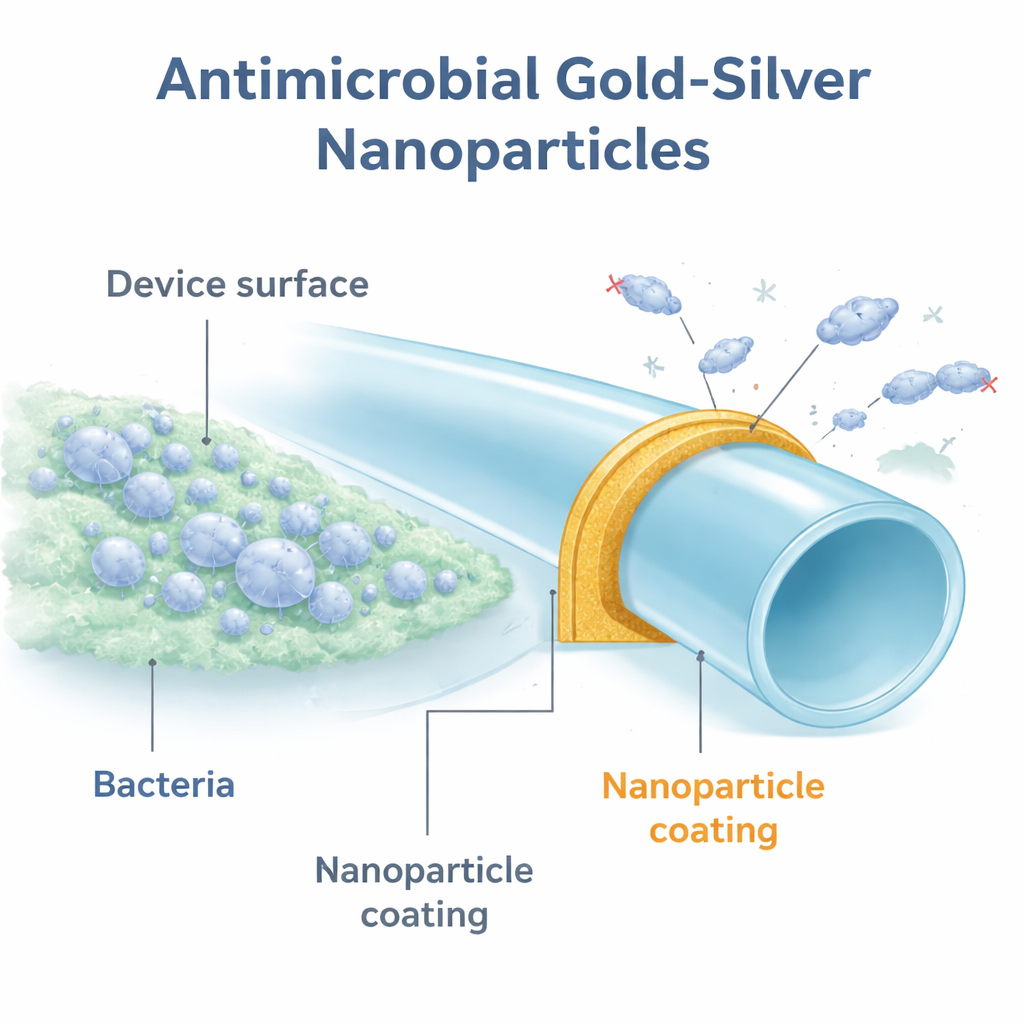
Un nuovo tipo di armatura protettiva
I ricercatori si sono concentrati su particelle metalliche piccolissime, larghe solo pochi miliardesimi di metro. Queste nanoparticelle sono state costruite attorno a un materiale a gabbia di carbonio chiamato polidrossi fullerene, noto per essere non tossico e per migliorare le prestazioni di alcuni metalli. Hanno creato diverse versioni usando metalli differenti, poi hanno rivestito piccoli dischi di poliuretano, una plastica comunemente usata nei dispositivi urologici. Quando hanno testato questi dischi rivestiti contro un ceppo standard di Escherichia coli, solo le particelle contenenti argento hanno mostrato forti effetti antibatterici. Il risultato più evidente è stata una combinazione oro–argento, indicata come GSNPs, che ha ridotto il numero di batteri fino a 100.000 volte rispetto alla plastica non rivestita.
Fermare i germi urologici del mondo reale
Per verificare se questo effetto resistesse oltre il ceppo di laboratorio, il team ha testato il loro miglior rivestimento contro sei tipi di batteri prelevati direttamente da stent ureterali e protesi peniene infetti. Questi includevano specie sia Gram-positive sia Gram-negative note per causare infezioni ostinate. A livelli batterici simili a quelli riscontrati nei pazienti, le superfici rivestite con GSNP hanno ottenuto una riduzione del 100% sia dei batteri placcati in sospensione sia di quelli aderenti alla superficie per ogni ceppo testato. In esperimenti separati, i ricercatori hanno esposto i batteri a diverse concentrazioni di nanoparticelle in soluzione e stimato quanto GSNP fosse necessario per fermarne la crescita. Tutti i ceppi sono stati completamente inibiti a o sotto i 3 microgrammi di GSNP per millilitro di liquido, con quantità leggermente superiori richieste per alcuni organismi Gram-positivi.
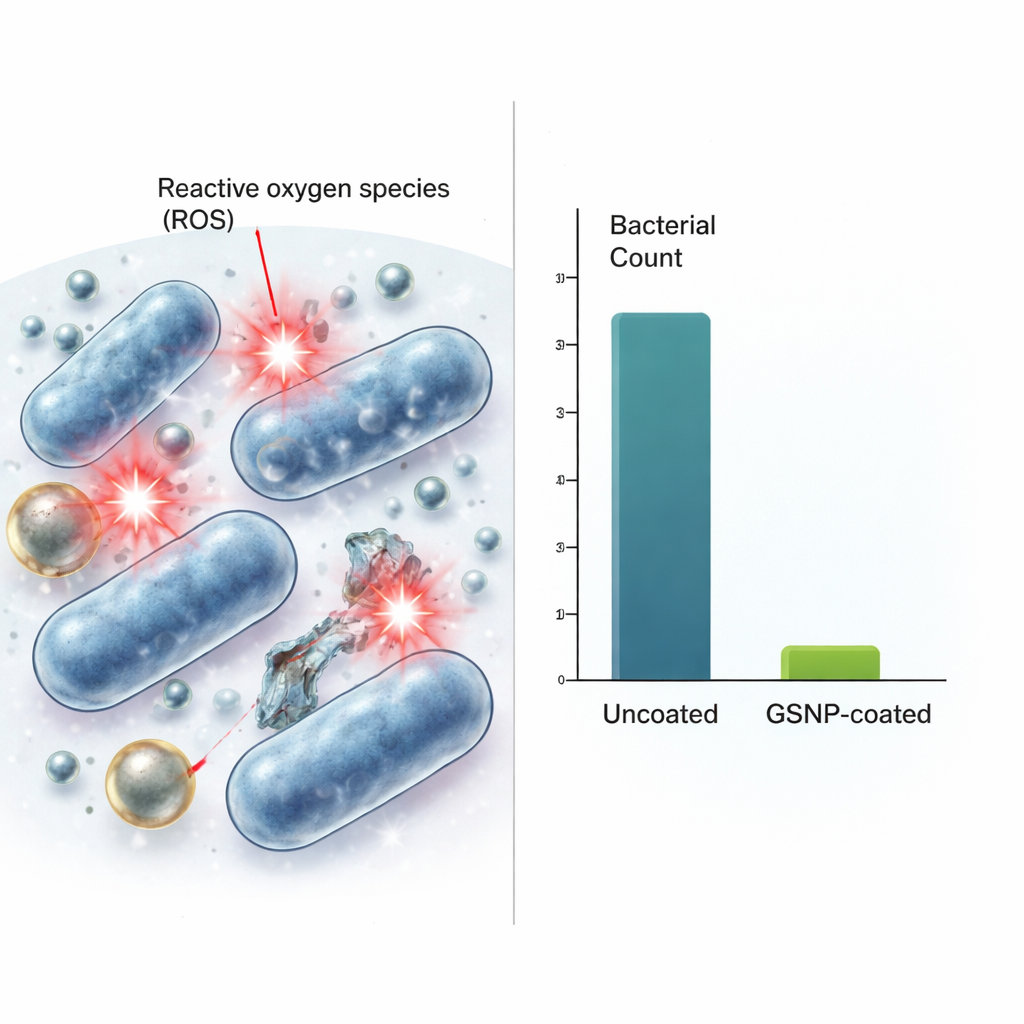
Come funzionano e quanto sono sicure
Il team ha quindi indagato come questi rivestimenti uccidano i batteri e se possano anche danneggiare le cellule umane. I dati indicano le specie reattive dell’ossigeno—forme chimicamente reattive dell’ossigeno—come parte chiave del meccanismo di uccisione. Sebbene le nanoparticelle da sole non generassero queste molecole reattive, i batteri esposti alle GSNP hanno prodotto livelli molto più alti rispetto ai batteri non trattati, suggerendo che le particelle inneschino una chimica dannosa all’interno o vicino ai microbi. Quando cellule di fibroblasti murini sono state esposte a concentrazioni simili o superiori di GSNP, oltre l’80% delle cellule è rimasto vivo alla dose antibatterica peggiore. In altre parole, i livelli che hanno eliminato i batteri hanno avuto solo un impatto modesto sulle cellule dei mammiferi. Le GSNP si sono inoltre rivelate dramaticamente più efficaci di un prodotto commerciale di nanoparticelle oro–argento testato in parallelo, ottenendo circa una riduzione di batteri di un milione di volte maggiore a dosi equivalenti.
Cosa potrebbe significare per i pazienti
Sebbene questo lavoro sia stato condotto in laboratorio e non ancora in animali o persone, i risultati indicano una strategia promettente per impianti medici più sicuri. Uno strato sottile di GSNP su un catetere o una protesi potrebbe fornire una protezione ampia contro molti batteri diversi, ridurre la necessità di rimozione del dispositivo e farlo senza fare affidamento sugli antibiotici tradizionali. Il rivestimento utilizza basse quantità di metallo, mostra una tossicità relativamente bassa nei test iniziali ed è semplice da produrre. Con ulteriori perfezionamenti per migliorare la stabilità a lungo termine e test accurati in modelli realistici, questi rivestimenti di nanoparticelle oro–argento potrebbero aiutare a mantenere i dispositivi urologici vitali funzionanti per i pazienti, invece di diventare una base per le infezioni.
Citazione: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Parole chiave: biofilm, dispositivi urologici, rivestimento antimicrobico, nanoparticelle, oro-argento