Clear Sky Science · it
Analisi proteomica quantitativa del plasma dopo conditioning ischemico remoto nell’ictus ischemico acuto
Perché stringere un braccio potrebbe aiutare a proteggere il cervello
Quando una persona subisce un ictus causato dall’ostruzione di un vaso sanguigno, ogni minuto di flusso sanguigno perso mette a rischio le cellule cerebrali. I trattamenti standard mirano a riaprire l’arteria bloccata, ma molti pazienti arrivano troppo tardi o non sono idonei. I ricercatori stanno esplorando una terapia aggiuntiva sorprendentemente semplice: interrompere brevemente il flusso sanguigno a un braccio o a una gamba con un manicotto per la pressione, una strategia chiamata conditioning ischemico remoto (RIC). Questo studio pone una domanda chiave per trasformare quell’idea in una terapia reale: cosa cambia esattamente nel sangue dei pazienti con ictus dopo il RIC e quelle modifiche potrebbero indicare chi potrebbe beneficiarne di più?
Un segnale di lieve stress inviato dall’arto al cervello
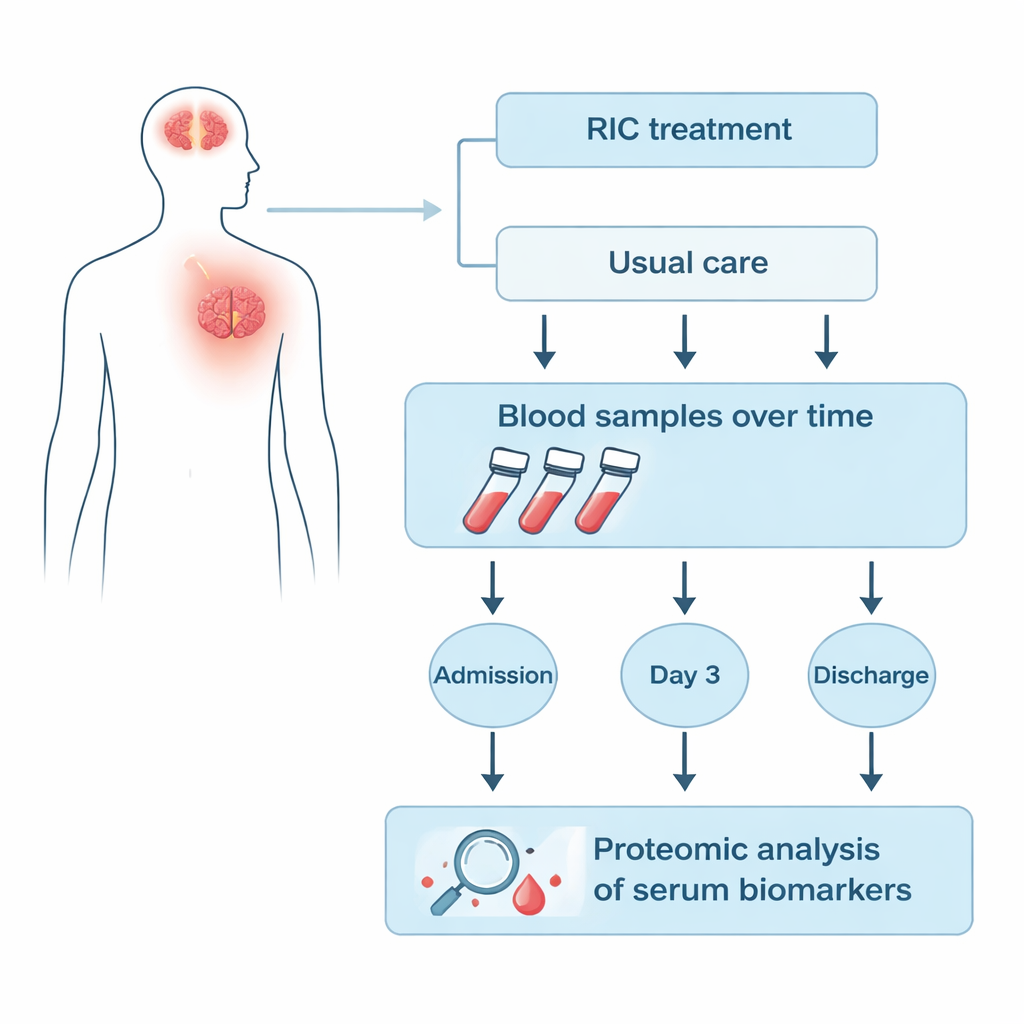
Il RIC funziona gonfiando ripetutamente un manicotto su un arto per alcuni minuti, poi sgonfiandolo, creando brevi e innocui episodi di ridotto flusso sanguigno. Esperimenti su animali e trial clinici iniziali suggeriscono che questo “stress controllato” può segnalare organi distanti, incluso il cervello, per attivare programmi di protezione. In un ampio trial clinico chiamato RICAMIS, pazienti con ictus ischemico di entità moderata che ricevettero RIC oltre alla cura usuale hanno avuto risultati migliori a 90 giorni rispetto a chi ricevette solo la cura usuale. Un altro studio (RESIST) non riportò invece tale beneficio, lasciando i medici incerti su quando e per chi il RIC funzioni davvero. Lo studio attuale analizza il sangue dei pazienti alla ricerca di indizi molecolari—proteine misurabili, o biomarcatori, che cambiano nel tempo con il RIC.
Seguire il sangue dei pazienti durante il ricovero
I ricercatori si sono concentrati su 25 pazienti del trial RICAMIS ai quali sono stati raccolti campioni di sangue in tre momenti: all’ammissione, tre giorni dopo l’assegnazione del trattamento e alla dimissione ospedaliera. Nove pazienti ricevettero RIC oltre alla cura usuale, mentre sedici ricevettero solo la cura usuale. Usando una tecnica chiamata proteomica quantitativa, il team ha misurato centinaia di proteine nella porzione sierica del sangue contemporaneamente, invece di analizzare solo pochi marker pre‑selezionati. Hanno quindi confrontato come i livelli di ciascuna proteina aumentassero o diminuissero nel tempo nel gruppo RIC rispetto al gruppo controllo per trovare firme uniche associate al RIC.
Nove segnali distintivi nel flusso sanguigno
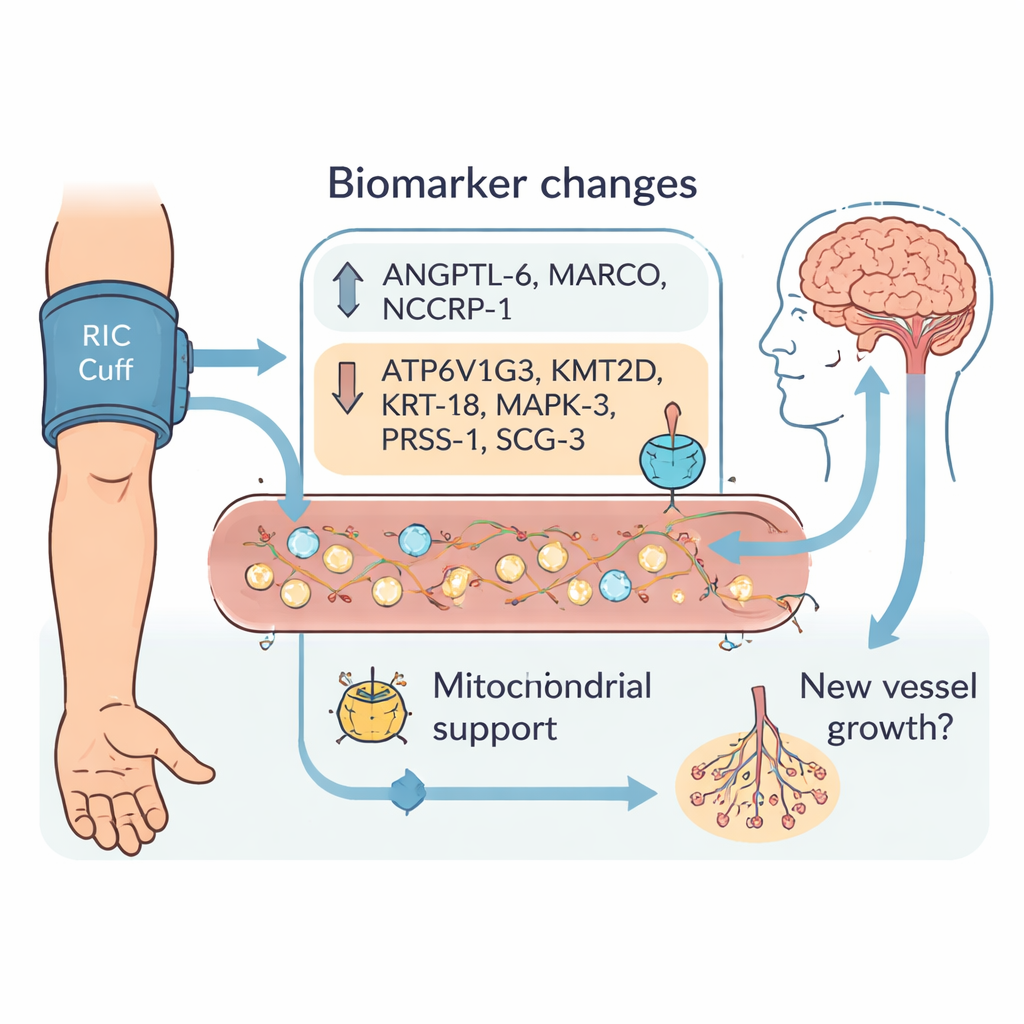
Durante il ricovero, dozzine di proteine variarono in modo differente tra i due gruppi. Dopo un accurato filtraggio, il team ha evidenziato nove biomarcatori i cui cambiamenti dall’ammissione al giorno 3 e alla dimissione separavano chiaramente i pazienti trattati con RIC dai controlli. Tre proteine—ANGPTL‑6, MARCO e NCCRP‑1—in crebbero maggiormente con il RIC. Altre sei—ATP6V1G3, KMT2D, KRT‑18, MAPK‑3, PRSS‑1 e SCG‑3—tendevano a diminuire. Molte di queste molecole sono coinvolte nella gestione dell’energia nelle centrali cellulari, i mitocondri, o nei processi di crescita e rimodellamento dei nuovi vasi sanguigni. Ciò è coerente con l’idea che il RIC non si limiti a proteggere i neuroni dal danno, ma possa aiutare le aree cerebrali lesionate a riorganizzarsi, riparare l’apporto di sangue e recuperare funzione nell’arco di giorni o settimane.
Indizi sull’uso di energia e sulla crescita vascolare
Per comprendere meglio cosa potrebbero fare queste nove proteine, gli autori le hanno mappate su vie biologiche note. Due di esse, KMT2D e MAPK‑3, sono collegate a come il DNA viene impacchettato e a come i geni vengono attivati o disattivati, in particolare nei programmi legati alla crescita dei vasi. Altre, come ATP6V1G3 e KRT‑18, sono state associate in studi precedenti al mantenimento di mitocondri sani e alla protezione del tessuto cardiaco dopo un danno. Nel loro insieme, questi schemi indicano che il RIC orienta l’organismo verso un uso più efficiente dell’energia e favorisce la crescita o il rimodellamento dei vasi sanguigni—potenzialmente migliorando il flusso attorno all’area danneggiata dall’ictus. Allo stesso tempo, alcuni marker, come NCCRP‑1 e MARCO, possono riflettere la risposta acuta allo stress e immunitaria del corpo alla procedura di gonfiaggio del manicotto, sottolineando che il RIC innesca una reazione complessa a livello sistemico.
Cosa significa per la cura futura dell’ictus
Questo piccolo studio esplorativo non può dimostrare esattamente come il RIC protegga il cervello e ha coinvolto solo 25 pazienti di un unico paese, quindi i risultati devono essere confermati in gruppi molto più grandi e diversificati. Tuttavia, identificare una lista breve di nove proteine che si muovono in modo coerente e opposto con e senza RIC è un passo importante. In futuro, tali biomarcatori potrebbero aiutare i medici a capire rapidamente se il RIC sta “prendendo” in un dato paziente, guidare la scelta di chi dovrebbe riceverlo o persino ispirare trattamenti farmacologici che imitino i suoi effetti benefici senza il manicotto. Per ora, il lavoro rafforza un’idea semplice ma potente: stressando in modo sicuro una parte del corpo, potremmo essere in grado di indurre il cervello in uno stato più resiliente e più capace di guarire dopo un ictus.
Citazione: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Parole chiave: ictus ischemico acuto, conditioning ischemico remoto, biomarcatori sierici, analisi proteomica, neuroprotezione