Clear Sky Science · it
Analisi del proteoma e del fosfoproteoma basata su Orbitrap Astral identifica proteine candidate associate alla fosfatidato fosfatasi MoPah1 in Magnaporthe oryzae
Perché un enzima della malattia del riso è importante
Il riso è un alimento fondamentale per miliardi di persone, eppure un singolo fungo microscopico, Magnaporthe oryzae, provoca la blastosi del riso che può devastare interi campi. Questo studio esplora la chimica interna di quel fungo, concentrandosi su un enzima, MoPah1, che regola i grassi cellulari e molecole di segnalazione. Mappando migliaia di proteine e i loro interruttori on/off, i ricercatori rivelano come questo enzima colleghi il metabolismo di base alla capacità del fungo di infettare le piante di riso.
Un fungo che penetra le piante di riso
Magnaporthe oryzae infetta le foglie di riso usando una struttura specializzata chiamata appressorio, che accumula enorme pressione interna per perforare la superficie fogliare. Per alimentare questo processo, il fungo consuma rapidamente zuccheri e grassi immagazzinati. Studi precedenti hanno mostrato che MoPah1, un enzima che converte una molecola lipidica chiamata acido fosfatidico in un’altra chiamata diacilglicerolo, è vitale per questo stile di vita: l’eliminazione del gene MoPah1 indebolisce il fungo e riduce la sua capacità di causare malattia. Rimaneva tuttavia da capire quali altre proteine fossero collegate a MoPah1 e come questo enzima si inserisca in reti cellulari più ampie.
Uso della mappatura proteica di nuova generazione
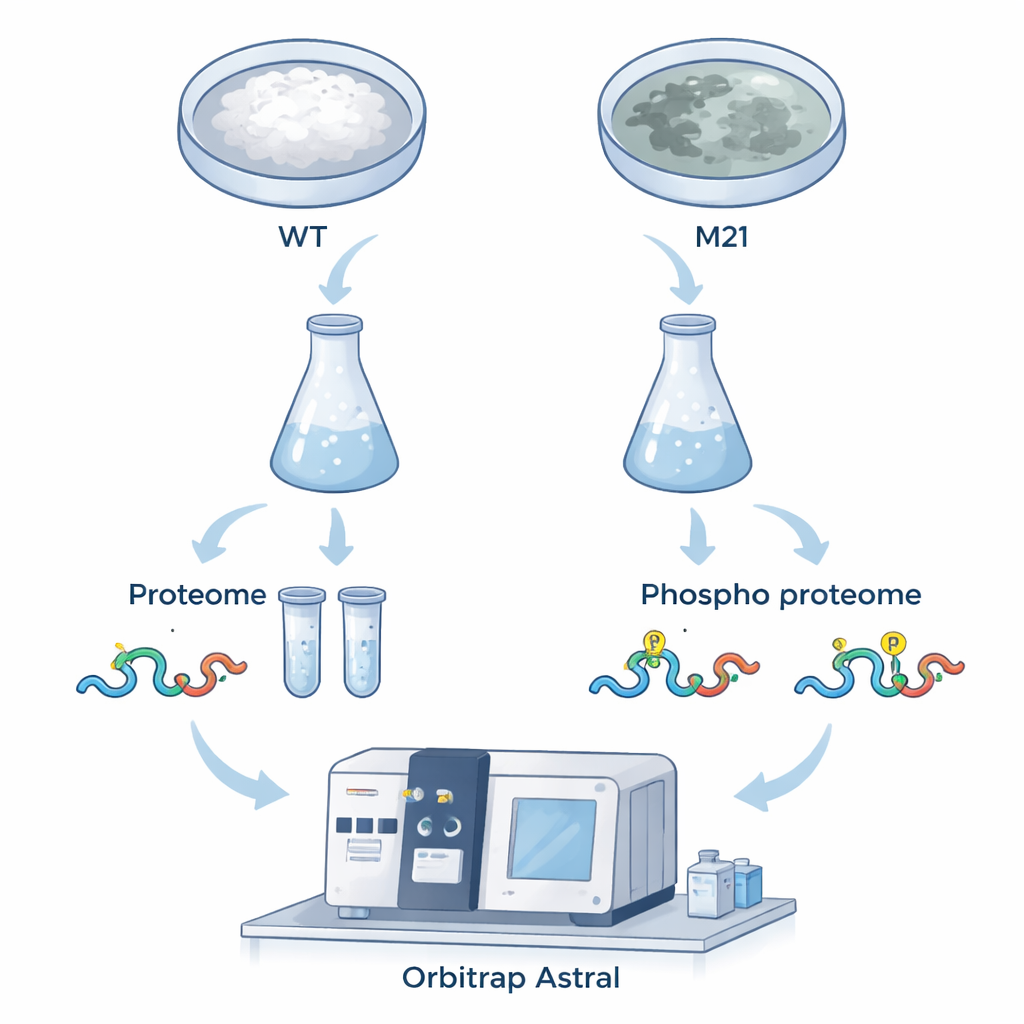
Per rispondere a queste domande, il team ha confrontato funghi normali con un mutante privo di MoPah1. Si sono concentrati sulla crescita filamentosa (micelio), perché il mutante non può produrre le spore normalmente usate negli studi di infezione. Utilizzando uno spettrometro di massa avanzato chiamato Orbitrap Astral e una strategia di acquisizione indipendente dai dati (DIA), hanno misurato sia l’abbondanza delle proteine sia la presenza di gruppi fosfato che agiscono come interruttori molecolari. In totale hanno identificato 6.799 proteine e oltre 15.000 siti di fosforilazione, con centinaia che mostrano aumenti o diminuzioni evidenti nel mutante. Questo ampio dataset di alta qualità offre un’istantanea dettagliata di come la rimozione di MoPah1 rimodelli la cellula fungina.
Spostamenti nell’uso dell’energia e nel riciclo cellulare
Quando i ricercatori hanno esaminato quali tipi di proteine cambiavano, sono emersi due temi principali: il metabolismo dei lipidi di membrana e un processo di “autoingestione” chiamato autofagia, che le cellule usano per riciclare componenti e sopravvivere allo stress. Molte proteine coinvolte nei glicerofosfolipidi—i mattoni delle membrane cellulari—e nelle vie energetiche correlate risultavano alterate. Le proteine associate all’autofagia hanno mostrato in particolare forti cambiamenti nei loro schemi di fosforilazione, suggerendo che MoPah1 influisce non solo sulla sintesi e degradazione dei lipidi, ma anche su come il fungo ricicla il proprio materiale durante la crescita e l’infezione. Un sottoinsieme di 72 proteine è cambiato sia nella quantità sia nello stato di fosforilazione, segnalandole come candidate principali per un controllo diretto o indiretto da parte di MoPah1.
Trovare i partner proteici di MoPah1
Per andare oltre le correlazioni, il team ha indagato quali proteine si legano fisicamente a MoPah1. Hanno prodotto una versione di MoPah1 fusa con una “maniglia” (GST) in batteri, poi l’hanno usata come esca per pescare le proteine interagenti dagli estratti fungini. La spettrometria di massa ha identificato 183 candidati, molti dei quali si raggruppano in grandi complessi proteici, rafforzando l’idea che MoPah1 si trovi al centro di ampie reti cellulari. Tra questi partner, uno ha spiccato: Pmk1, una proteina chiave della via di segnalazione MAPK che controlla la formazione dell’appressorio, la crescita all’interno della pianta e le risposte allo stress. Ulteriori test con il sistema two‑hybrid nel lievito hanno confermato che MoPah1 e Pmk1 possono interagire direttamente.
Collegare il controllo dei lipidi ai segnali di infezione
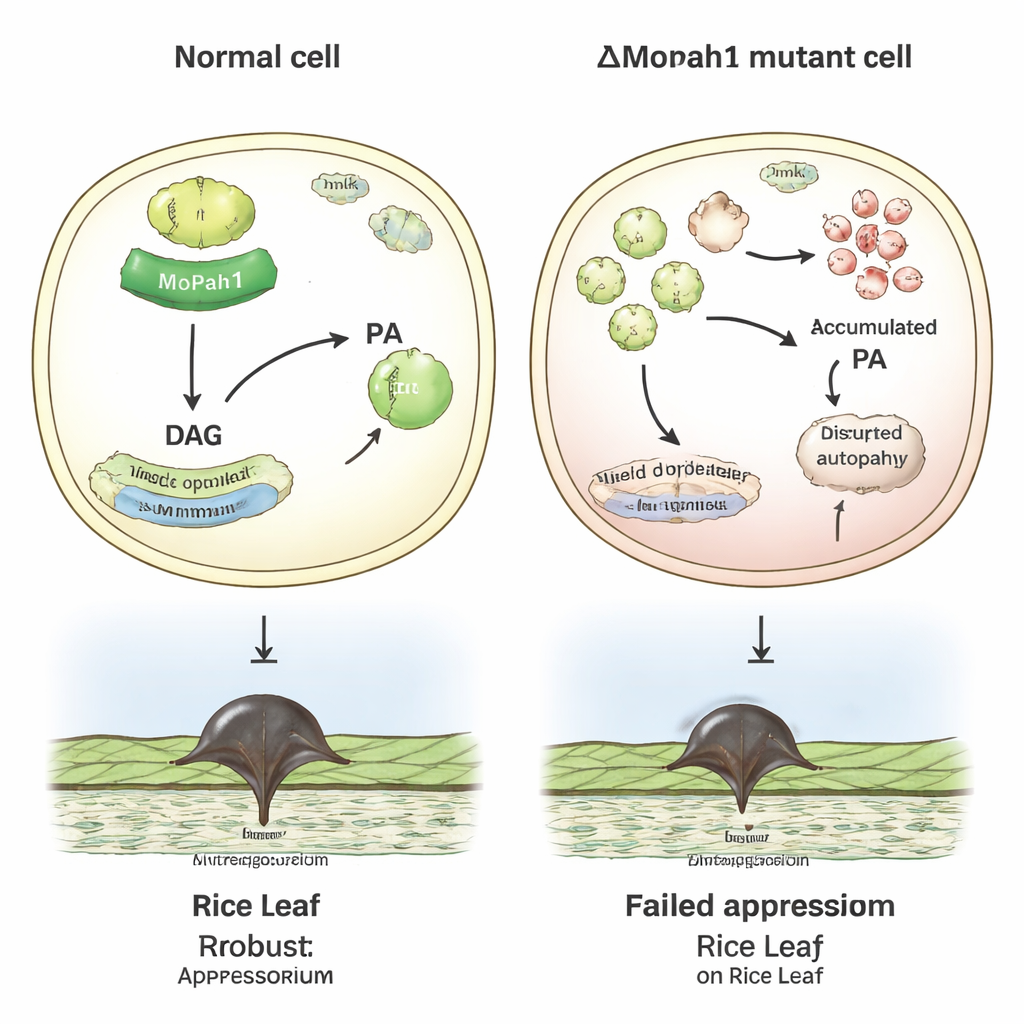
Mettendo insieme questi filoni, gli autori propongono che MoPah1 aiuti a modulare sia l’equilibrio dei lipidi di membrana sia le principali vie di segnalazione in Magnaporthe oryzae. Nei funghi privi di MoPah1, vaste perturbazioni nel metabolismo lipidico, nel riciclo proteico e nella segnalazione MAPK sembrano compromettere la formazione e l’efficacia delle strutture infettive necessarie a penetrare le foglie di riso. Pur essendo lo studio limitato ai campioni miceliali—perché il mutante non può formare spore—esso fornisce comunque una ricca risorsa di dati su proteine e fosforilazioni, oltre a una lista ristretta di proteine più probabili partner di MoPah1. Per i non specialisti, la conclusione chiave è che il controllo di un singolo enzima in un patogeno delle colture può riverberare su molti sistemi cellulari, offrendo nuovi punti di vista per comprendere e, forse un giorno, contrastare il fungo che minaccia una delle risorse alimentari più importanti al mondo.
Citazione: Zhao, J., Yang, L., Shi, X. et al. Orbitrap Astral–based proteome and phosphoproteome analysis identifies candidate proteins associated with the phosphatidate phosphatase MoPah1 in Magnaporthe oryzae. Sci Rep 16, 6901 (2026). https://doi.org/10.1038/s41598-026-36940-1
Parole chiave: fungo della ruggine del riso, Magnaporthe oryzae, reti proteiche, metabolismo dei lipidi, patogenicità fungina