Clear Sky Science · it
Una sottopopolazione pro‑infiammatoria di neutrofili guida il danno da ischemia‑riperfusione intestinale tramite la via dello stress del reticolo endoplasmatico mediata da ATF4
Quando il flusso sanguigno danneggia l’intestino
I chirurghi e i medici delle cure intensive si sono a lungo interrogati su un paradosso pericoloso: quando l’apporto di sangue all’intestino viene interrotto e poi ripristinato, il ripristino stesso può danneggiare gravemente la mucosa intestinale. Questo processo, chiamato danno da ischemia‑riperfusione intestinale, può portare a complicazioni potenzialmente letali come sepsi e insufficienza multiorgano. Lo studio qui riassunto rivela che non tutte le cellule immunitarie che accorrono sono uguali: una sottopopolazione particolarmente aggressiva di globuli bianchi gioca un ruolo centrale nel trasformare una risposta salvavita in un effetto dannoso.
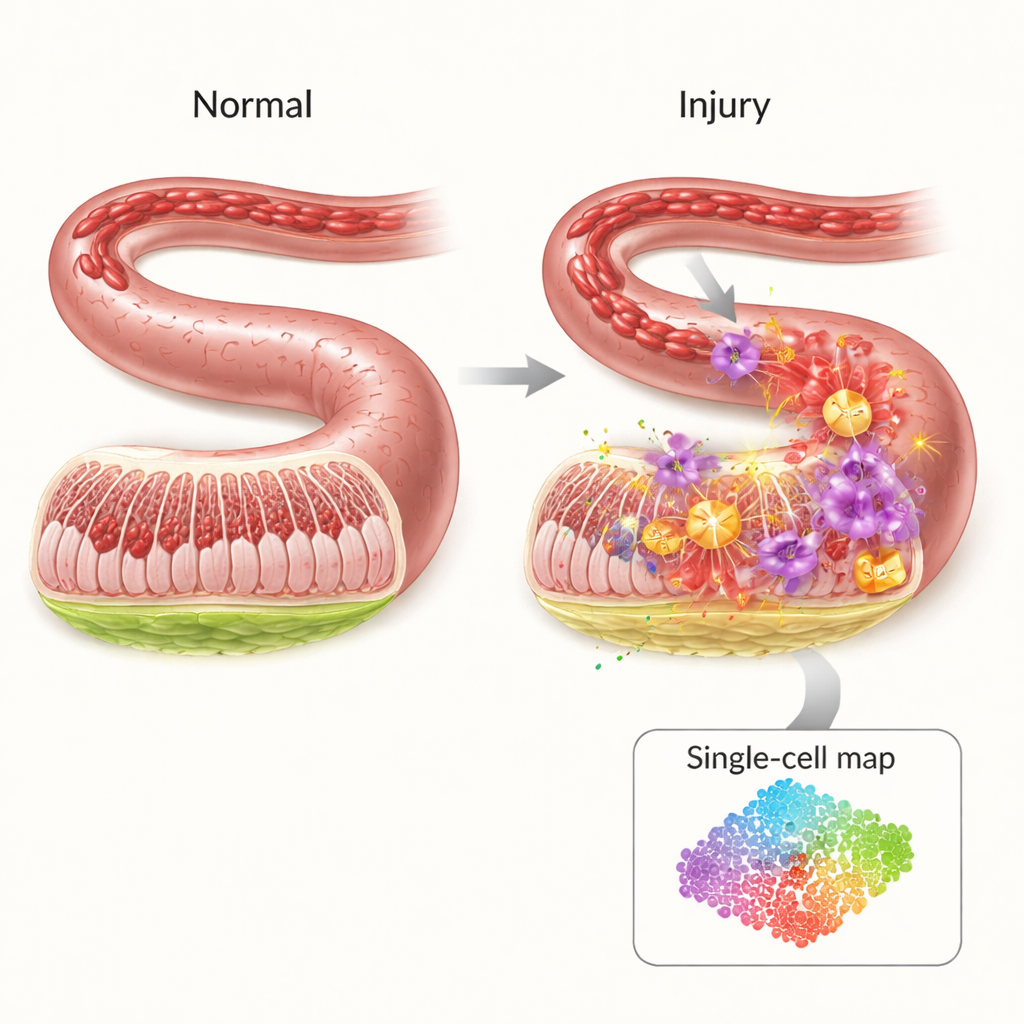
La fragile barriera protettiva dell’intestino
L’interno dell’intestino è rivestito da una barriera sottile ma altamente organizzata che mantiene batteri e tossine confinati nel lume consentendo però il passaggio dei nutrienti. Quando il flusso sanguigno viene interrotto — per esempio durante uno shock, un intervento chirurgico maggiore o un trauma grave — questa barriera viene privata di ossigeno. Sorprendentemente, la maggior parte del danno non avviene durante la mancanza di sangue, ma quando la circolazione ritorna. L’improvviso afflusso di ossigeno e cellule immunitarie scatena una tempesta di segnali infiammatori e molecole reattive che possono creare perforazioni nella parete intestinale, permettendo ai germi di entrare nel circolo sanguigno. Nonostante l’importanza clinica, oggi i medici dispongono di pochi trattamenti mirati per prevenire questa cascata.
Osservare le singole cellule
Per capire chi fa cosa durante questa crisi, i ricercatori hanno usato il sequenziamento dell’RNA a cellula singola, una tecnica che legge quali geni sono attivi in migliaia di singole cellule contemporaneamente. In un modello murino di ischemia‑riperfusione intestinale, hanno confrontato intestini danneggiati con intestini sani e mappato 19 tipi cellulari principali. Hanno osservato che alcune cellule immunitarie — in particolare i neutrofili e i monociti infiammatori — si espandevano drasticamente dopo l’evento, mentre cellule protettive come linfociti T, linfociti B e cellule natural killer diminuivano. Anche le reti di comunicazione tra i tipi cellulari si sono spostate, con i neutrofili che sono emersi come nodi centrali che inviano e ricevono molti segnali infiammatori, indicandoli come principali promotori del danno.
Una sottopopolazione dannosa di cellule “primi soccorritori”
I neutrofili sono tra i primi soccorritori più veloci del corpo, affluendo nel sangue per affrontare le infezioni e rimuovere detriti. Ma questo studio mostra che all’interno della popolazione dei neutrofili esiste un sottogruppo particolarmente aggressivo responsabile di gran parte dei danni collaterali nell’intestino. Quando gli scienziati hanno depletato i neutrofili nei topi prima di indurre ischemia‑riperfusione, gli animali hanno mostrato minore accorciamento intestinale, livelli più bassi di marker di danno nel sangue, migliore aspetto tissutale al microscopio e proteine di tenuta della mucosa più integre. In esperimenti di co‑coltura, neutrofili prelevati da topi danneggiati hanno danneggiato direttamente le cellule intestinali, riducendone la sopravvivenza, aumentando la morte cellulare e compromettendo importanti proteine a «cerniera» che mantengono la barriera intestinale intatta.
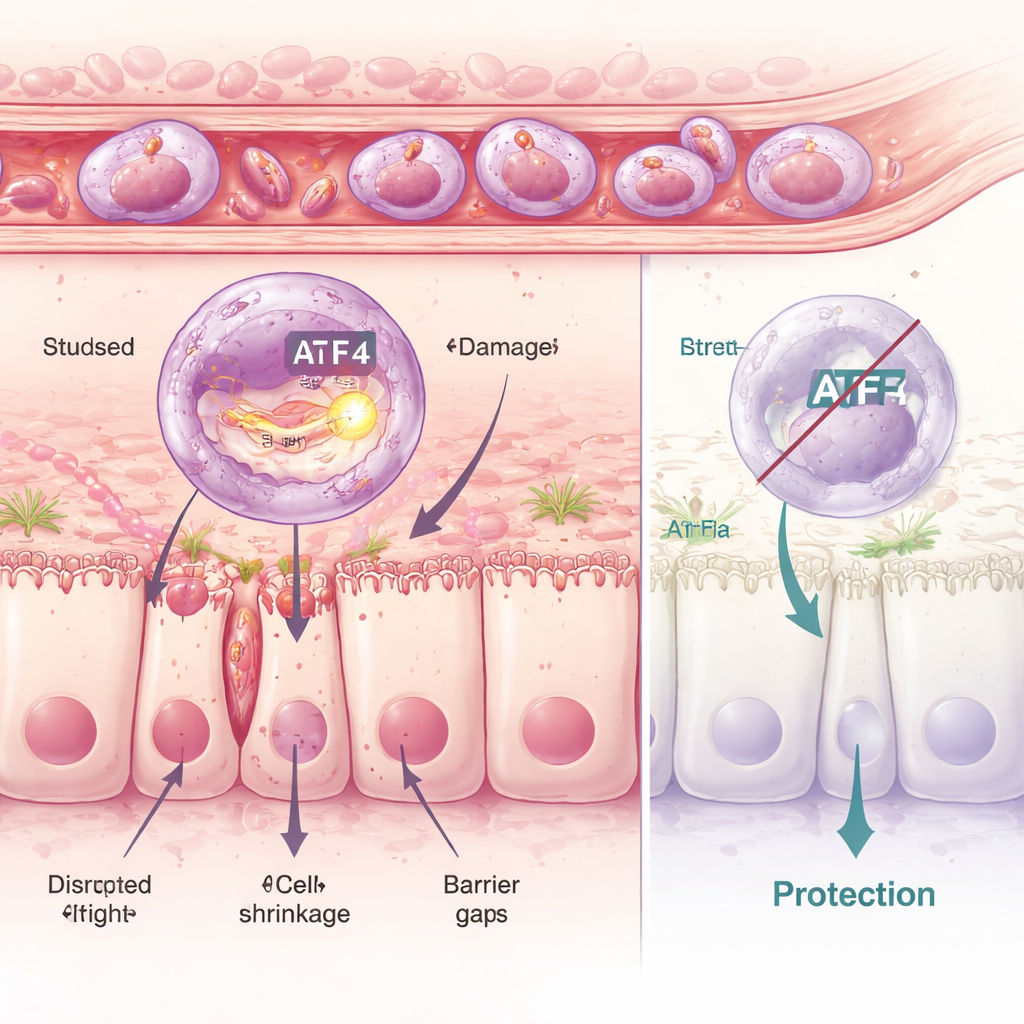
Stress all’interno delle cellule: quando il controllo qualità fallisce
Approfondendo l’analisi, i ricercatori hanno esaminato i neutrofili uno per uno e identificato sei sottogruppi distinti. Uno, denominato cluster C5, si è distinto per il suo forte profilo infiammatorio e per l’attivazione di un programma molecolare di stress all’interno di una struttura chiamata reticolo endoplasmatico, il laboratorio cellulare del ripiegamento proteico. Un regolatore chiave di questo programma è una proteina chiamata ATF4. Nelle cellule dannose del cluster C5, ATF4 e i suoi geni bersaglio erano fortemente attivi. Utilizzando farmaci che aumentano o attenuano questa risposta di stress interna, il gruppo ha mostrato che più stress significava più danno intestinale, mentre bloccarlo preservava la barriera. Topi ingegnerizzati geneticamente per non esprimere ATF4 erano in gran parte protetti: anche quando venivano somministrati farmaci che inducono stress, i loro neutrofili non riuscivano a eseguire pienamente il programma dannoso e la mucosa intestinale restava molto più integra.
Cosa significa per i trattamenti futuri
Nel complesso, questi risultati offrono un quadro chiaro per il pubblico non specialista: tra lo sciame di cellule immunitarie che invadono l’intestino quando il flusso sanguigno ritorna, una specifica sottopopolazione di neutrofili primed dallo stress agisce come una squadra di pulizia troppo zelante che abbatte l’edificio insieme ai detriti. Il loro potere distruttivo dipende da una via di stress intracellulare controllata da ATF4. Moderare questa via — senza eliminare tutti i neutrofili — potrebbe offrire un modo per proteggere l’intestino durante eventi ad alto rischio come interventi chirurgici maggiori, infezioni gravi o traumi. Pur essendo necessario ulteriore lavoro per confermare questi risultati nell’uomo e per trovare farmaci sicuri e precisi, lo studio apre una promettente strada verso terapie in grado di mantenere integra la barriera intestinale quando i pazienti ne hanno più bisogno.
Citazione: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Parole chiave: barriera intestinale, ischemia riperfusione, neutrofili, stress del reticolo endoplasmatico, ATF4