Clear Sky Science · it
Nanolisosome a lunga circolazione coniugati al peptide CKAAKN per la somministrazione mirata di oridonina ai tumori pancreatici
Perché questa ricerca è importante
Il cancro del pancreas è uno dei tumori più letali, in parte perché viene spesso scoperto in fase avanzata e resiste ai trattamenti chemioterapici standard. Questo studio esplora un modo più intelligente di veicolare un composto antitumorale di origine vegetale, l’oridonina, direttamente ai tumori pancreatici utilizzando piccole bolle lipidiche chiamate nanolisosomi. Facilitando l’arrivo di una maggiore quantità di farmaco al tumore e risparmiando i tessuti sani, il lavoro apre la strada a opzioni terapeutiche più efficaci e meno invasive per una neoplasia che ne ha urgente bisogno.
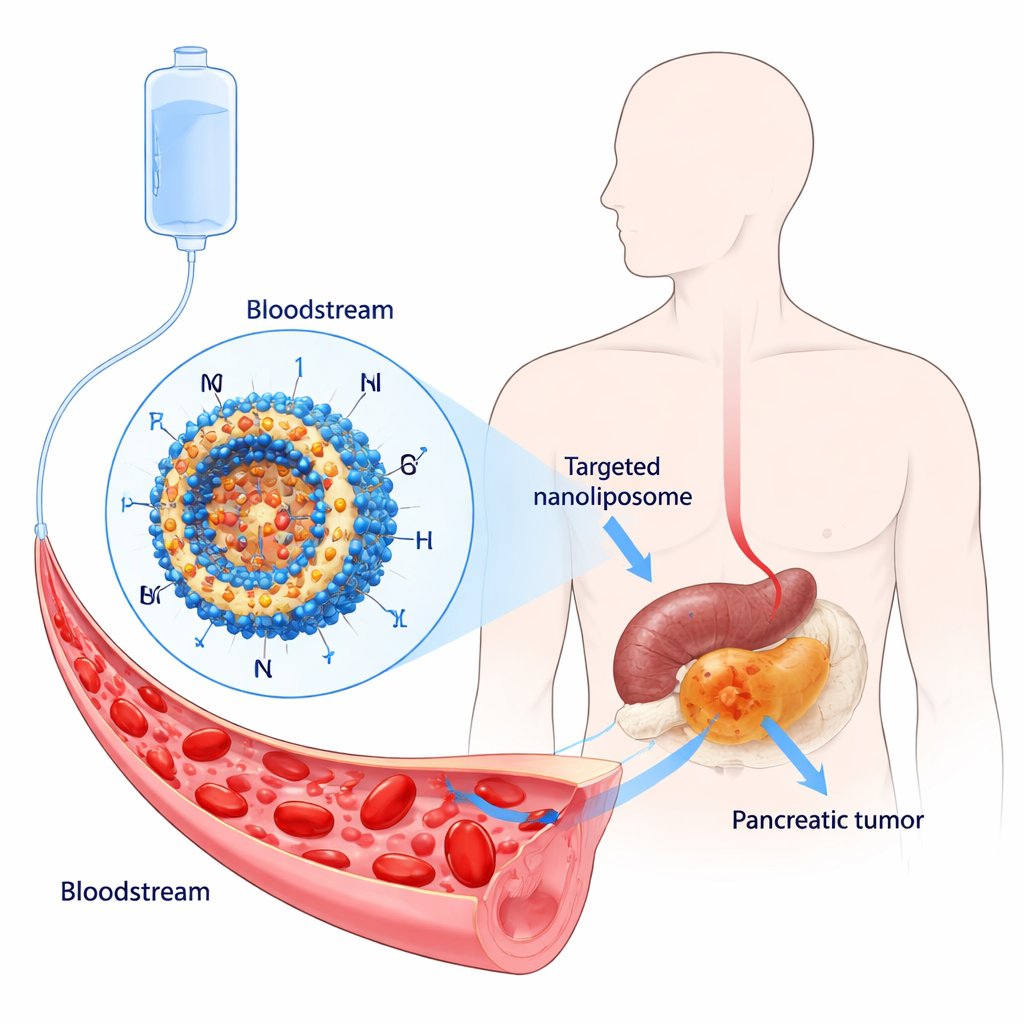
Un cancro letale e difficile da trattare
Il cancro del pancreas si è guadagnato il triste soprannome di “re dei tumori” perché i tassi di sopravvivenza restano a una cifra per la maggior parte dei pazienti. Solo una piccola parte delle persone è idonea all’intervento chirurgico e, anche in quei casi, molti tumori recidivano. Farmaci chemioterapici come paclitaxel e cisplatino possono rallentare la malattia, ma provocano effetti collaterali pesanti e i tumori spesso sviluppano resistenza. I ricercatori cercano quindi farmaci più precisi e meno tossici, insieme a sistemi di somministrazione in grado di concentrare la terapia nel tumore anziché distribuirla in tutto l’organismo.
Trasformare una molecola erbacea in una medicina moderna
L’oridonina è un composto naturale estratto dalla pianta medicinale cinese tradizionale Rabdosia rubescens. Studi di laboratorio hanno mostrato che può uccidere o rallentare la crescita di vari tipi di cellule tumorali, incluse quelle pancreatiche, interferendo con la divisione cellulare e inducendo l’autodistruzione delle cellule. Tuttavia, l’oridonina da sola è difficile da usare come farmaco: si scioglie male in acqua, viene assorbita poco ed è potenzialmente tossica a dosi più alte. Per sfruttarne il potenziale, gli autori hanno confezionato l’oridonina all’interno di nanolisosomi — minuscole sfere lipidiche simili alle membrane cellulari — progettate per trasportare il farmaco in sicurezza nel flusso sanguigno e rilasciarlo lentamente nel sito tumorale.
Progettare un involucro “stealth” che indirizzi il farmaco
Il gruppo ha messo a punto un sistema di somministrazione a due livelli. In primo luogo, hanno creato liposomi a lunga circolazione rivestendo la loro superficie con polietilenglicole (PEG), un polimero idrofilo e flessibile che aiuta le particelle a sfuggire alla cattura da parte delle cellule immunitarie e a rimanere più a lungo nel sangue. Poi hanno aggiunto un peptide corto, CKAAKN, che funge da etichetta di richiamo per il cancro pancreatico. Questo peptide imita una parte della via di segnalazione Wnt, spesso iperattiva in molti tumori pancreatici, permettendo ai liposomi modificati (chiamati ORI@CPD-Lipo) di legarsi alle cellule tumorali che esprimono i recettori corrispondenti. Le particelle finali avevano un diametro di circa 100 nanometri, contenevano elevate quantità di oridonina e rilasciavano il farmaco lentamente nel corso di molte ore invece che tutto in una volta.
Come si comportano le particelle mirate nelle cellule e negli animali
Nei test in coltura cellulare, i liposomi marcati con CKAAKN venivano assorbiti molto più efficacemente dalle cellule tumorali pancreatiche umane rispetto alle cellule pancreatiche normali, specialmente nelle prime ore di contatto. Quando è stato aggiunto in eccesso peptide CKAAKN libero come esca, le cellule tumorali hanno assorbito meno particelle, a sostegno dell’ipotesi di un passaggio di legame specifico. I liposomi vuoti hanno mostrato bassa tossicità e non hanno danneggiato i globuli rossi, suggerendo una buona sicurezza. Caricati con oridonina, i liposomi mirati hanno ucciso le cellule tumorali più efficacemente sia rispetto all’oridonina libera sia rispetto ai liposomi non mirati, e hanno rallentato in misura maggiore la migrazione delle cellule tumorali attraverso una “ferita” da graffi in coltura. In topi portatori di tumori pancreatici, i liposomi mirati marcati con fluorescenza si accumulavano nel tumore per fino a 48 ore e si concentravano più del materiale non mirato, pur venendo in gran parte eliminate attraverso fegato e milza come previsto.
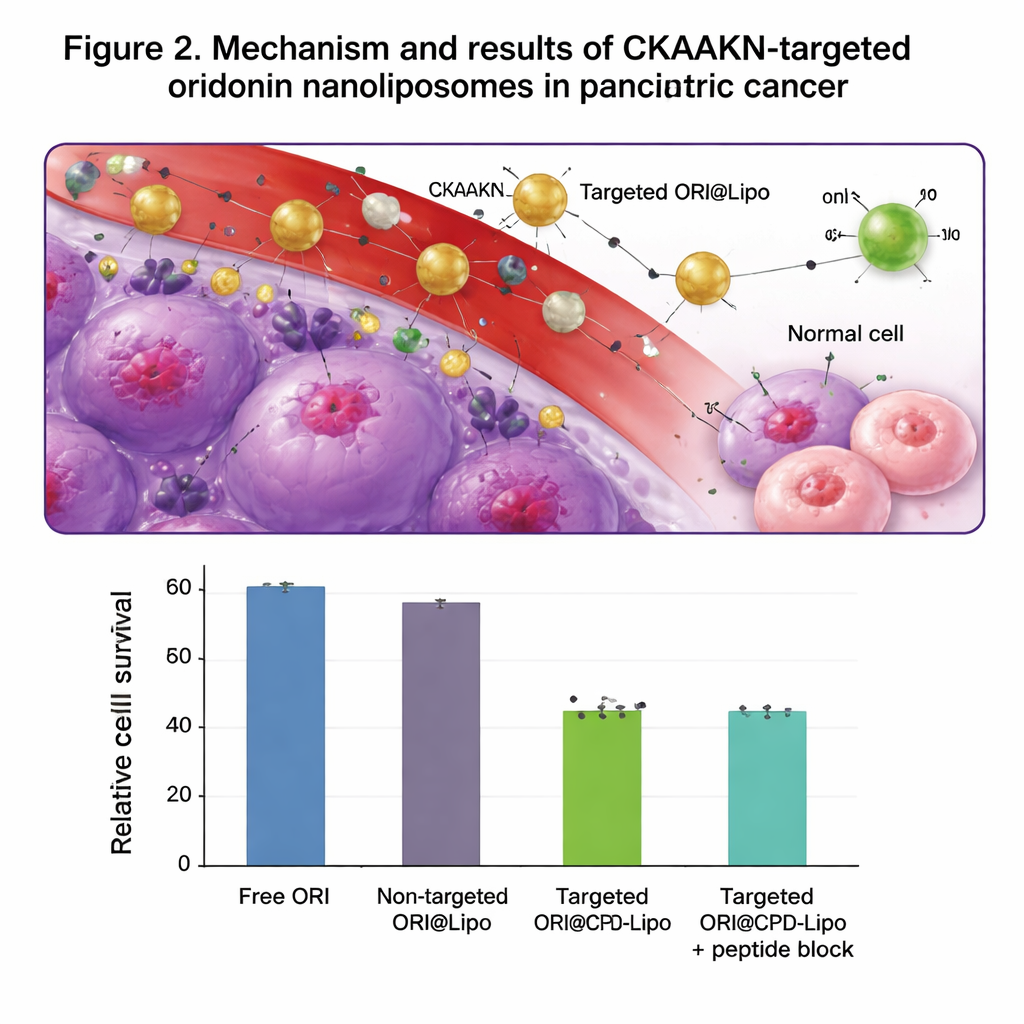
Cosa potrebbe significare per i trattamenti futuri
Complessivamente, i risultati mostrano che combinare un composto erbaceo tradizionale con un veicolo di somministrazione moderno e mirato può potenziare significativamente la sua efficacia antitumorale nei modelli di laboratorio. I nanolisosomi a lunga circolazione decorati con CKAAKN convogliano più oridonina nelle cellule del cancro pancreatico limitando l’esposizione del tessuto sano, aumentando la morte tumorale e riducendo la migrazione che potrebbe favorire la diffusione. Sebbene questi risultati siano ancora preclinici e gli autori sottolineino la necessità di studi completi su trattamenti animali e di trial clinici, il lavoro fornisce una solida base per approcci di nanomedicina mirata nel cancro del pancreas e suggerisce una strategia generale per trasformare altre molecole naturali promettenti in farmaci pratici con destinazione tumorale.
Citazione: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
Parole chiave: cancro del pancreas, nanolisosomi, somministrazione mirata di farmaci, oridonina, peptide che indirizza il tumore