Clear Sky Science · it
Sintesi e valutazione anticancro di nuovi derivati tioimidazolo contenenti un frammento trimetossifenilico
Nuovi strumenti chimici nella lotta contro il cancro
I farmaci chemioterapici spesso danneggiano le cellule sane oltre ai tumori, causando effetti collaterali pesanti. Questo studio esplora una nuova famiglia di molecole sintetiche che puntano a colpire le cellule tumorali in modo molto più incisivo rispetto ai tessuti normali. Unendo in modo intelligente due mattoni chimici già noti per la loro efficacia nei medicinali, i ricercatori hanno creato composti che mostrano un forte effetto letale mirato sulle cellule cancerose in saggi in vitro e in modelli tumorali 3D, risparmiando in gran parte le cellule sane.
Progettare molecole antitumorali più intelligenti
Il gruppo si è concentrato su due strutture chimiche “privilegiate” che ricorrono frequentemente nei farmaci di successo. Una è l'imidazolo, un piccolo anello che si inserisce bene in molti bersagli biologici. L'altra è il gruppo trimetossifenilico (TMP), uno schema di tre catene contenenti ossigeno su un anello aromatico, centrale in diversi farmaci anticancro che disturbano la divisione cellulare. Inserendo un atomo di zolfo nel nucleo imidazolico (creando un tioimidazolo) e collegandolo a un gruppo TMP, i chimici miravano a mettere a punto il comportamento farmacocinetico delle molecole e la loro affinità per proteine correlate al cancro. Tramite un percorso sintetico passo dopo passo, hanno costruito una libreria di composti correlati, ciascuno modificato in modo sottile per sondare quali caratteristiche siano più importanti per l'attività anticancro. 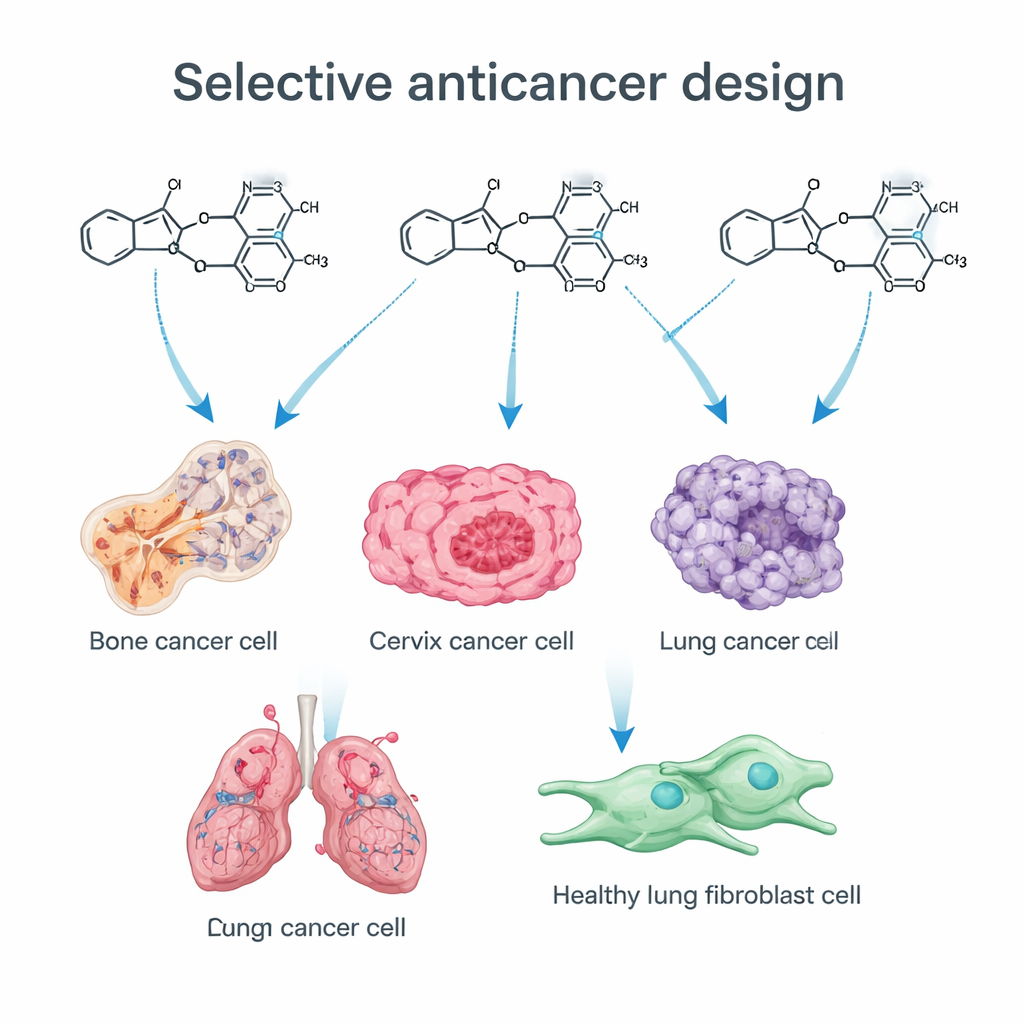
Testare le cellule tumorali risparmiando il tessuto sano
Le nuove molecole sono state testate su quattro linee cellulari tumorali umane — osteosarcoma (osso), carcinoma cervicale, colon e polmone — nonché su fibroblasti polmonari non tumorali. Molti dei composti hanno rallentato o arrestato la crescita delle cellule cancerose, ma uno in particolare, denominato 13b, si è distinto. Ha ucciso cellule di tumore osseo e cervicale a concentrazioni molto basse, mostrando tuttavia nessuna tossicità rilevabile verso i fibroblasti normali anche a dosi oltre 60 volte superiori. Diversi altri composti erano moderatamente potenti ma meno selettivi, sottolineando come piccole modifiche strutturali — per esempio l'aggiunta di un atomo di cloro o di un gruppo nitro in posizioni specifiche — possano spostare l'equilibrio tra tossicità generalizzata e azione mirata sul cancro.
Come il composto guida le cellule tumorali all'autodistruzione
Per capire cosa faccia concretamente il 13b all'interno delle cellule, i ricercatori hanno cercato i segni distintivi della morte cellulare programmata, o apoptosi. Le cellule tumorali trattate con 13b sono risultate positive per Annexin V e hanno attivato le proteasi caspasi-3 e -7, marcatori classici che indicano l'avvio di un programma ordinato di suicidio cellulare piuttosto che una semplice rottura. La microscopia ha rivelato punti luminosi di γH2AX, segnale di rotture del DNA, nei nuclei delle cellule trattate. Col tempo, l'impalcatura interna delle cellule ha cominciato a riorganizzarsi e a decadere, soprattutto nelle cellule di carcinoma cervicale, che si sono arrotondate e staccate — indizi visivi che l'apoptosi era in fase avanzata. Complessivamente, questi risultati mostrano che 13b danneggia il DNA delle cellule tumorali e poi ne induce la morte attraverso una via controllata.
Dai monostrati alle mini-tumorazioni 3D
La maggior parte dei test di laboratorio coltiva le cellule tumorali in strati sottili, che non riproducono completamente la struttura densa e stratificata dei tumori reali. Per questo motivo, il gruppo ha coltivato le cellule in sfere tridimensionali — piccoli ammassi sferici che somigliano maggiormente all'architettura di un tumore e alle sfide della penetrazione dei farmaci. Quando queste sfere sono state trattate con 13b, si sono ridotte in modo dipendente dalla dose. Le sfere di tumore osseo sono state particolarmente sensibili, diventando piccole, friabili e frammentate a livelli di farmaco più elevati. La colorazione fluorescente ha mostrato ondate di apoptosi che si propagavano dall'esterno verso l'interno della sfera all'aumentare della concentrazione, dimostrando che 13b è in grado di penetrare e uccidere cellule in tutte le parti di queste strutture compatte. 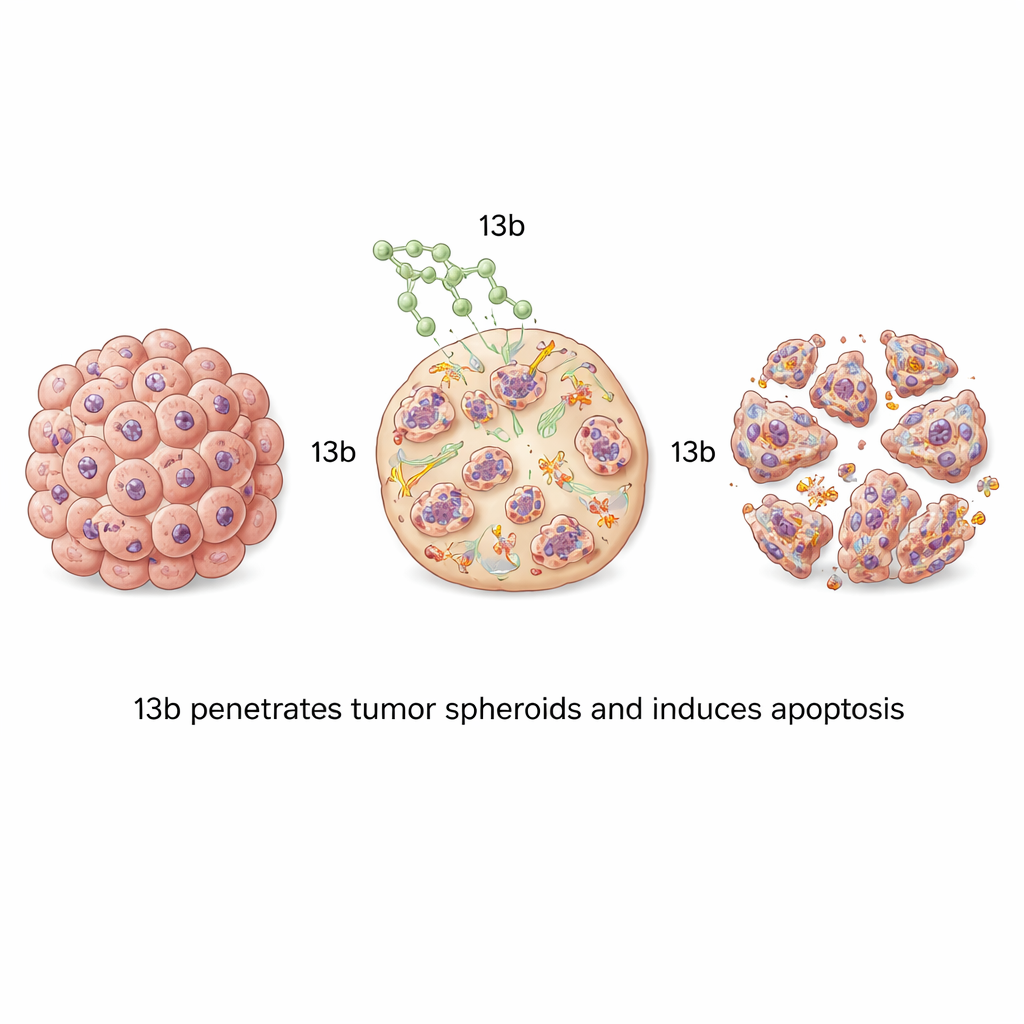
Perché questo lavoro è importante per i futuri trattamenti antitumorali
Per un lettore non specialista, il messaggio chiave è che i ricercatori hanno creato una nuova classe di piccole molecole che combinano in un unico progetto ibrido i punti di forza di due componenti di farmaci già collaudati. Il composto principale, 13b, è in grado di riconoscere e distruggere efficientemente le cellule tumorali risparmiando in gran parte le cellule sane nei test di laboratorio, e resta efficace anche in modelli tumorali 3D più realistici. Sebbene molto lavoro resti da fare — come identificare esattamente i bersagli molecolari, migliorare la solubilità e testare il composto in organismi animali — questo studio dimostra che combinare i framework tioimidazolo e TMP è una strategia promettente per progettare agenti anticancro più selettivi e potenti.
Citazione: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Parole chiave: agenti anticancro, derivati dell'imidazolo, trimetossifenilico, apoptosi, sfere tumorali 3D