Clear Sky Science · it
Variazioni di volume e funzionali del pancreas residuo dopo diversi tipi di pancreatectomia: Esplorare il potenziale rigenerativo
Perché chirurghi e pazienti tengono al "pancreas residuo"
Quando una parte del pancreas viene rimossa chirurgicamente—per trattare il cancro, cisti o un’infiammazione grave—i pazienti spesso si chiedono che cosa succede al pezzo che resta. Ricresce, si restringe o si adatta in qualche modo? E, cosa più importante, come incide sul rischio di sviluppare il diabete in futuro? Questo studio ha seguito i pazienti per due anni dopo due comuni interventi pancreatici per vedere come il pancreas residuo cambiava in volume e quanto fosse capace di continuare a produrre insulina, l’ormone che regola la glicemia.
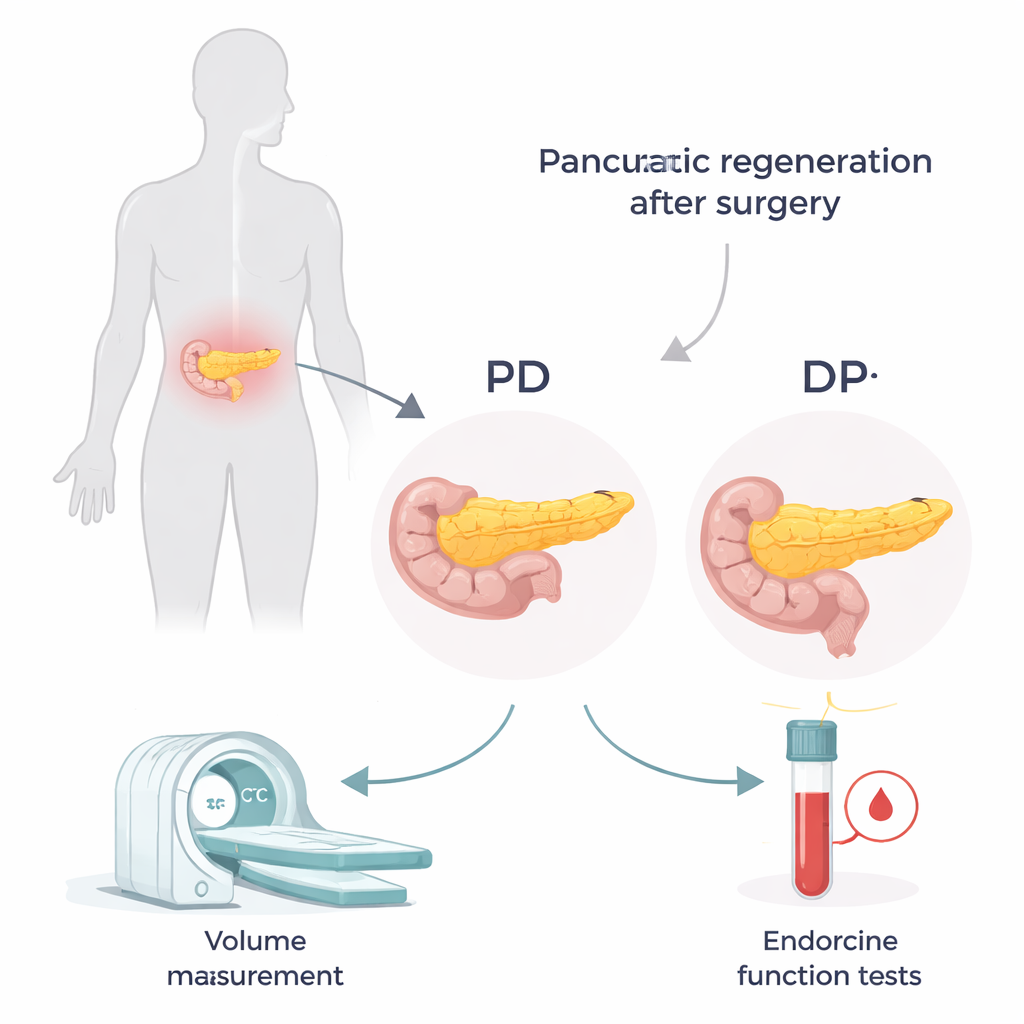
Due interventi diversi, due residui diversi
Il pancreas è situato in profondità nell’addome e si estende da destra a sinistra. I chirurghi scelgono tra due interventi principali a seconda della localizzazione della malattia. Nella pancreaticoduodenectomia (PD, spesso chiamata procedura di Whipple) viene rimossa la porzione destra, la “testa”, lasciando la “corpo e coda” a sinistra. Nella pancreatectomia distale (DP) viene asportata la porzione sinistra, la “coda”, lasciando prevalentemente la testa. Testa e coda non sono identiche: la coda è più ricca dei piccoli ammassi cellulari che producono insulina. Ciò significa che perdere la coda può avere un impatto maggiore sul controllo del glucosio, anche se la quantità complessiva di pancreas rimosso appare simile.
Misurare volume e potenza ormonale nel tempo
Per monitorare come il pancreas si adattasse dopo l’intervento, i ricercatori hanno esaminato le cartelle di 135 pazienti trattati in un singolo ospedale tra il 2009 e il 2017. Hanno usato TC con mezzo di contrasto per misurare il volume dell’intero pancreas prima dell’intervento e della porzione residua a 3 mesi, 1 anno e 2 anni dopo l’intervento. Nelle stesse visite hanno eseguito esami del sangue relativi al metabolismo del glucosio, incluso il peptide C—un marcatore di quanta insulina il corpo produce. Combinando il peptide C con i livelli di glucosio in un indice semplice, hanno potuto stimare quanto efficientemente funzionasse il tessuto pancreatico residuo.
Quando più grande non significa migliore
I due interventi hanno prodotto modelli di rigenerazione e atrofia nettamente diversi. Dopo la pancreatectomia distale, la porzione residua della testa spesso aumentava di volume nel tempo: in media, il suo volume raggiungeva circa il 110% rispetto alle dimensioni immediate postoperatorie a due anni, e quasi tre quarti di questi pazienti mostravano una chiara ipertrofia, ossia ingrandimento. Dopo la pancreaticoduodenectomia, è successo l’opposto: il residuo di corpo e coda si è gradualmente atrofizzato fino a circa due terzi delle dimensioni iniziali, e l’ingrandimento vero era raro. La dilatazione del dotto pancreatico principale—un segno che la via di drenaggio potrebbe essere ristretta—era associata a una maggiore atrofia nei pazienti PD. Eppure, nonostante conservassero più tessuto nel complesso, i pazienti DP andavano peggio sul piano metabolico: circa un terzo dei pazienti DP precedentemente non diabetici ha sviluppato un nuovo diabete, e nessuno di quelli con diabete preesistente è andato in remissione.
La forza nascosta delle cellule insuliniproduttrici residue
Un’analisi più attenta della produzione ormonale ha rivelato perché il solo volume non raccontava tutta la storia. In entrambi i gruppi, la produzione di insulina è diminuita a tre mesi per poi recuperare parzialmente. Quando i ricercatori hanno corretto la produzione di insulina in rapporto al tessuto pancreatico residuo, hanno scoperto che il pancreas dopo PD diventava sorprendentemente efficiente: ogni unità di tessuto produceva più insulina nel tempo. Al contrario, i pazienti che avevano perso la coda ricca di isole nel DP tendevano ad avere una ripresa endocrina più debole, anche se il loro pancreas residuo era più voluminoso e talvolta addirittura ingrandito. Questo supporta studi anatomici che mostrano come la coda contenga circa il doppio delle cellule produttrici di insulina rispetto alla testa, e suggerisce che le cellule sopravvissute possono “lavorare di più” per compensare quando necessario.
Implicazioni per la chirurgia e la salute a lungo termine
Per pazienti e chirurghi, questi risultati sottolineano che ciò che conta di più non è solo quanto pancreas viene preservato, ma quale porzione. Rimuovere la coda distale, ricca di isole, comporta un rischio più elevato di diabete rispetto alla rimozione della testa, anche quando viene salvato più tessuto complessivo. Il restringimento del dotto pancreatico dopo una procedura di Whipple può danneggiare ulteriormente il residuo causando cicatrizzazione e atrofia. Gli autori concludono che gli interventi per tumori benigni o a basso rischio dovrebbero essere pianificati per preservare il maggior numero possibile di cellule produttrici di insulina—talvolta privilegiando procedure che risparmino la coda—affinché i pazienti abbiano la migliore probabilità di mantenere una glicemia sana negli anni successivi all’intervento.
Citazione: Lu, WH., Tsai, HM., Liao, TK. et al. Volume and functional changes of remnant pancreas after different types of pancreatectomy: Exploring the regenerative potential. Sci Rep 16, 6947 (2026). https://doi.org/10.1038/s41598-026-36886-4
Parole chiave: pancreatectomia, rigenerazione pancreatica, diabete pancreatogenico, funzione endocrina, pancreaticoduodenectomia vs pancreatectomia distale