Clear Sky Science · it
Meccanismi differenziali di inattivazione di SARS-CoV-2 da parte di tensioattivi anionici: uno studio comparativo tra sali di acidi grassi e tensioattivi sintetici
Perché il sapone che usi continua a fare la differenza
La pandemia di COVID‑19 ha trasformato il lavarsi le mani in un mantra domestico, ma non tutti i saponi agiscono allo stesso modo contro il virus che causa la malattia. Questo studio esamina al microscopio gli ingredienti comuni del sapone per capire quali sono più efficaci nello neutralizzare SARS‑CoV‑2 e come lo fanno. I risultati potrebbero orientare scelte migliori per saponi e disinfettanti di uso quotidiano, rendendo un gesto abituale come lavarsi le mani uno strumento ancora più potente per mantenersi in salute.
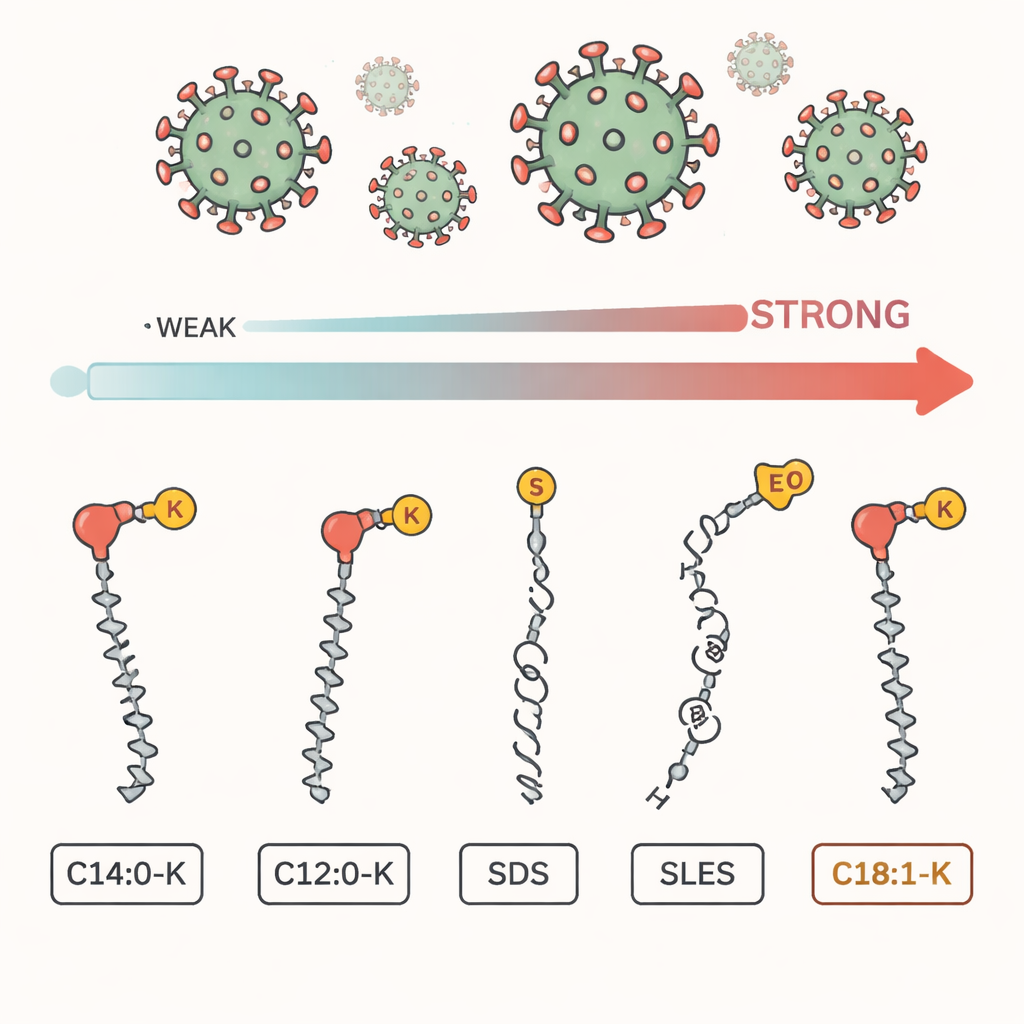
Come il sapone combatte uno scudo grasso
SARS‑CoV‑2, come molti virus pericolosi, è avvolto da un fragile involucro oleoso composto da lipidi. Le molecole del sapone hanno due facce: un lato che ama l’acqua e un altro che ama i grassi. Quando ci laviamo le mani, queste molecole si insinuano in quello strato grasso e possono lacerarlo, rendendo il virus incapace di infettare le cellule. Ma i saponi sono fatti con ingredienti diversi, e questo studio ha confrontato cinque di uso comune: tre sali naturali di acidi grassi (incluso il oleato di potassio, chiamato C18:1‑K) e due tensioattivi sintetici comuni, SDS e SLES, spesso presenti in saponi liquidi e shampoo.
Quali ingredienti del sapone colpiscono di più il virus
Quando i ricercatori hanno mescolato il virus con questi tensioattivi in laboratorio, un ingrediente è emerso chiaramente. C18:1‑K, un componente naturale del sapone con una coda lunga e leggermente piegata, ha ridotto l’infettività del virus di oltre 100.000 volte a concentrazioni molto basse. SDS, un ingrediente sintetico più aggressivo, ha ottenuto solo circa una riduzione di dieci volte allo stesso livello, mentre SLES e un ingrediente con coda più corta, C12:0‑K, hanno quasi non inattivato il virus. Nel complesso il gradimento è stato chiaro: C18:1‑K ha funzionato meglio, seguito da SDS, poi SLES, con gli acidi grassi più corti indietro. Catene più lunghe e più lipofile hanno prodotto un’inattivazione virale molto più potente.
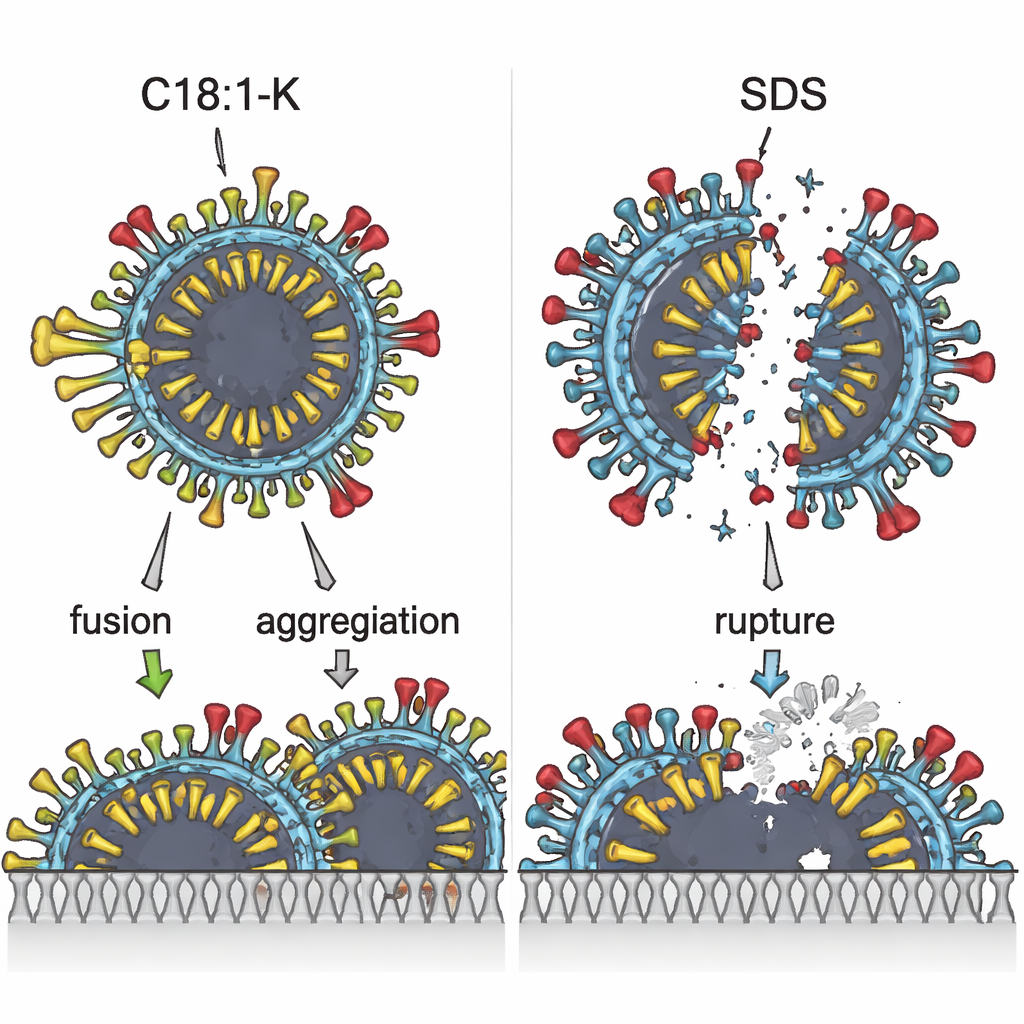
Uno sguardo alle battaglie invisibili
Per capire perché queste differenze fossero così marcate, il gruppo ha usato una tecnica di misurazione termica per tracciare come i tensioattivi interagiscono con il virus. C18:1‑K ha mostrato un profilo termico che indica principalmente l’inserimento della sua coda oleosa nell’involucro lipidico del virus, un processo guidato da forze idrofobiche (attrazione per i grassi). SDS e C12:0‑K, al contrario, hanno mostrato un cambiamento termico opposto, segnalando che si attaccano più alle parti cariche delle proteine sulla superficie virale piuttosto che disturbare profondamente la guaina lipidica. SLES è sembrato trovarsi a metà strada, con le sue tendenze idrofile e idrofobe che in parte si annullano. Queste impronte energetiche hanno rivelato che non solo la potenza, ma anche il modo d’attacco, differiva tra gli ingredienti.
Cosa ha rivelato il microscopio
La microscopia elettronica ha fornito un corrispettivo visivo di questi spostamenti energetici invisibili. Quando il virus è stato trattato con tensioattivi che agiscono principalmente per attrazione elettrica alle proteine, come SDS o C12:0‑K, molte particelle apparivano lacerate o rotte. Con C18:1‑K, invece, le particelle virali apparivano più spesso fuse o aggregate, senza evidenti rotture. Tutti i tensioattivi hanno causato un certo grado di aggregazione virale a concentrazioni più alte, ma solo C18:1‑K ha prodotto estese formazioni a «membrana fusa», che è improbabile rimangano infettive. L’ingrediente che ha inattivato meglio il virus, C18:1‑K, ha anche mostrato la concentrazione micellare critica più bassa — un segnale che le sue code oleose si assemblano facilmente e possono disturbare fortemente l’involucro virale una volta raggiunta una certa soglia.
Cosa significa per la protezione di tutti i giorni
Per i non specialisti, il messaggio è semplice: il sapone per le mani danneggia chimicamente SARS‑CoV‑2, e alcuni ingredienti di origine naturale sono particolarmente efficaci. I saponi ricchi di sali di acidi grassi a catena lunga come l’oleato di potassio possono attaccare l’involucro oleoso del virus attraverso forti interazioni idrofobe e favorire la fusione e l’aggregazione delle particelle virali, rendendole innocue. Sebbene tutti i tensioattivi testati possano contribuire all’inattivazione, quelli progettati o selezionati per una forte azione idrofoba possono offrire una protezione superiore. Queste intuizioni possono aiutare i chimici a progettare saponi e disinfettanti più efficaci e delicati sulla pelle non solo contro SARS‑CoV‑2, ma anche contro altri virus avvolti che dipendono dallo stesso tipo di fragile rivestimento lipidico.
Citazione: Yamamoto, A., Iseki, Y., Elsayed, A.M.A. et al. Differential mechanisms of SARS-CoV-2 inactivation by anionic surfactants: a comparative study of fatty acid salts and synthetic surfactants. Sci Rep 16, 6394 (2026). https://doi.org/10.1038/s41598-026-36858-8
Parole chiave: lavaggio delle mani, SARS-CoV-2, tensioattivi del sapone, involucro virale, disinfettanti