Clear Sky Science · it
Farmacocinetica, patologia ed efficacia dell’inibitore della proteasi principale SARS-CoV-2 VPC285785 in un modello murino di infezione da coronavirus
Perché abbiamo ancora bisogno di pillole migliori contro il COVID
Le prime pillole antivirali per il COVID-19, come il Paxlovid, hanno segnato una svolta nella pandemia. Non sono tuttavia perfette: devono essere assunte molto precocemente, richiedono più compresse al giorno e possono interferire in modo pericoloso con altri farmaci. Questo studio esplora nuovi candidati farmacologici progettati per bloccare il coronavirus in più modi, funzionare bene come singole compresse per via orale e causare meno problemi di interazione farmacologica, usando un modello murino di infezione da coronavirus.
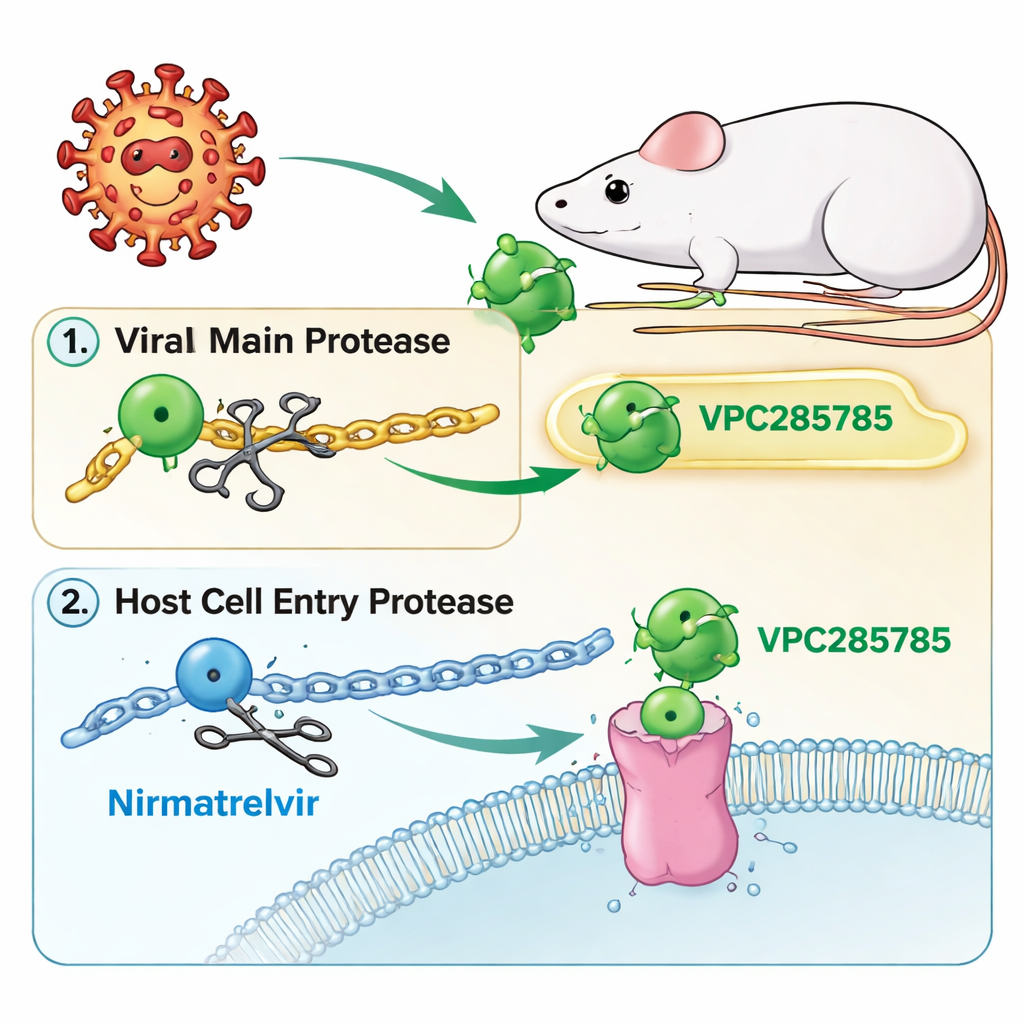
Una nuova variante sull’obiettivo della proteasi del COVID-19
Come il Paxlovid, i nuovi composti — chiamati VPC285785 e VPC285786 — mirano alla “proteasi principale” del virus, delle forbici molecolari che tagliano le lunghe proteine virali in parti funzionanti. Se queste forbici si bloccano, il virus non può completare la propria costruzione e si arresta. I ricercatori hanno anche progettato le molecole per colpire una seconda proteina nelle nostre cellule, la cisteina proteasi cathepsina L, che aiuta alcuni coronavirus a entrare nelle cellule. Mirando sia alle forbici virali sia a un fattore cellulare di ingresso, il gruppo sperava di creare una pillola a doppia azione che fosse più difficile da eludere per il virus e che non richiedesse un farmaco potenziante.
Progettate per durare, non per un potenziatore
Il Paxlovid combina il nirmatrelvir con un altro farmaco, il ritonavir, il cui scopo non è combattere il virus ma rallentare la degradazione del nirmatrelvir nel fegato. Il ritonavir, però, interferisce con molti enzimi che metabolizzano farmaci comuni, portando a interazioni complesse e talvolta pericolose. VPC285785 e VPC285786 sono stati modificati chimicamente per resistere alla degradazione da soli, usando elementi come atomi di fluoro e un irrigidimento degli anelli che li rende meno appetibili agli enzimi epatici. Nei test di laboratorio con preparati di fegato umano e murino, entrambi i nuovi composti si sono dimostrati almeno altrettanto stabili quanto il nirmatrelvir, e VPC285786 in alcuni aspetti si è rivelato ancora più robusto, senza alcun ritonavir presente.
Come si comportano i farmaci e come si distribuiscono nei topi
Il gruppo ha poi esaminato come i composti si muovono nell’organismo dei topi, misurando la velocità con cui scompaiono dal sangue e quanto sono ben assorbiti per via orale. Dopo iniezione, VPC285785 e VPC285786 sono rimasti in circolo per un tempo simile al nirmatrelvir e hanno raggiunto una esposizione complessiva superiore. Somministrati per via orale, però, i loro percorsi sono divergenti: VPC285785 ha ottenuto un assorbimento moderato ma utilizzabile (circa il 15% della dose ingerita raggiunge la circolazione), mentre VPC285786 è entrato nel sangue solo in minima parte (circa il 3%). Poiché le compresse devono attraversare la parete intestinale per essere trattamenti pratici, solo VPC285785 è stato portato avanti negli esperimenti di infezione.
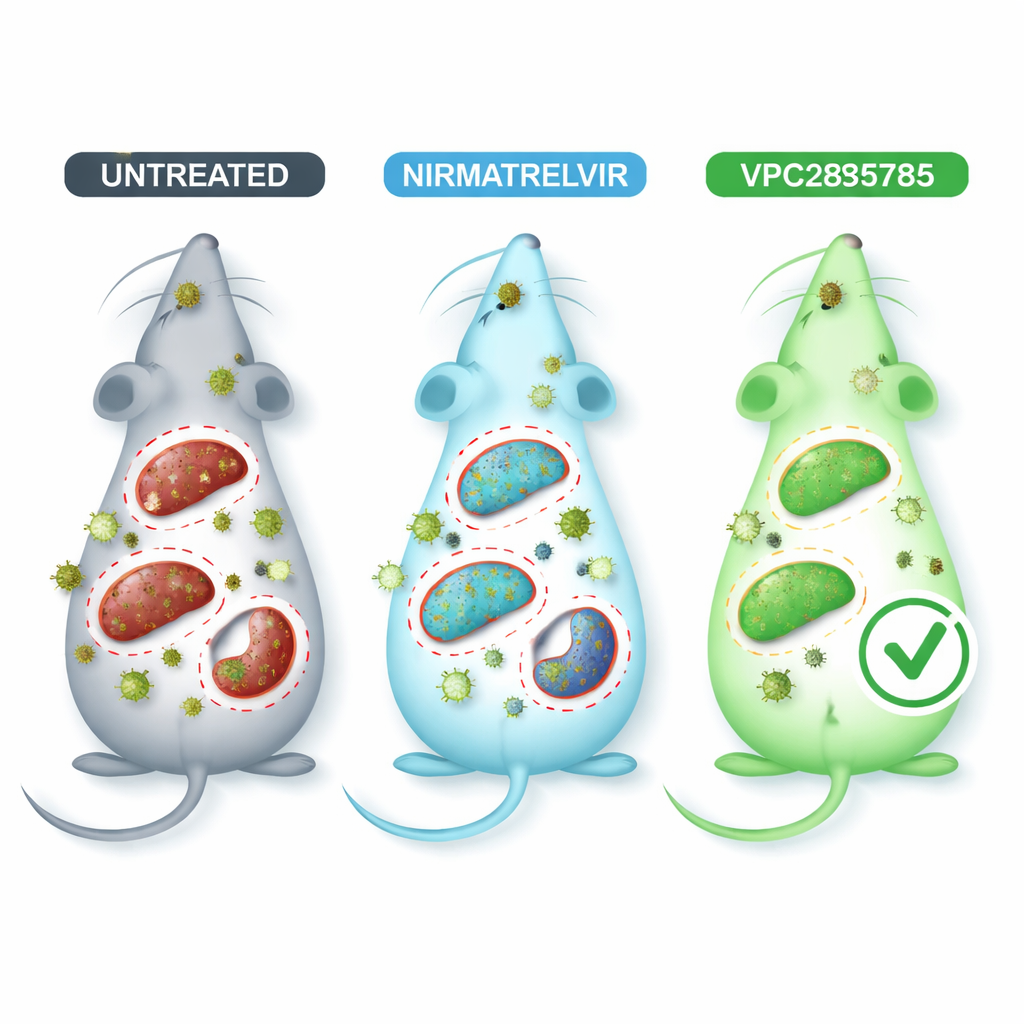
Mettere alla prova la nuova pillola nei topi infettati
Per simulare la malattia da coronavirus in un contesto più sicuro, i ricercatori hanno usato un coronavirus murino chiamato MHV-A59, che invade più organi e provoca danni a polmoni e fegato in modi simili all’infezione umana. I topi infettati sono stati trattati per via orale con VPC285785, con nirmatrelvir come confronto, o con un veicolo inattivo. Gli esami del sangue hanno mostrato che l’infezione ha stressato fegato e reni, ma gli animali trattati con VPC285785 o con nirmatrelvir tendevano ad avere parametri epatici e renali più sani rispetto ai topi non trattati. Più significativamente, VPC285785 ha ridotto nettamente la quantità di materiale genetico virale nel fegato, nel cervello e nella milza, mentre il nirmatrelvir ha prodotto una diminuzione evidente solo nel cervello. Nei polmoni, nel cuore e nei reni, nessuno dei due trattamenti ha mostrato una forte differenza nelle condizioni testate.
Che cosa potrebbe significare per i futuri trattamenti contro il COVID
Pur essendo VPC285785 meno potente contro la proteasi virale in provetta rispetto al nirmatrelvir, funziona bene negli animali vivi, riducendo in modo significativo i livelli virali in diversi organi chiave e preservando la funzione d’organo, il tutto senza un potenziatore ritonavir. Il composto affine, VPC285786, dimostra che è possibile un targeting duale ancora più forte della proteasi virale e della cathepsina L, ma il suo scarso assorbimento deve essere risolto. Nel complesso, questi risultati suggeriscono che le pillole anti‑COVID di prossima generazione potrebbero essere progettate come farmaci singoli, disponibili per via orale, che colpiscono sia bersagli virali sia cellulari, offrono meno interazioni pericolose con altri medicinali e mantengono una protezione significativa nei tessuti vitali.
Citazione: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Parole chiave: antivirali SARS-CoV-2, inibitori della proteasi principale, alternative a Paxlovid, modello murino di coronavirus, trattamento orale per COVID