Clear Sky Science · it
YTHDC1 modula il fenotipo maligno del retinoblastoma mediante l'autofagia mediata da SQSTM1
Perché questo conta per il cancro oculare dei bambini
Il retinoblastoma è il tumore oculare più comune nei bambini piccoli. I medici spesso riescono a curarlo se viene diagnosticato precocemente, ma quando il tumore inizia a invadere i tessuti intorno all’occhio o a estendersi verso il cervello, salvare sia la vita sia la vista del bambino diventa molto più difficile. Questo studio esplora un “freno” molecolare all’interno delle cellule tumorali — due molecole chiamate YTHDC1 e SQSTM1 — che sembrano contribuire a mantenere il retinoblastoma meno aggressivo. Capire come funziona questo freno potrebbe aprire nuove strade per trattamenti più mirati e meno invasivi.
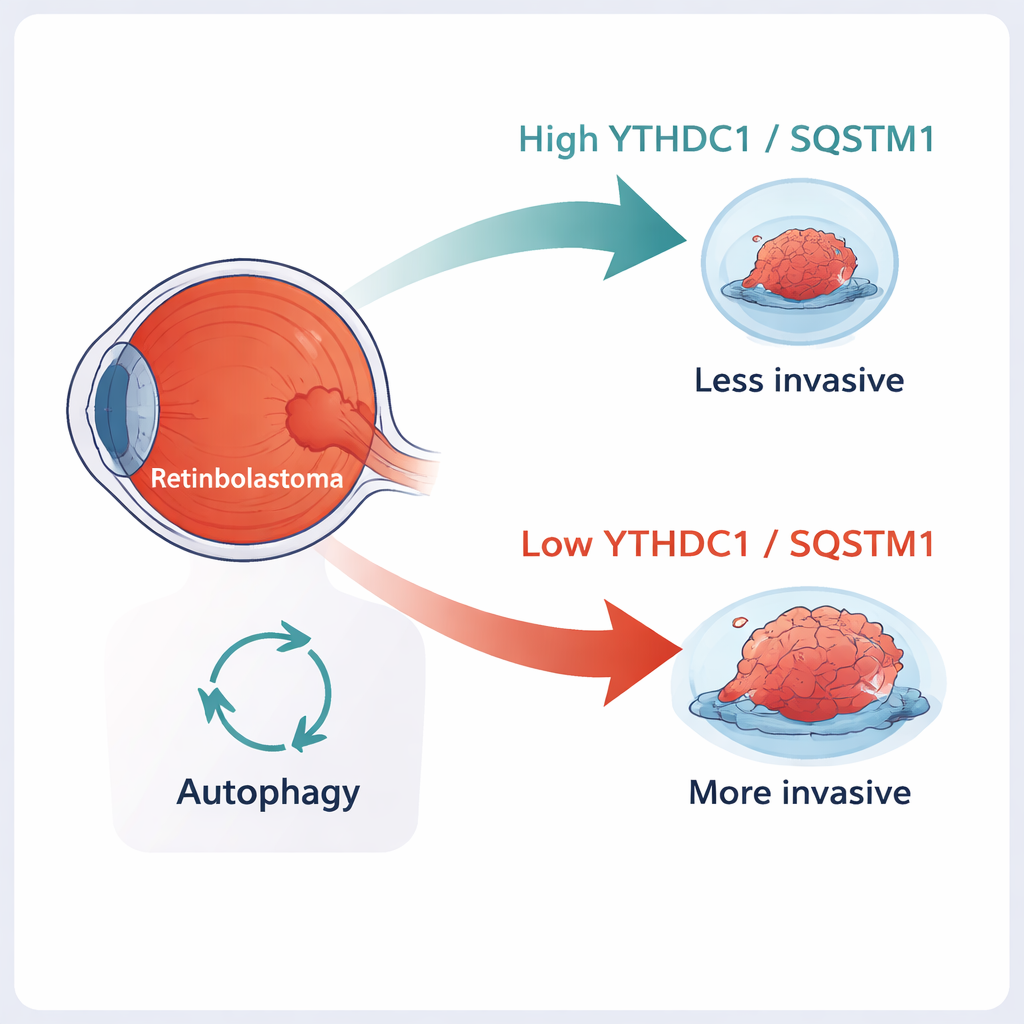
Uno sguardo più ravvicinato ai tumori oculari infantili
Il retinoblastoma origina dallo strato fotosensibile dell’occhio, la retina, generalmente nei bambini sotto i cinque anni. Classicamente la malattia inizia quando vengono persi entrambi gli alleli di un gene guardiano, RB1. Ma la perdita di RB1 da sola non spiega completamente perché alcuni tumori restano confinati all’occhio mentre altri penetrano nei tessuti circostanti o si diffondono lungo il nervo ottico. Sempre più ricercatori riconoscono che i marcatori chimici posti sull’RNA — i messaggi temporanei che dicono alla cellula quali proteine produrre — possono influenzare in modo significativo il comportamento dei tumori. Uno dei marcatori più comuni, chiamato m6A, può modificare la stabilità di questi messaggi e la loro durata all’interno della cellula.
Scoprire un freno molecolare mancante
Gli autori hanno iniziato confrontando l’attività genica in tumori rimasti all’interno dell’occhio con quelli già invasivi. Utilizzando un dataset pubblico di sequenziamento dell’RNA da campioni di retinoblastoma, hanno identificato migliaia di geni la cui attività differiva tra i due gruppi e si sono poi concentrati su regolatori chiave di m6A. Questi includono enzimi che aggiungono o rimuovono m6A e proteine “lettrici” che interpretano questo marcatore. Tra dieci regolatori principali, hanno constatato che un lettore, YTHDC1, era costantemente più basso nei tumori invasivi. Esaminando campioni di 50 bambini e svolgendo test di laboratorio sui tessuti tumorali, hanno confermato che i livelli di YTHDC1 — sia dell’RNA sia della proteina — erano ridotti nei tumori più aggressivi.
Mettere YTHDC1 alla prova
Per capire cosa faccia concretamente YTHDC1, il gruppo ha manipolato i suoi livelli in due linee cellulari umane di retinoblastoma. Quando hanno abbassato YTHDC1 con strumenti genetici, le cellule si sono moltiplicate più rapidamente e hanno attraversato meglio membrane artificiali che simulano barriere tissutali — segnali di un tumore più invasivo. Nei topi, le cellule prive di YTHDC1 hanno formato tumori più grandi e pesanti. Anche l’opposto è risultato vero: indurre nelle cellule una sovraespressione di YTHDC1 ha rallentato la loro crescita e ridotto la capacità di migrare e invadere. Questi esperimenti suggeriscono che YTHDC1 agisca come soppressore tumorale, aiutando a contenere i comportamenti più pericolosi del retinoblastoma.
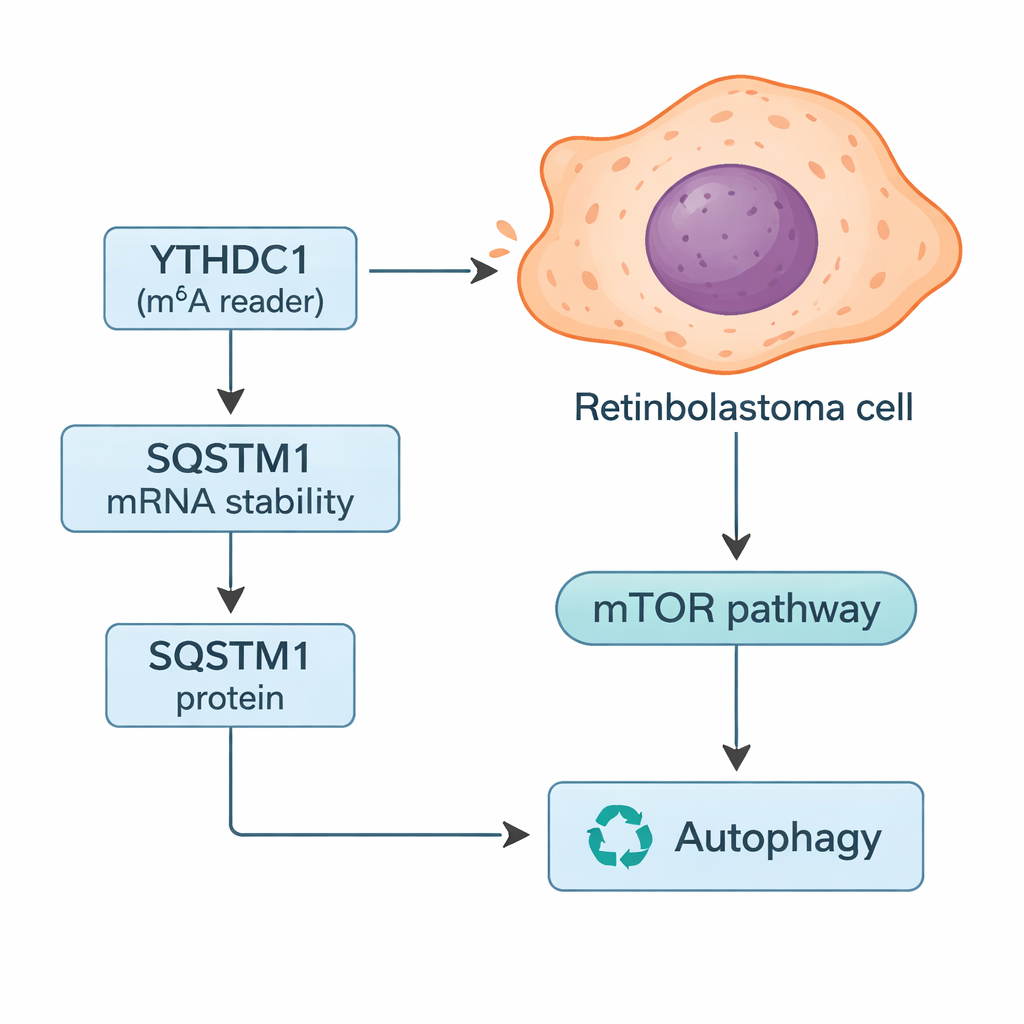
Come YTHDC1 controlla il sistema di riciclo della cellula
Approfondendo, i ricercatori hanno cercato geni specifici i cui messaggi potessero essere regolati da YTHDC1. Combinando ricerche in banche dati con i loro dati tumorali, hanno individuato SQSTM1, una proteina meglio nota come p62. SQSTM1 contribuisce a gestire l’autofagia, il sistema di riciclo cellulare che degrada componenti danneggiati e può fornire energia quando le risorse scarseggiano. Lo studio ha mostrato che YTHDC1 si lega fisicamente all’RNA di SQSTM1 e ne stabilizza il messaggio, permettendo la produzione di più proteina SQSTM1. Quando YTHDC1 veniva ridotto, i livelli di SQSTM1 calavano e il suo RNA degradava più rapidamente. Silenziare SQSTM1 da solo rendeva le cellule di retinoblastoma più proliferative e invasive, e attenuava parzialmente gli effetti protettivi osservati con la sovraespressione di YTHDC1, collocando SQSTM1 come un intermediario chiave in questa via.
Autofagia, energia e aggressività tumorale
Poiché SQSTM1 è centrale per l’autofagia, il gruppo ha testato come la modulazione di YTHDC1 e SQSTM1 influisse su questo processo di riciclo. Utilizzando una combinazione di markers fluorescenti e misure proteiche, hanno riscontrato che la riduzione di YTHDC1 o di SQSTM1 aumentava il “flusso” autofagico — più materiale cellulare veniva incanalato nel sistema di riciclo. Hanno anche osservato cambiamenti nella via mTOR, un interruttore chiave sensibile ai nutrienti che normalmente sopprime l’autofagia. Con meno SQSTM1, l’attività di mTOR scendeva, coerente con un aumento dell’autofagia. Negli esiti invasivi del retinoblastoma, gli autori propongono che la riduzione di YTHDC1 porti a segnali SQSTM1 più deboli, a una minore attività di mTOR e a un’autofagia aumentata che aiuta le cellule tumorali a sopravvivere allo stress e a diffondersi.
Cosa significa per i trattamenti futuri
Per un non specialista, il messaggio principale è che questo studio identifica una catena di eventi dentro le cellule di retinoblastoma — YTHDC1 che controlla SQSTM1, che a sua volta modula il sistema di riciclo cellulare — che influenza quanto il tumore diventi aggressivo. Quando questa catena si indebolisce, i tumori crescono più in fretta e invadono di più. Pur rimanendo molto lavoro da fare prima che questi risultati possano arrivare in clinica, la via offre nuove idee terapeutiche: ripristinare la funzione di YTHDC1, stabilizzare SQSTM1 o modulare l’autofagia e l’attività di mTOR potrebbero un giorno integrare le chemioterapie esistenti. Per i bambini colpiti da questo cancro oculare, tali strategie mirate potrebbero aiutare a limitare la diffusione del tumore preservando più vista e riducendo gli effetti collaterali dei trattamenti.
Citazione: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Parole chiave: retinoblastoma, YTHDC1, SQSTM1, autofagia, via mTOR