Clear Sky Science · it
Irisin regola il metabolismo lipidico e la ferroptosi nelle cellule del cancro ovarico modulando l’asse ALOX5-5-HETE-PD-L1
Perché questa molecola vegetale è importante per il cancro ovarico
Il cancro ovarico è uno dei tumori più letali nelle donne perché viene spesso diagnosticato in fase avanzata e tende a recidivare dopo il trattamento. Questo studio indaga se un composto naturale chiamato tectorigenina, presente nella pianta Belamcanda chinensis, possa rallentare il cancro ovarico privando le cellule tumorali di determinati lipidi e inducendole a una forma di morte cellulare dipendente dal ferro. Esamina inoltre se questo composto possa indebolire il “mantello d’invisibilità” che i tumori usano per nascondersi dal sistema immunitario.
Una fonte di carburante nascosta all’interno delle cellule tumorali
Come molti tumori, i tumori ovarici riorientano il modo in cui gestiscono i lipidi. Invece di usarli solo per energia, le cellule cancerose li accumulano come mattoni per nuove membrane e come cuscinetto contro i danni. In cellule di cancro ovarico coltivate in laboratorio, l’aggiunta di acidi grassi monoinsaturi ha portato a un accumulo di acidi grassi liberi, trigliceridi e colesterolo—forme chiave di grasso immagazzinato. Questo surplus lipidico ha favorito la crescita e l’invasione delle cellule e le ha aiutate a resistere a un processo distruttivo chiamato ferroptosi, in cui il ferro e i lipidi ossidati provocano la rottura delle membrane cellulari. In altre parole, il metabolismo lipidico alterato ha fornito al cancro un vantaggio di crescita e uno scudo di sopravvivenza.
Spingere le cellule tumorali verso l’autodistruzione
I ricercatori hanno quindi testato la tectorigenina sia su cellule ovariche normali sia su diverse linee di cellule di cancro ovarico. A dosi fino a 200 microgrammi per litro, il composto non ha danneggiato le cellule normali ma ha chiaramente rallentato la crescita delle cellule tumorali, ridotto la loro capacità di invadere attraverso una membrana e aumentato il tasso di morte cellulare programmata. Quando le cellule tumorali sono state pretrattate con un farmaco che blocca la ferroptosi, sono diventate più aggressive. L’aggiunta di tectorigenina ha invertito questi effetti: le riserve lipidiche sono diminuite, sono aumentati i livelli di marker legati al ferro e all’ossidazione, e più cellule sono morte. In modelli murini portatori di tumori ovarici umani, le iniezioni di tectorigenina hanno ridotto le dimensioni dei tumori, abbassato il contenuto lipidico nei tessuti tumorali e incrementato i segni chimici di ferroptosi, suggerendo ancora una volta che il composto spinge le cellule tumorali verso questa via di morte dipendente dal ferro.
Un interruttore molecolare chiave che collega i lipidi e la fuga dal sistema immunitario
Per capire come la tectorigenina agisce a livello molecolare, il team ha combinato l’analisi di grandi banche dati con la modellizzazione informatica delle interazioni farmaco‑proteina. Hanno individuato un enzima chiamato ALOX5, che converte un acido grasso comune in una molecola di segnalazione chiamata 5‑HETE. Nelle cellule di cancro ovarico e nei campioni tumorali, i livelli di ALOX5 erano molto più alti rispetto ai tessuti normali. Simulazioni di docking e dinamica molecolare hanno mostrato che la tectorigenina può legarsi stabilmente ad ALOX5, agendo come un freno interno. Quando i ricercatori hanno aumentato artificialmente ALOX5 nelle cellule tumorali, le riserve lipidiche sono aumentate, i marker di ferroptosi sono diminuiti e le cellule sono diventate più invasive. Il trattamento con tectorigenina ha annullato questi cambiamenti. L’abbattimento di ALOX5 ha prodotto l’effetto opposto—meno grasso, più ferroptosi e crescita indebolita—collocando con decisione questo enzima al centro dell’azione del composto.
Come i tumori perdono il loro scudo contro il sistema immunitario
Lo studio ha inoltre collegato questa via lipidica a una importante molecola del checkpoint immunitario chiamata PD‑L1, che i tumori usano per disattivare le cellule immunitarie attaccanti. Il prodotto di ALOX5, il 5‑HETE, ha aumentato i livelli di PD‑L1, rafforzando questo scudo. Quando ALOX5 è stato silenziato, sono diminuiti sia 5‑HETE sia PD‑L1; quando il 5‑HETE è stato reintegrato, PD‑L1 è risalito e le cellule tumorali hanno riacquistato parte della loro protezione dalla ferroptosi. La tectorigenina ha ridotto ALOX5, abbassato 5‑HETE e, di conseguenza, diminuito PD‑L1 sia nelle colture cellulari sia nei tumori nei topi. Questo suggerisce che colpendo un singolo enzima metabolico, il composto può sia interrompere le difese lipidiche del cancro sia indebolire la sua capacità di nascondersi dall’attacco immunitario.
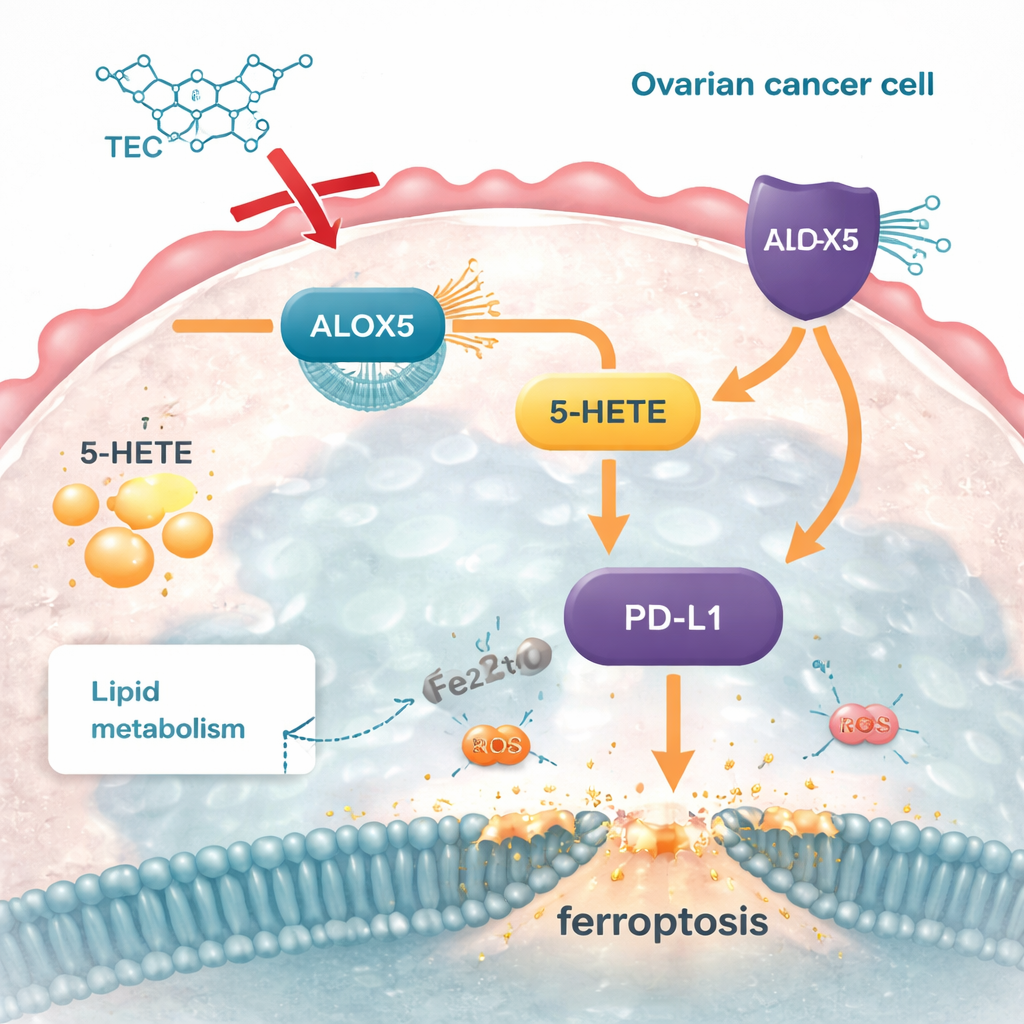
Cosa potrebbe significare per i trattamenti futuri
In parole semplici, questo lavoro mostra che la tectorigenina agisce come una chiave di precisione inserita nel meccanismo di gestione dei lipidi della cellula tumorale. Bloccando ALOX5, interrompe la produzione di 5‑HETE, riduce l’accumulo eccessivo di lipidi, rende le cellule vulnerabili al danno indotto dal ferro e toglie parte della loro mimetizzazione immunitaria. Sebbene questi risultati provengano da studi su cellule e topi—e molto resta da verificare negli esseri umani—indicano una strategia promettente: mirare all’asse ALOX5–5‑HETE–PD‑L1 per privare i tumori ovarici delle loro riserve e renderli più esposti alle difese dell’organismo o alle future immunoterapie.
Citazione: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Parole chiave: cancro ovarico, metabolismo lipidico, ferroptosi, ALOX5, terapia con composti naturali