Clear Sky Science · it
Caratterizzazione sperimentale della somministrazione della terapia con protoni a minibeam in condizioni di dose-rate FLASH
Fascio di radiazioni più veloce e meno dannoso
La radioterapia è una colonna portante del trattamento del cancro, ma può danneggiare anche i tessuti sani oltre ai tumori. Questo studio esplora un nuovo modo di somministrare radiazioni protoniche che mira a colpire duramente i tumori attenuando l’impatto sugli organi normali. Combinando due idee emergenti — i “minibeam” molto ravvicinati e i tassi di dose ultra‑rapidi di FLASH — i ricercatori dimostrano che è tecnicamente possibile erogare trattamenti altamente precisi in pochi secondi utilizzando apparecchiature simili a quelle già presenti negli ospedali moderni.
Perché trasformare la radiazione in fasci sottilissimi?
I campi di radiazione tradizionali appaiono uniformi: la dose è distribuita in modo relativamente omogeneo nella regione trattata. La radioterapia frazionata spazialmente infrange intenzionalmente questa regola. Nella terapia con protoni a minibeam, la radiazione è suddivisa in numerosi fasci sottili submillimetrici separati da spazi vuoti. Vicino alla superficie ciò crea un motivo di “picchi” ad alta dose e “valli” a bassa dose. Il tessuto sano tra i picchi ha maggiori possibilità di ripararsi, mentre più in profondità i fasci si disperdono e si sovrappongono, fornendo al tumore una dose più uniforme ed efficace. Studi preliminari in laboratorio e su animali suggeriscono che questo schema può ridurre gli effetti collaterali e può persino stimolare risposte immunitarie utili contro il cancro.
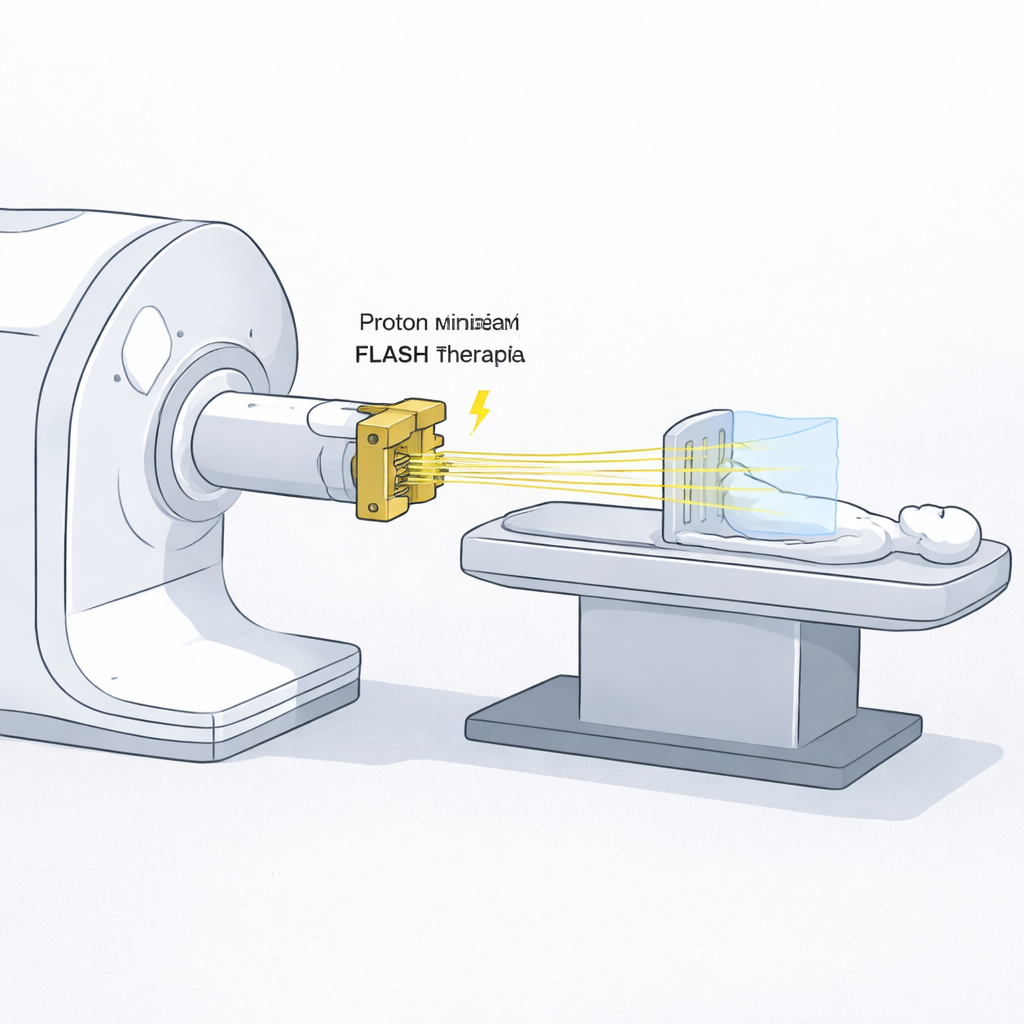
Cos’è FLASH e perché la velocità conta?
La terapia FLASH è un nuovo modo di concepire il tempo nella somministrazione della radiazione. Invece di erogare lentamente una dose nell’arco di decine di secondi o minuti, FLASH somministra la stessa dose in una frazione di secondo a tassi di dose ultra‑elevati — decine o centinaia di gray al secondo. Sorprendentemente, molti esperimenti hanno mostrato che i tessuti normali possono essere meglio preservati in queste condizioni estreme, mentre i tumori restano altrettanto vulnerabili. Per i minibeam protonici, tuttavia, esisteva un ostacolo pratico: i blocchi metallici multi‑fenditura usati per modellare il fascio in raggi sottili sprecano molti dei protoni in ingresso, quindi i trattamenti possono richiedere diversi minuti. Se i minibeam potessero essere erogati in modalità FLASH, il tempo perso potrebbe essere recuperato e i vantaggi biologici di entrambe le metodiche potrebbero essere combinati.
Portare minibeam e FLASH su una macchina clinica
Il gruppo ha lavorato con un sistema protonico clinico compatto che normalmente tratta i pazienti con un fascio protonico di scansione uniforme. Hanno fissato collimatori multi‑fenditura personalizzati in ottone — ciascuno contenente cinque sottili fessure larghe solo 1 millimetro e distanziate di 2,8 millimetri — all’estremità dell’ugello di trattamento. Aumentando la corrente del fascio e ottimizzando con cura l’ottica del fascio, hanno fatto funzionare il sistema in modalità a dose ultra‑alta a 228 MeV, mantenendo comunque la possibilità di tornare alle impostazioni cliniche ordinarie. Hanno poi misurato come la dose si distribuiva in blocchi di plastica che simulano l’acqua usando film radiosensibili speciali e hanno confrontato quelle misure con simulazioni al computer dettagliate che tracciano le interazioni dei singoli protoni.
Come si è comportato il nuovo fascio?
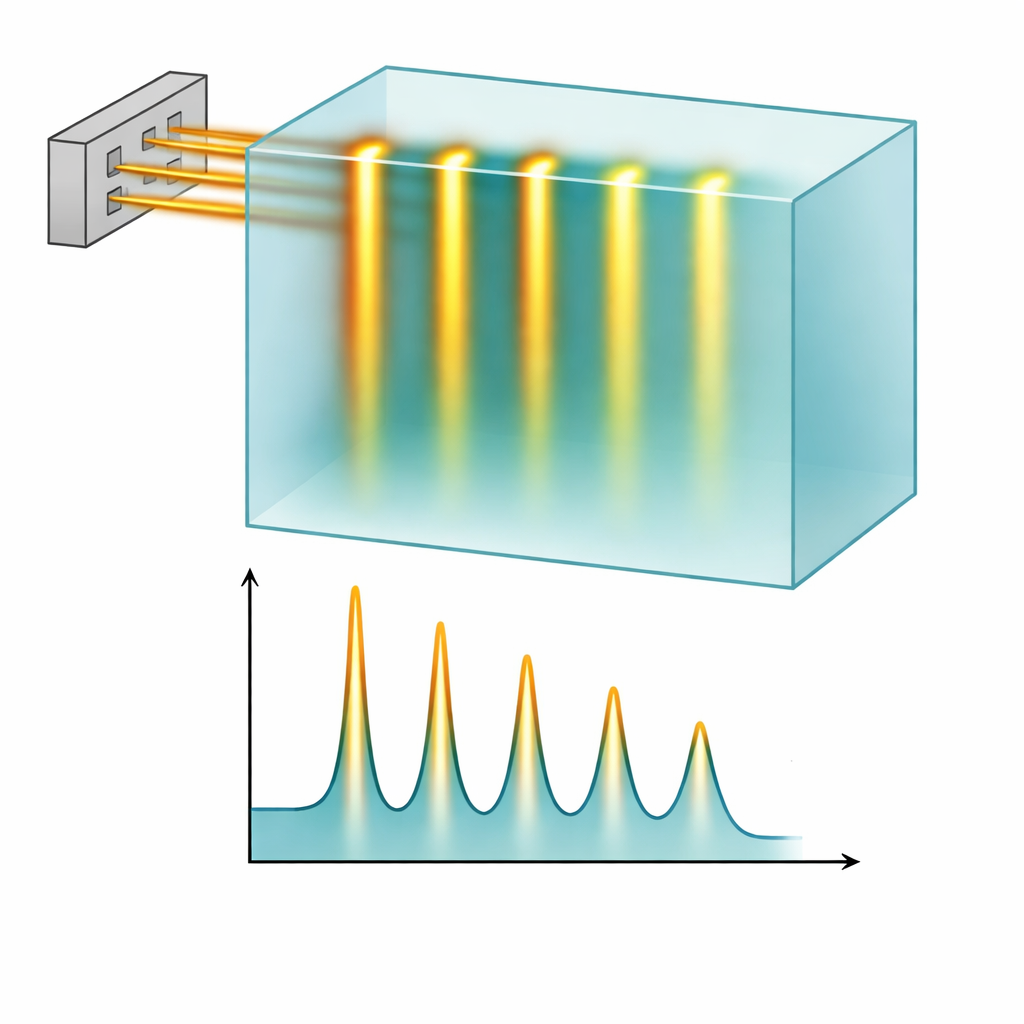
In condizioni FLASH, il fascio protonico ha mantenuto un netto pattern a minibeam: picchi marcati lungo i percorsi delle fessure e valli profonde tra di essi. Misure e simulazioni concordavano strettamente su come questo schema evolvesse con la profondità e su quanto rapidamente si sfocasse a causa della dispersione dei fasci. Un collimatore più spesso da 10 cm ha prodotto una separazione più netta tra picchi e valli rispetto alla versione da 6,5 cm, specialmente vicino alla superficie, proteggendo meglio le regioni di “valle”. Crucialmente, far funzionare la macchina in modalità FLASH ha ridotto il tempo di erogazione per un tipico campo a minibeam di 3 per 3 centimetri da circa 3 minuti a soli 2,5 secondi. Calcoli basati sui log temporali della macchina hanno mostrato che i tassi di dose locali nelle regioni dei picchi superavano agevolmente le soglie comunemente associate a FLASH, il tutto preservando la sottile struttura spaziale dei minibeam.
Cosa potrebbe significare per la cura del cancro in futuro
Questo lavoro è una prova di principio precoce ma importante. Dimostra che un sistema protonico clinico di tipo standard può essere adattato per erogare minibeam protonici a tassi di dose FLASH senza sacrificare precisione o qualità del fascio. I pazienti non vengono ancora trattati in questo modo: gli esperimenti sono stati condotti in allestimenti di prova e è stato usato un singolo fascio ad alta energia, anziché i profili energetici stratificati che i tumori reali richiedono. Anche gli effetti biologici della combinazione di schemi spaziali a minibeam con la somministrazione ultra‑rapida FLASH rimangono da dimostrare su animali e, in ultima istanza, sull’uomo. Tuttavia, lo studio pone le basi tecniche per futuri trattamenti che potrebbero controllare i tumori con la stessa efficacia delle migliori metodiche attuali riducendo drasticamente i danni agli organi sani sfruttando sia dove sia quanto velocemente la radiazione viene somministrata.
Citazione: Lin, Y., Wu, W., Setianegara, J. et al. Experimental characterization of proton minibeam therapy delivery under FLASH dose-rate conditions. Sci Rep 16, 7803 (2026). https://doi.org/10.1038/s41598-026-36739-0
Parole chiave: terapia con protoni, radioterapia FLASH, radiazione a minibeam, trattamento del cancro, velocità di dose delle radiazioni