Clear Sky Science · it
Sviluppo e convalida di un modello murino di carcinoma mammario triplo negativo PSMA-positivo per terapie radionuclide mirate precliniche
Perché questa ricerca è importante
Il carcinoma mammario triplo negativo è una delle forme di cancro al seno più difficili da trattare. Tende a diffondersi rapidamente, offre ai pazienti meno opzioni terapeutiche mirate e spesso recidiva dopo le terapie standard. Allo stesso tempo, una nuova classe di farmaci radioterapeutici “intelligenti” che si legano a una specifica molecola chiamata PSMA ha trasformato la cura del cancro prostatico avanzato. Questo studio pone una domanda semplice ma potente: è possibile costruire un modello di laboratorio realistico di carcinoma mammario triplo negativo che esprima lo stesso bersaglio PSMA, in modo da poter valutare in modo equo se questi farmaci radioterapeutici potrebbero aiutare anche i pazienti con questo tumore aggressivo?
Da un bersaglio prostatico a una sfida nel tumore mammario
La PSMA, acronimo di prostate-specific membrane antigen, è una piccola struttura presente sulla superficie di alcune cellule. È abbondante in molti tumori della prostata e può essere riconosciuta da farmaci radiomarcati che sia rivelano i tumori nelle scansioni sia apportano radiazione direttamente a essi. I ricercatori hanno recentemente scoperto che la PSMA compare, con intensità variabile, anche nei vasi sanguigni e nelle cellule di diversi altri tumori, incluso il carcinoma mammario triplo negativo. Tuttavia, in questi tumori non prostatici la PSMA tende a essere irregolare e meno intensa, rendendo difficile capire se le terapie mirate contro la PSMA funzioneranno. Prima di testare nuovi trattamenti nei pazienti, gli scienziati hanno bisogno di modelli animali che riproducano fedelmente questo pattern di PSMA nei tumori mammari—una cosa che si è rivelata sorprendentemente difficile da ottenere.
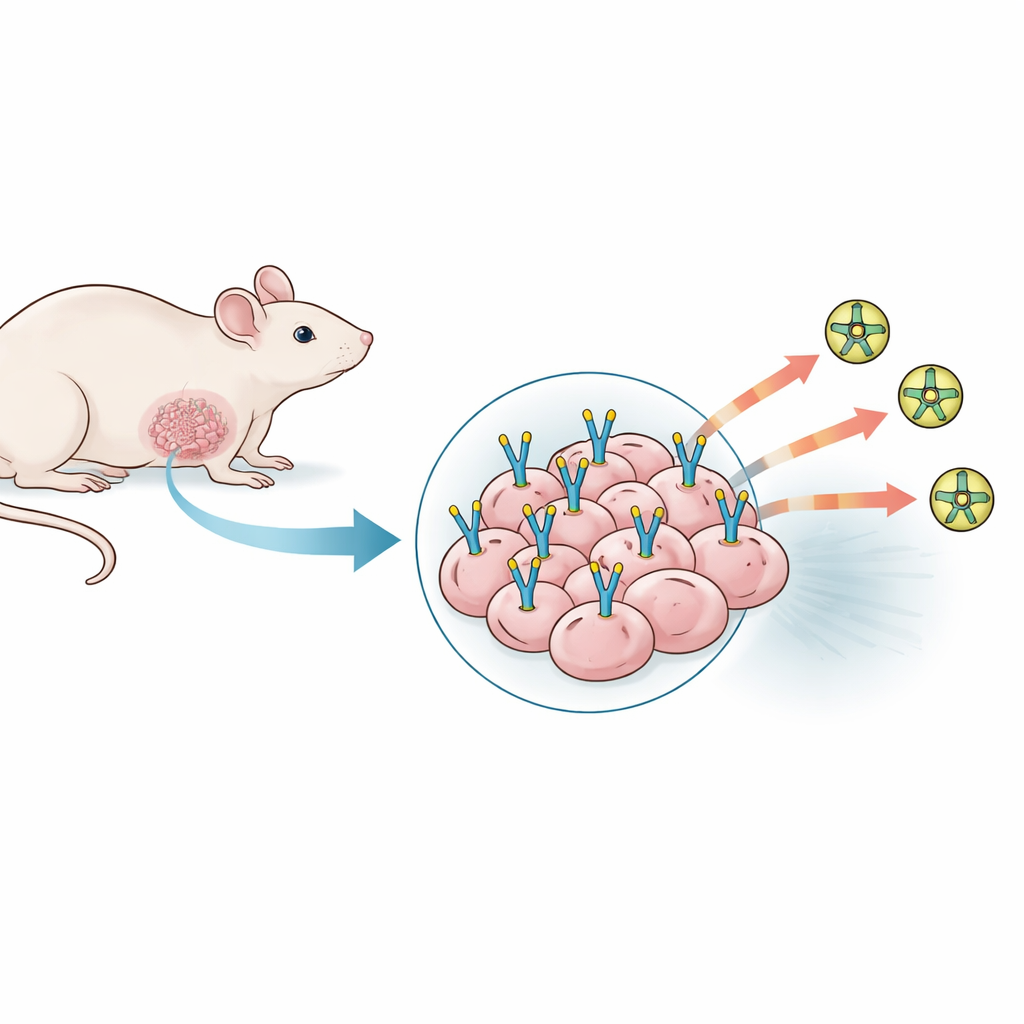
Testare molti modelli tumorali che si rifiutavano di collaborare
Il team ha inizialmente esplorato un'ampia gamma di modelli murini esistenti di carcinoma mammario triplo negativo, utilizzando sia linee cellulari tumorali murine sia umane impiantate in sedi diverse e in condizioni differenti. Hanno variato il numero di cellule tumorali iniettate, aggiunto gel di supporto per favorire la crescita dei vasi, e persino miscelato cellule dei vasi sanguigni umane nella speranza di aumentare i livelli di PSMA. Per ogni modello hanno valutato quanto fossero affidabili l’insorgenza e la crescita dei tumori, ispezionato sezioni tumorali al microscopio e utilizzato un tracciante PET specifico per la PSMA per verificare se i tumori si illuminavano nelle scansioni corporee. Malgrado una crescita tumorale robusta e reti vascolari ricche, nessuno di questi 23 modelli ha mostrato una presenza significativa di PSMA, né con la colorazione tessutale né con l’imaging PET. I tumori risultavano metabolicamente attivi e ben irrorati, ma il vero “sito di ancoraggio” PSMA necessario ai ricercatori era praticamente assente.
Progettare un tumore che mostri il bersaglio giusto
Di fronte a questo ostacolo, i ricercatori hanno seguito una strada più diretta. Hanno modificato geneticamente una linea cellulare umana di carcinoma mammario triplo negativo ampiamente utilizzata, MDA-MB-231, costringendola a esprimere PSMA sulla superficie. Queste cellule alterate sono state poi impiantate nella regione del grasso mammario di topi immunodeficienti, un sito che riproduce meglio l’ambiente naturale della mammella. Gli scienziati hanno creato due versioni del modello: una in cui tutte le cellule tumorali esprimevano PSMA e un altro tumore “misto” contenente parti uguali di cellule PSMA-positive e di cellule tumorali ordinarie, per imitare i pattern a chiazze osservati nei pazienti. Entrambi i modelli hanno formato tumori con la stessa affidabilità e sono cresciuti a velocità simili ai tumori generati da cellule non modificate, dimostrando che l’aggiunta di PSMA non alterava il comportamento intrinseco del cancro.
Osservare il nuovo bersaglio nelle scansioni e al microscopio
Quando il tracciante PET diretto contro la PSMA è stato iniettato in questi topi, i tumori ingegnerizzati sono risultati molto visibili nelle scansioni, con un’assorbimento tumorale circa dieci volte superiore rispetto al fegato o al muscolo. Questo segnale forte e selettivo ha confermato che la PSMA era ora presente in abbondanza sulle cellule tumorali ed era raggiungibile da un farmaco circolante. L’analisi microscopica del tessuto tumorale ha confermato i risultati: la colorazione per PSMA era elevata ma eterogenea, con chiazze di espressione più intensa e altre più debole, somigliante al pattern osservato nei carcinomi mammari triplo negativi umani. È importante sottolineare che la PSMA aggiunta era confinata alle cellule tumorali, non ai vasi circostanti, mantenendo il modello focalizzato sulle terapie mirate alle cellule. Aree di tessuto necrotico all’interno di tumori più grandi non incorporavano il tracciante, coerente con quanto osservato clinicamente.
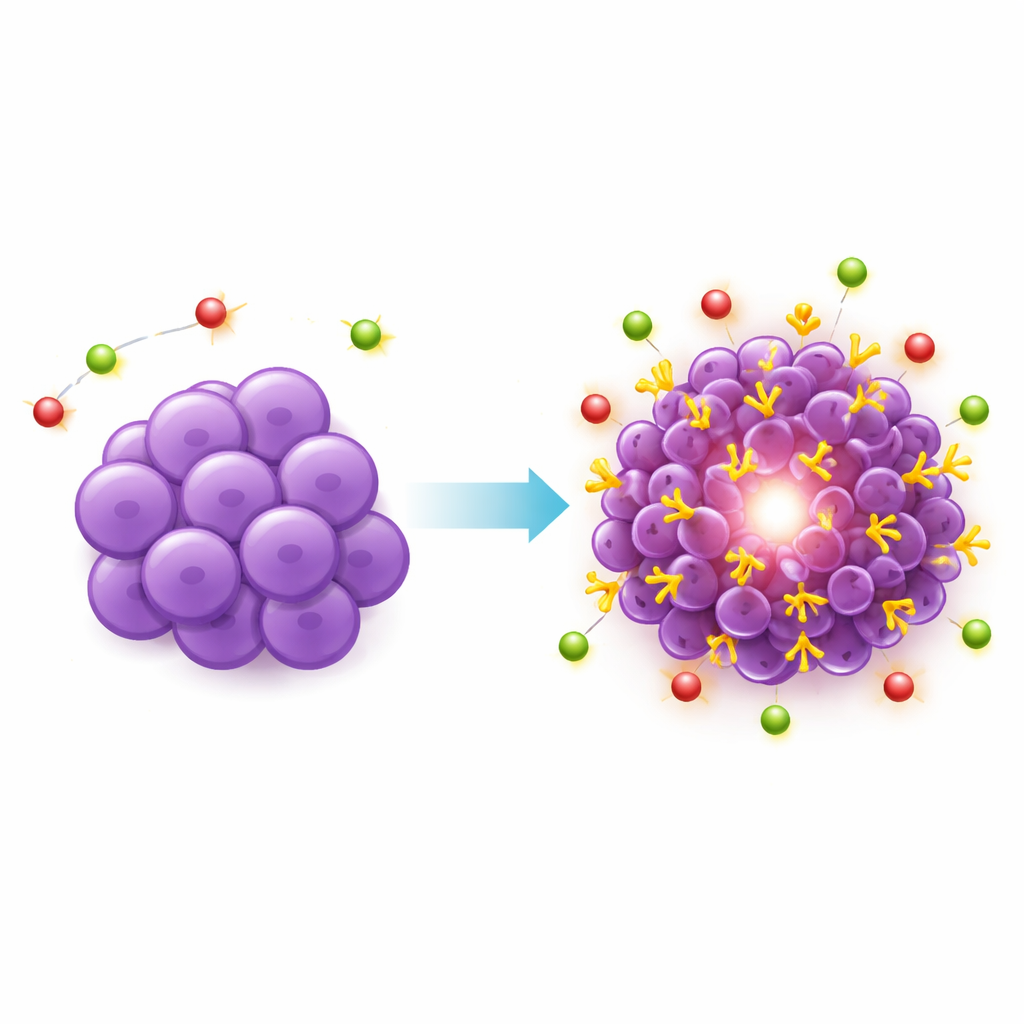
Cosa significa per i trattamenti futuri
Dimostrando in modo sistematico che i modelli murini standard di cancro al seno non esprimono in modo affidabile la PSMA e poi costruendo un nuovo modello che lo fa, questo lavoro fornisce un terreno di prova cruciale per le terapie radioterapeutiche mirate di nuova generazione. Il modello di carcinoma mammario triplo negativo PSMA-positivo è stabile, cresce in modo prevedibile e mostra un mix realistico di aree ad alta e bassa espressione di PSMA, rendendolo adatto a valutare come si comportino i farmaci diretti contro la PSMA prima di testarli nei pazienti. Pur non potendo catturare ogni aspetto della malattia umana—come l’influenza di un sistema immunitario pienamente funzionante—offre uno strumento potente per esplorare se il successo delle terapie basate su PSMA nel cancro prostatico possa un giorno essere esteso alle persone affette da questa forma particolarmente aggressiva di carcinoma mammario.
Citazione: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Parole chiave: carcinoma mammario triplo negativo, PSMA, terapia radionucleidica mirata, modello murino preclinico, imaging PET