Clear Sky Science · it
Caratterizzazione bioinformatica e rilevamento automatizzato di sottopopolazioni di monociti metabolicamente attivate nella dislipidemia
Perché le cellule immunitarie nascoste contano per la salute del cuore
I problemi del colesterolo si discutono di solito in termini di dieta, valori degli esami del sangue e rischio di infarto. Ma sotto quei numeri il nostro sistema immunitario cambia silenziosamente. Questo studio esamina un gruppo speciale di globuli bianchi nel sangue di giovani adulti con LDL elevato (il cosiddetto colesterolo “cattivo”). Queste cellule sembrano diventare “metabolicamente attivate” e conservare una memoria di esposizione a eccessi lipidici, aumentando potenzialmente l’infiammazione delle arterie — e con essa il rischio di malattia cardiovascolare futura. Comprendere questi tipi cellulari nascosti potrebbe aiutare i medici a individuare problemi prima e a progettare trattamenti più mirati.
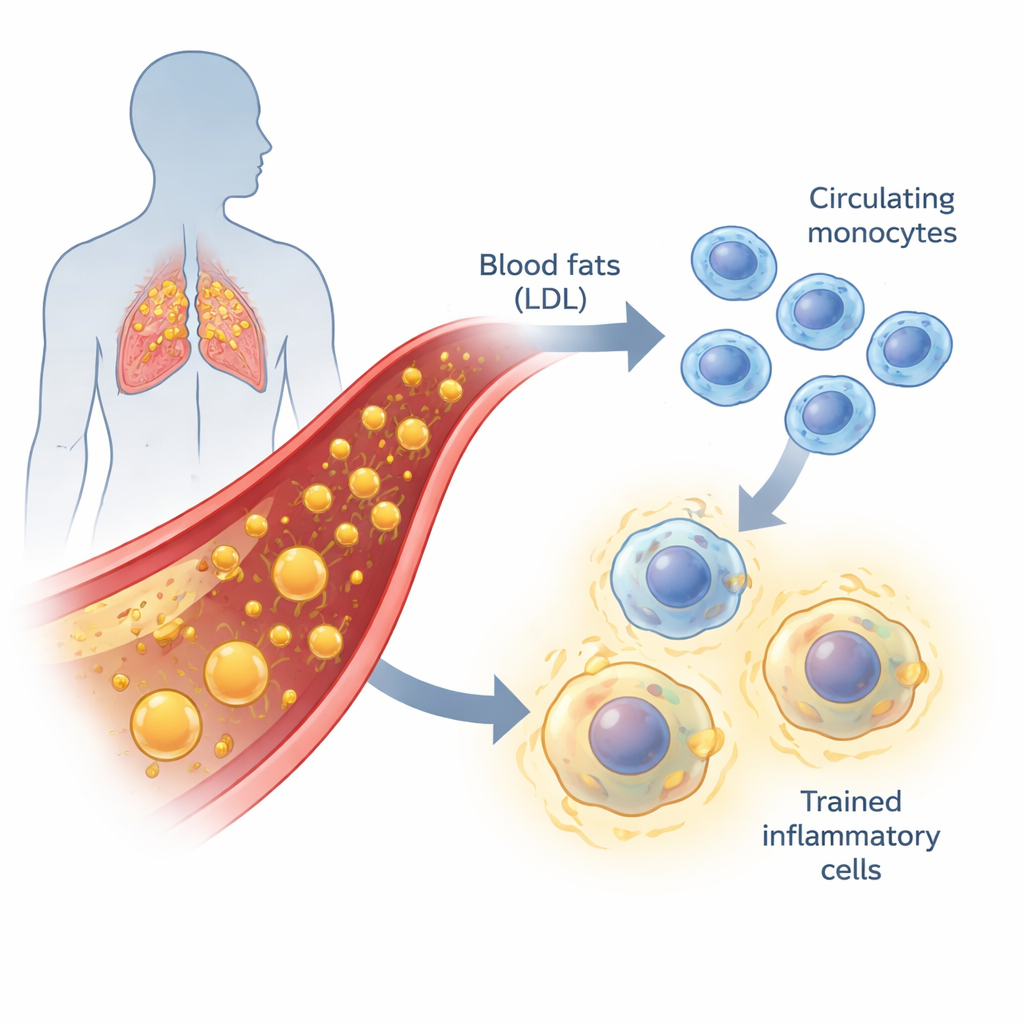
Grassi nel sangue e infiammazione a lenta combustione
L’aterosclerosi, il processo che porta all’ostruzione delle arterie, non riguarda solo il deposito di grasso sulle pareti vascolari. È anche una malattia infiammatoria cronica e lenta. Quando il colesterolo LDL è alto, specialmente nelle sue forme ossidate, irrita l’endotelio dei vasi sanguigni. I monociti — globuli bianchi circolanti — e i macrofagi in cui si trasformano vengono attratti in queste aree e iniziano a inglobare lipidi. Se questo processo di pulizia è mal regolato, le cellule si trasformano in “foam cells” e contribuiscono alla formazione di placche lipidiche. Tradizionalmente, gli scienziati hanno diviso i monociti circolanti in tre gruppi basati su marcatori di superficie, ciascuno con ruoli diversi nel pattugliamento dei vasi, nell’innesco dell’infiammazione o nel mantenimento dell’omeostasi tissutale.
Oltre le etichette: scoprire nuovi tipi di monociti
Gli autori hanno ipotizzato che alcuni monociti circolanti in persone con dislipidemia potessero essere già riprogrammati in uno stato metabolicamente attivo, pronti a diventare macrofagi dannosi. Per esplorare questa possibilità, hanno prelevato sangue da 23 giovani adulti con LDL elevato e da 17 partecipanti sani con profili lipidici normali. Nessuno assumeva farmaci ipocolesterolemizzanti né presentava altre malattie rilevanti, il che ha aiutato a isolare l’impatto della sola dislipidemia. Utilizzando una tecnologia chiamata citometria a flusso, hanno misurato non solo i marcatori di superficie classici ma anche proteine coinvolte nella gestione dei lipidi e tag chimici sugli istoni — piccole proteine che aiutano a regolare quali geni vengono attivati o disattivati in ciascuna cellula.
Algoritmi intelligenti per leggere paesaggi immunitari complessi
Invece di affidarsi solo al “gating” manuale (tracciare confini a occhio su grafici a due marcatori), il team ha costruito una pipeline bioinformatica che trattava ogni cellula come un punto in uno spazio ad alta dimensionalità. Hanno pulito e standardizzato i dati, quindi hanno usato t-SNE, un metodo matematico che trasforma misure a molti marcatori in una mappa bidimensionale dove le cellule simili si raggruppano. Successivamente hanno applicato algoritmi di clustering (X-shift e FlowSOM) per raggruppare automaticamente le cellule con pattern di marcatori affini. Questo ha permesso di andare oltre i tre tipi classici di monociti e identificare quattro popolazioni monocitarie principali definite da combinazioni di proteine per la gestione dei lipidi (ABCA1, PLIN2, CD36) e i consueti marcatori CD14 e CD16.
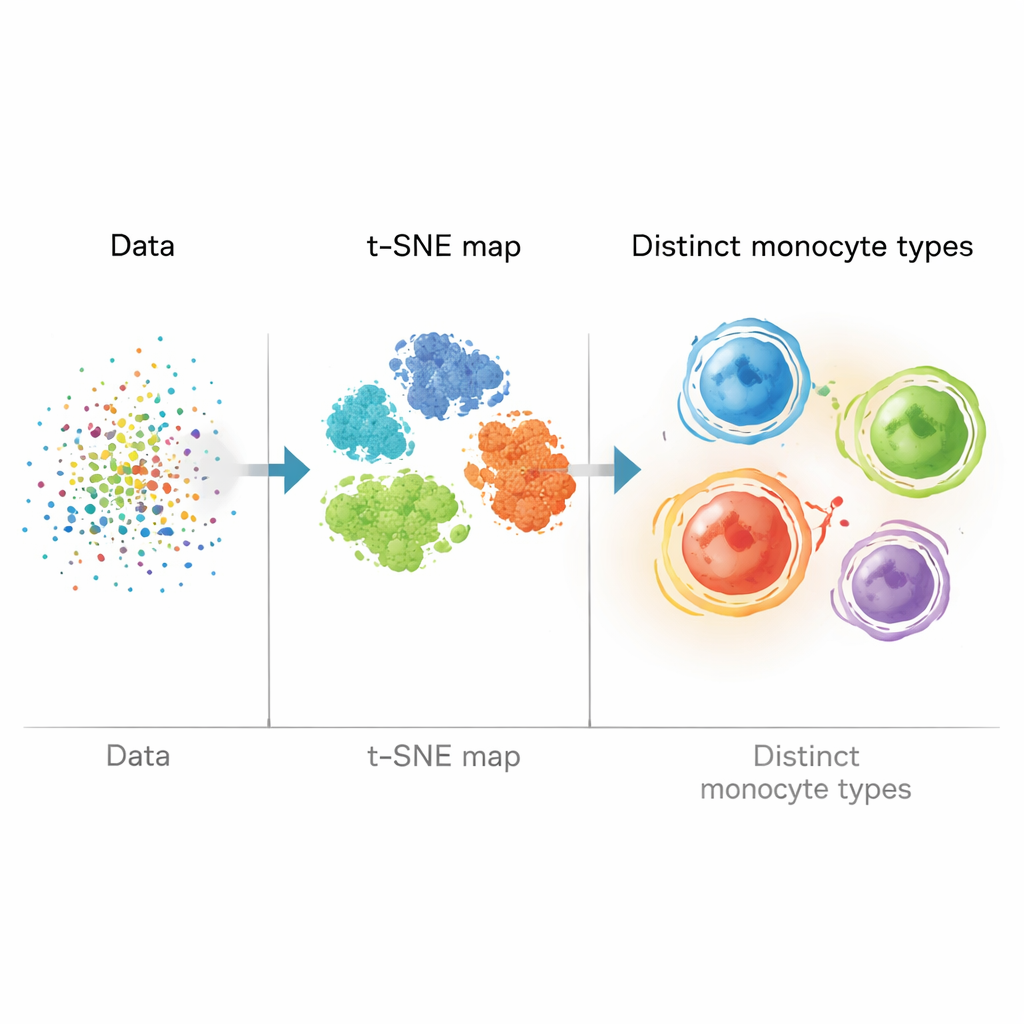
Una popolazione infiammatoria «predisposta» nella dislipidemia
Due di queste quattro popolazioni monocitarie si sono distinte. Una in particolare — caratterizzata da alto CD14, assenza di CD16 e forte espressione di ABCA1 con PLIN2 e CD36 variabili — corrispondeva al profilo dei monociti “metabolicamente attivati” (MoMe). Nelle persone con dislipidemia, questa popolazione MoMe e un gruppo correlato erano significativamente più abbondanti rispetto ai controlli sani. Quando i ricercatori hanno esaminato i marchi epigenetici — in particolare H3K4me3 e H3K27me3, tag chimici sugli istoni legati all’attività genica — hanno trovato che le cellule MoMe degli individui dislipidemici presentavano livelli più elevati di H3K4me3. Questo marchio è associato a geni che promuovono l’infiammazione, suggerendo che queste cellule possiedono una forma di “memoria” innata, o immunità addestrata, dopo esposizioni ripetute a LDL alta.
Dalle cellule circolanti ai macrofagi che costruiscono la placca
Per capire cosa questi monociti potessero diventare nei tessuti, il team ha coltivato monociti purificati in condizioni di laboratorio che imitavano la sindrome metabolica, inducendoli a differenziarsi in macrofagi. Anche in questo caso hanno utilizzato analisi avanzate per identificare sottogruppi di macrofagi e misurare i loro marchi epigenetici. Interessante notare che i macrofagi derivati da donatori sani spesso mostravano livelli più elevati di tag istonici attivanti rispetto a quelli derivati da pazienti dislipidemici, suggerendo che l’addestramento infiammatorio potrebbe manifestarsi in modo diverso una volta che le cellule lasciano il circolo ematico. Pur con una dimensione di campione modesta, i risultati supportano l’idea che l’esposizione prolungata a lipidi plasmatici in eccesso rimodelli i monociti sia a livello proteico sia epigenetico, predisponendoli a risposte infiammatorie più intense.
Cosa significa per i pazienti e per la cura futura
Per un lettore non specialistico, la conclusione è che l’LDL alto non è solo un problema di “troppo grasso” ma anche di cellule immunitarie “riwrestate” (riprogrammate). Questo studio mostra che anche nei giovani adulti la dislipidemia è associata a una popolazione distinta di monociti che appare metabolicamente carica ed epigeneticamente pronta a alimentare l’infiammazione arteriosa. Combinando potenti strumenti computazionali con misurazioni dettagliate delle cellule, i ricercatori possono ora identificare questi tipi di cellule a rischio nel sangue, molto prima che si verifichi un infarto. In futuro, tali approcci potrebbero aiutare i medici a valutare meglio il rischio cardiovascolare, monitorare quanto efficacemente i trattamenti stanno invertendo l’addestramento immunitario dannoso e, in ultima analisi, progettare terapie che prendano di mira non solo i livelli di colesterolo ma anche le cellule immunitarie che rispondono a essi.
Citazione: Ramírez-Torres, R., Ramírez-Segovia, S.G., González-Huerta, M.J. et al. Bioinformatic characterization and automated detection of metabolically activated monocyte subpopulations in dyslipidemia. Sci Rep 16, 6170 (2026). https://doi.org/10.1038/s41598-026-36678-w
Parole chiave: dislipidemia, monociti, immunità addestrata, aterosclerosi, citometria a flusso