Clear Sky Science · it
Applicazione di Lactococcus che esprime la proteina collagen‑like 1 dello streptococco di gruppo A come nuova immunoterapia contro l’adenocarcinoma duttale pancreatico
Trasformare batteri amichevoli in combattenti contro il cancro
Il cancro del pancreas è uno dei tumori più letali, in parte perché si nasconde dietro difese potenti che spengono il sistema immunitario dell’organismo. Questo studio esplora un alleato inatteso nella lotta contro la malattia: un comune batterio “buono” del mondo caseario, reingegnerizzato per localizzarsi nei tumori pancreatici e aiutare il sistema immunitario ad attaccarli più efficacemente. Prendendo in prestito una proteina di superficie adesiva da un pericoloso streptococco, i ricercatori hanno trasformato un microbo innocuo in uno strumento mirato anti‑tumorale nei topi.
Un cancro difficile che inganna il sistema immunitario
L’adenocarcinoma duttale pancreatico è notoriamente letale: solo circa uno su otto pazienti è in vita cinque anni dopo la diagnosi. Una ragione principale è il suo microambiente tumorale: un involucro denso, simile a una cicatrice, ricco di cellule e molecole che attenuano gli attacchi immunitari e ostacolano molti farmaci. Tra i colpevoli ci sono le trappole extracellulari dei neutrofili, o NET—reti di DNA e proteine che i globuli bianchi lanciano nell’ambiente circostante. Nel cancro del pancreas queste reti viscide fanno più danno che beneficio: favoriscono la crescita tumorale, tengono lontane le cellule T citotossiche e sono associate a esiti peggiori. Disattivare le NET, risvegliando al contempo l’immunità anti‑tumorale, è diventata una strategia attraente.
Prendere in prestito una proteina adesiva, ma non il germe pericoloso
Precedenti lavori avevano dimostrato che una proteina di superficie dello Streptococcus di gruppo A, chiamata Scl1, può sia legarsi alle fibre associate ai tumori sia ridurre la formazione di NET, rallentando la crescita dei tumori pancreatici nei topi. Ma lo streptococco di gruppo A è anche il batterio responsabile della faringite streptococcica e di gravi infezioni invasive, il che lo rende inadatto come terapia vivente. Per mantenere la proteina utile evitando il germe dannoso, il team ha ingegnerizzato Lactococcus lactis—un probiotico ampiamente usato negli alimenti e considerato sicuro—per esporre Scl1 sulla sua superficie. Questo nuovo ceppo, denominato Lactococcus::620, è stato testato in topi portatori di tumori pancreatici, usando sia tumori sottocutanei semplici sia modelli più realistici con tumori che crescono direttamente nel pancreas.
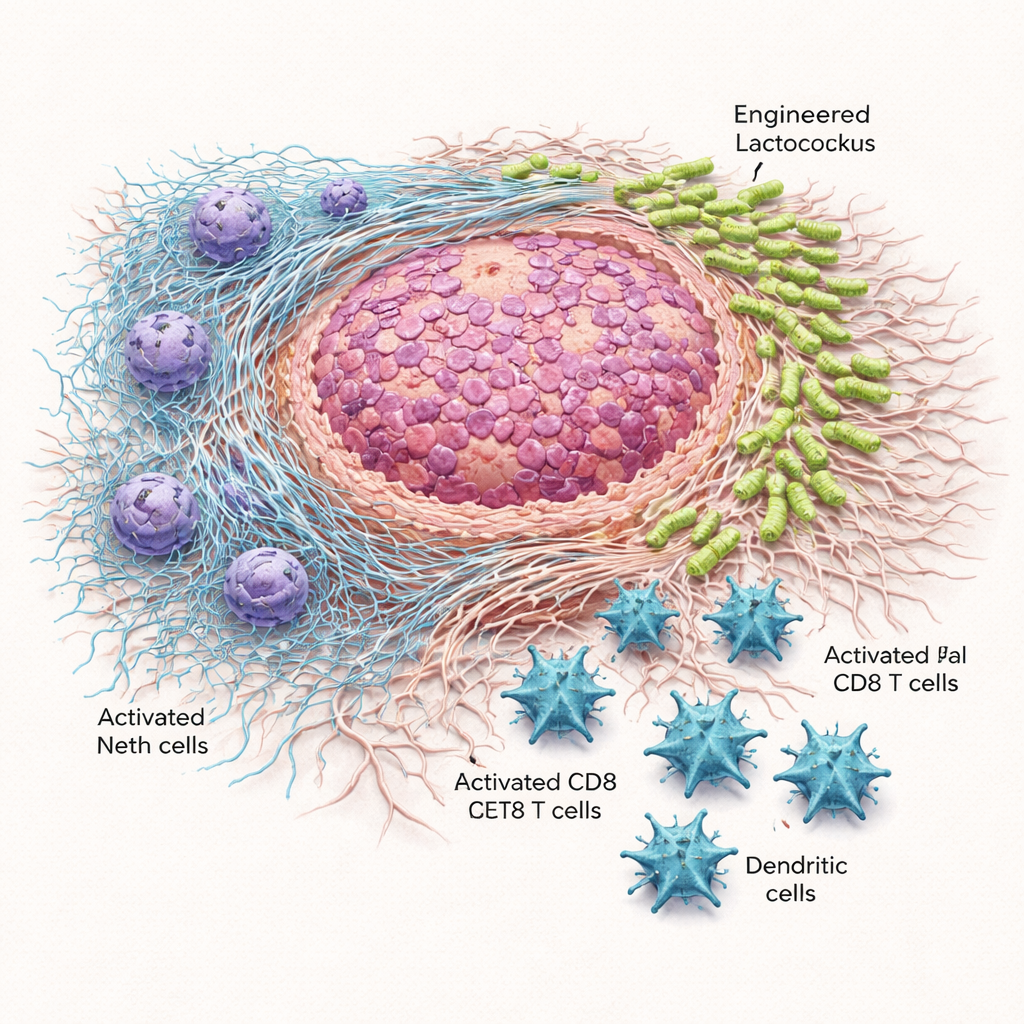
Batteri guidati riducono la crescita tumorale e allungano la sopravvivenza
Quando una singola dose del batterio ingegnerizzato è stata iniettata direttamente nei tumori sottocutanei o somministrata nella cavità addominale, i tumori crescevano più lentamente e pesavano meno rispetto ai topi trattati con Lactococcus ordinario o con un controllo salino. Nel modello pancreatico, più impegnativo, sono state necessarie dosi ripetute ogni tre giorni, ma i benefici sono stati marcati. Lactococcus::620 ha ridotto le dimensioni dei tumori, il loro peso e ha prolungato la sopravvivenza degli animali senza causare morti correlate al trattamento. Microscopia e colture dei tessuti tumorali hanno mostrato che i batteri portatori di Scl1 si accumulavano in modo affidabile nell’area tumorale, specialmente nella matrice fibrosa prodotta dai fibroblasti associati al cancro, risparmiando per lo più la milza. Al contrario, Lactococcus non modificato si diffondeva più ampiamente nell’organismo ed era talvolta tossico se somministrato in modo sistemico.
Disinnescare reti dannose e far entrare le cellule immunitarie
I batteri ingegnerizzati hanno anche rimodellato il paesaggio immunitario intorno ai tumori. I tumori dei topi trattati con Lactococcus::620 contenevano più cellule T CD8 “killer” e cellule dendritiche—attori chiave nel riconoscere e distruggere le cellule tumorali—e quelle cellule T mostravano meno marcatori di esaurimento e più molecole legate all’attività. Allo stesso tempo, sono diminuite le misure dell’attività delle NET. In test di laboratorio, i neutrofili esposti a Lactococcus::620 rilasciavano meno DNA libero e mostravano minore attività della mieloperossidasi, un enzima necessario alla formazione delle NET. Nei topi trattati, il DNA circolante associato alle NET risultava ridotto. Crucialmente, quando gli stessi esperimenti sono stati eseguiti in topi geneticamente incapaci di formare NET, i batteri ingegnerizzati non hanno più rallentato la crescita tumorale. Quella perdita di beneficio suggerisce fortemente che il blocco delle NET è centrale per il potere terapeutico della strategia.
Che cosa potrebbe significare per la cura futura del cancro
Complessivamente, i risultati delineano un nuovo concetto: usare un batterio sicuro, di grado alimentare, come veicolo programmabile per portare una proteina che blocca le NET e si dirige verso i tumori direttamente nell’ostile microambiente del cancro pancreatico. Nei topi, questo approccio ha ridotto il carico tumorale, migliorato la sopravvivenza e aperto la strada affinché le cellule immunitarie svolgessero meglio il loro compito. Pur restando molto lavoro prima che una simile strategia possa essere testata nell’uomo—compresi studi in modelli di malattia metastatica e combinazioni con immunoterapie moderne—lo studio dimostra che batteri “buoni” attentamente ingegnerizzati potrebbero un giorno contribuire a inclinare l’equilibrio contro uno dei nostri tumori più resistenti.
Citazione: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Parole chiave: cancro del pancreas, terapia probiotica, microambiente tumorale, modulazione immunitaria, trappole extracellulari dei neutrofili