Clear Sky Science · it
Diagnosi della malattia di Alzheimer con alta accuratezza tramite modellizzazione di vie di segnalazione con reti di Petri
Perché la rilevazione precoce delle malattie cerebrali ci riguarda tutti
La malattia di Alzheimer erode lentamente la memoria e l’indipendenza, spesso molto prima che compaiano sintomi evidenti. Gli strumenti diagnostici attuali, come le scansioni cerebrali e i test cognitivi, possono essere costosi, difficili da reperire e poco sensibili nelle fasi più precoci. Questo studio introduce un nuovo modo di leggere il “cablaggio” molecolare del corpo usando campioni di sangue o di cervello e un quadro matematico chiamato rete di Petri. L’obiettivo è semplice ma profondo: stabilire, con altissima accuratezza, se il modello di attività genica di una persona assomiglia di più a quello di un individuo sano o a quello di una persona con Alzheimer—idealmente abbastanza presto da poter modificare il corso della malattia.
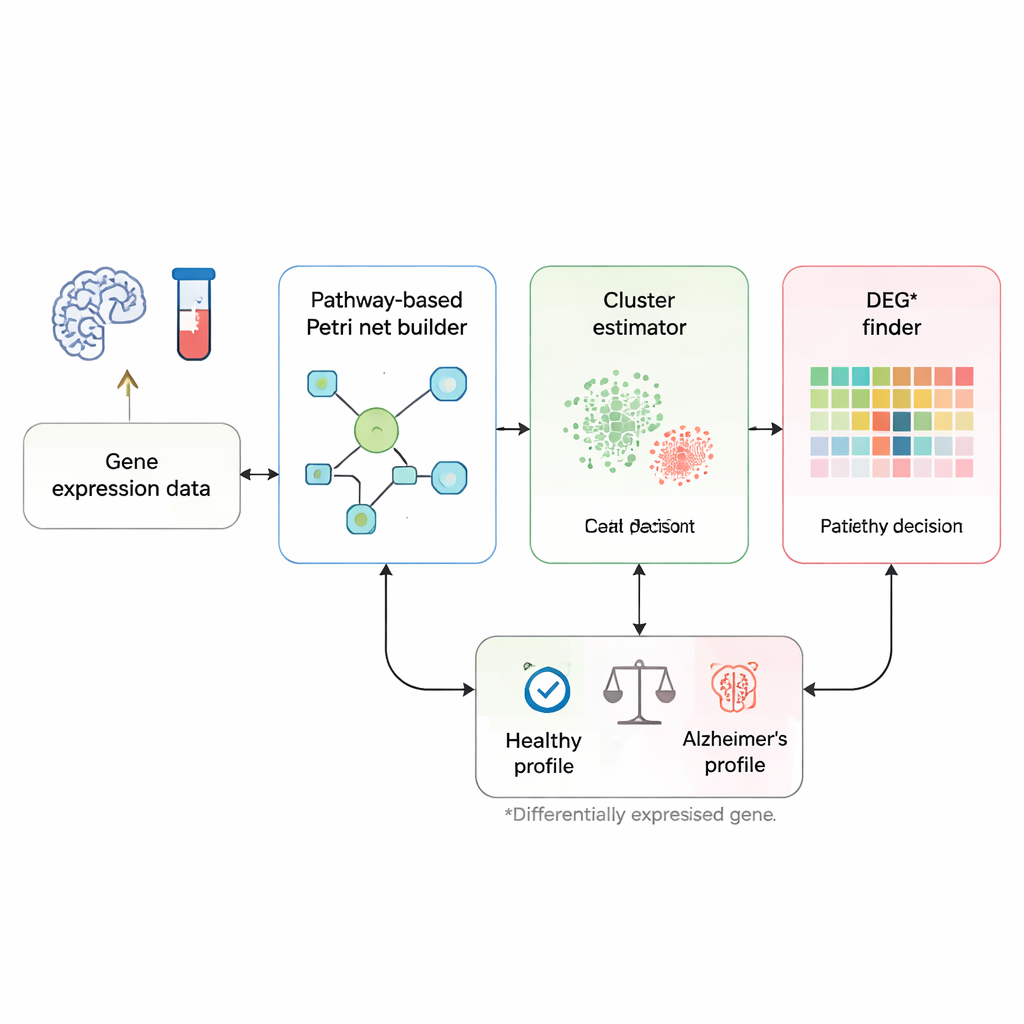
Leggere la malattia nei “circuiti” di segnalazione del corpo
Invece di considerare ogni gene come un marcatore isolato, i ricercatori si concentrano su come i geni comunicano tra loro lungo vie biologiche note associate all’Alzheimer. Partono da una mappa di vie curata dal database KEGG, che elenca i geni e le relazioni di attivazione o inibizione tra di essi. Questa via viene trasformata in una rete di Petri—una sorta di diagramma di flusso in cui i cerchi rappresentano i geni, i rettangoli le interazioni e piccoli gettoni i segnali che si muovono nella rete. Quando un gettone percorre la via fino a nodi “di malattia” speciali, rappresenta una catena di eventi genici che potrebbe condurre alla morte delle cellule cerebrali e alla demenza.
Da un campione di sangue a una risposta sì o no
Il metodo inizia con profili di espressione genica: misurazioni che indicano quanto siano attivi migliaia di geni nel sangue o nel tessuto cerebrale di una persona. Innanzitutto, un “stimatore di cluster” personalizzato confronta un nuovo campione con campioni etichettati precedentemente come sani o malati, concentrandosi sui geni già noti per differire tra questi gruppi. Per ciascun gene, lo strumento verifica quali campioni di training hanno livelli di espressione più simili e utilizza una sorta di voto di vicinato per dare al nuovo campione un’etichetta iniziale come verosimilmente sano o verosimilmente malato. Questo passaggio forma due gruppi di lavoro, o cluster: uno che rappresenta i pattern tipici dei sani e uno che rappresenta i pattern tipici dell’Alzheimer.
Trovare i geni più informativi per ogni persona
Segue una fase più personalizzata. Per un dato individuo, il metodo esamina gene per gene per vedere dove i suoi livelli di espressione emergono realmente. Per ciascun gene, confronta il valore della persona con l’intervallo osservato sia nel cluster sano sia in quello dei pazienti, usando statistiche robuste che attenuano l’influenza di outlier rumorosi. Se l’espressione di un gene ricade chiaramente nell’intervallo “malato” e al di fuori di quello sano, viene segnalato come DEG*, un gene particolarmente informativo per quell’individuo. Questi geni DEG* ricevono gettoni iniziali nella rete di Petri, segnando i punti in cui l’attività anormale appare per la prima volta nel circuito di segnalazione.
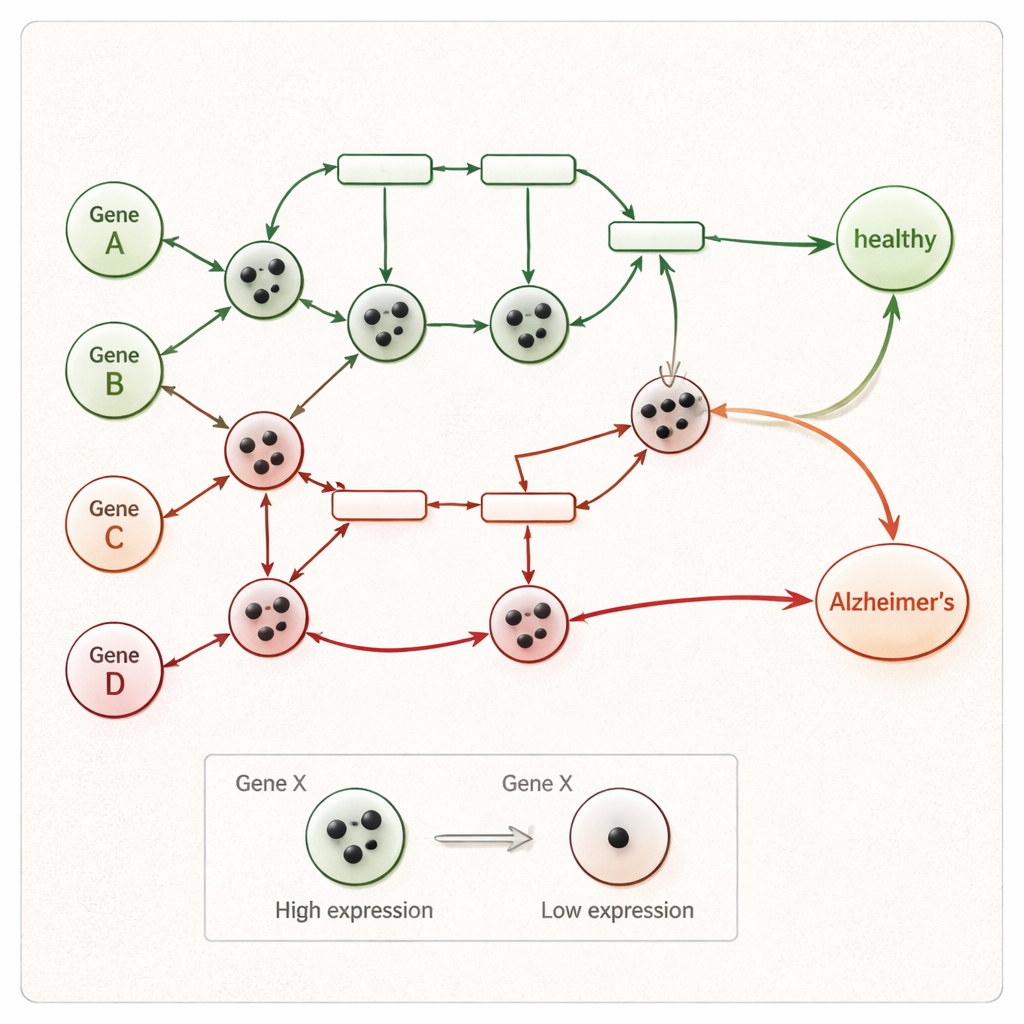
Lasciare che la rete si svolga fino alla diagnosi
Una volta posizionati i gettoni, la rete di Petri viene eseguita passo dopo passo. A ogni passo, ogni interazione i cui geni di input hanno un numero sufficiente di gettoni “scatta”, muovendo gettoni verso i geni a valle rispettando le regole di attivazione e inibizione. Questo continua finché non sono possibili ulteriori mosse. Se, al termine, almeno un gettone raggiunge il nodo finale di malattia della rete—che rappresenta processi come la morte neuronale o la neurodegenerazione—il campione viene classificato come Alzheimer; altrimenti viene etichettato come sano. Poiché ogni passo di scatto viene registrato, i ricercatori possono tracciare un percorso chiaro dall’attività genica anomala di una persona fino a un esito sano o malato, invece di basarsi su un punteggio statistico opaco.
Quanto è accurato questo approccio nella pratica?
Il team ha testato il proprio framework su diversi grandi dataset pubblici di espressione genica provenienti sia dal sangue sia dal tessuto cerebrale. In due dataset di sangue ampiamente utilizzati, il loro metodo ha distinto correttamente i pazienti con Alzheimer dagli individui sani in circa il 98–99% dei casi, molto oltre i precedenti approcci di machine learning che spesso raggiungevano solo il 65–81% di accuratezza. Hanno inoltre mostrato prestazioni solide su ulteriori dataset cerebrali e del sangue, anche quando il numero di campioni era ridotto. È importante notare che, a differenza di molti concorrenti, il loro metodo non scarta campioni rumorosi o difficili da interpretare; invece sfrutta il proprio disegno interno per gestire la variabilità mantenendo tutti i dati nell’analisi.
Cosa significa questo per i futuri test sull’Alzheimer
Per un non addetto ai lavori, il messaggio principale è che lo studio trasforma la genetica complessa e i diagrammi di vie in un processo decisionale chiaro e passo a passo in grado di leggere i segni precoci dell’Alzheimer da un campione semplice, potenzialmente anche solo dal sangue. Modellando come i geni anomali lavorano insieme, e non solo come si comportano singolarmente, il framework basato sulle reti di Petri offre sia un’elevata accuratezza diagnostica sia una “storia” comprensibile di come la malattia può svilupparsi in ciascun individuo. Sebbene questo lavoro sia ancora di ricerca e non ancora un test clinico, indica la strada verso strumenti futuri che potrebbero rilevare l’Alzheimer più precocemente, guidare le scelte terapeutiche e, in prospettiva, essere adattati ad altre malattie cerebrali e tumori usando la stessa idea di fondo.
Citazione: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Parole chiave: Diagnosi di Alzheimer, espressione genica, vie di segnalazione, modellizzazione con reti di Petri, biomarcatori del sangue