Clear Sky Science · it
Costruzione e validazione iniziale di una rete genica chiave per la resistenza al progesterone nel carcinoma endometriale basata su uno screening CRISPR a livello genomico
Perché alcuni tumori uterini smettono di “ascoltare” gli ormoni
Per molte persone con carcinoma endometriale precoce (della mucosa uterina) che desiderano ancora avere figli, compresse ormonali che imitano il progesterone naturale possono ridurre i tumori preservando l’utero. Tuttavia fino a un terzo di questi tumori non risponde mai o diventa rapidamente resistente, costringendo le pazienti a ricorrere alla chirurgia o a trattamenti più aggressivi. Questo studio utilizza uno strumento di editing genico potente per mappare quali geni fanno sì che le cellule del carcinoma endometriale ignorino il progesterone, indicando possibili test e farmaci futuri in grado di prolungare l’efficacia di questa terapia.
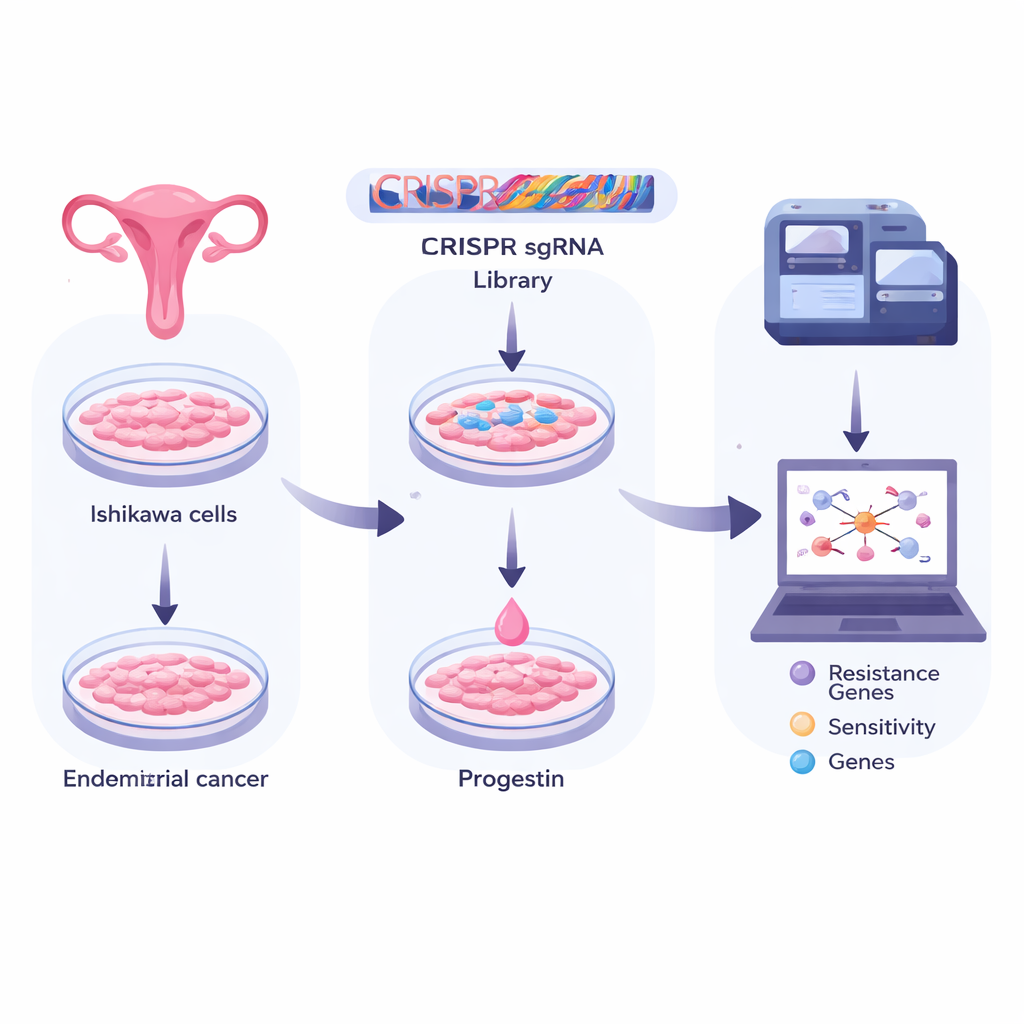
Usare le forbici geniche per esplorare l’intero genoma
I ricercatori hanno lavorato con cellule Ishikawa, un modello ampiamente utilizzato del carcinoma endometriale. Hanno infettato milioni di queste cellule con una libreria di CRISPR, ciascuna programmata per spegnere un diverso gene umano. In questo modo si è creata una vasta popolazione in cui, in principio, ogni cellula aveva un gene unico disattivato. Il gruppo ha poi diviso le cellule in più condizioni: una congelata come riferimento di base, una esposta solo a un solvente inerte e una trattata per molti giorni con un progesterone sintetico comune (medroxiprogesterone, o MPA). Mediante il sequenziamento profondo dei tag CRISPR sopravvissuti in ciascun gruppo, hanno potuto identificare quali knock-out genici aiutavano le cellule a sopravvivere o a morire durante il trattamento con progesterone.
Distinguere i geni che aiutano o ostacolano la risposta al farmaco
L’analisi di questo grande volume di dati ha richiesto statistiche sofisticate. Il team ha applicato due metodi complementari, RRA e MLE, per classificare i geni in base a quanto protegevano le cellule dal progesterone (geni di resistenza) o le rendevano più soggette a morire (geni di sensibilità). Hanno identificato centinaia di candidati in entrambe le direzioni. Molti di questi geni si raggruppavano in vie coinvolte nella copiatura e nella riparazione del DNA, nella sintesi e nel processamento dell’RNA e nel metabolismo cellulare generale. In altre parole, il macchinario di base che permette alle cellule di leggere, mantenere e agire sul proprio materiale genetico sembra strettamente collegato al fatto che le cellule del carcinoma endometriale obbediscano al segnale “smetti di crescere” del progesterone.
Restringere la lista ai protagonisti più importanti
Per evitare piste false, gli scienziati hanno confrontato i risultati del CRISPR con un dataset precedente del loro laboratorio, in cui avevano confrontato cellule tumorali ordinarie con una linea resa resistente al progesterone nel tempo. Cercando geni presenti in entrambi gli screening e con cambiamenti coerenti, hanno ridotto la lista a cinque geni che sembrano promuovere la resistenza e venti che sembrano contrastarla. Banche dati pubbliche sul cancro hanno mostrato che molti geni che bloccano la resistenza sono più attivi nel tipo più comune di carcinoma endometriale, mentre diversi geni promotori di resistenza correlano con esiti peggiori nei pazienti, suggerendo che questi segnali contano nei tumori reali, non solo nelle colture cellulari.
Testare i geni chiave nelle cellule e nei topi
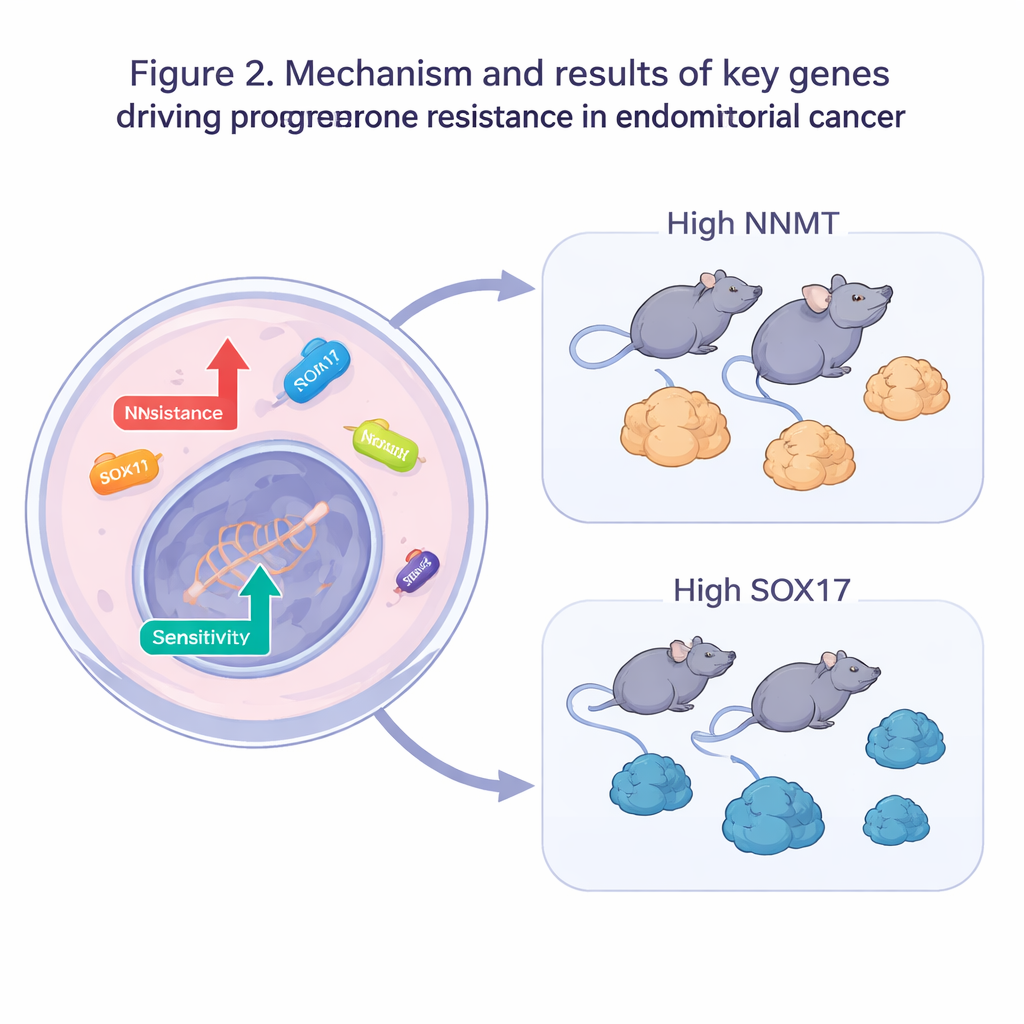
Il gruppo è poi passato dai big data agli esperimenti pratici. In cellule resistenti al progesterone hanno spento ciascuno dei cinque geni sospettati di promuovere la resistenza o hanno aumentato l’espressione dei cinque geni sospettati di sensibilizzare. Quando queste cellule modificate sono state esposte al progesterone, molte più sono morte e dosi di farmaco molto più basse sono state sufficienti a rallentarne la crescita, confermando che modulare singoli geni può ripristinare la sensibilità ormonale. Due geni si sono distinti: NNMT, coinvolto nel metabolismo cellulare, e SOX17, un gene che contribuisce a regolare lo sviluppo e il comportamento cellulare. Nei modelli murini tumorali, l’aumento di NNMT ha reso i tumori meno sensibili al progesterone, mentre l’incremento di SOX17 ha reso tumori resistenti più inclini a ridursi con lo stesso trattamento.
Cosa potrebbero significare questi risultati per le pazienti
In parole semplici, lo studio costruisce un primo “diagramma elettrico” di come le cellule del carcinoma endometriale decidano se rispondere o meno al progesterone. Suggerisce che la resistenza non dipende solo dalla perdita del recettore del progesterone, ma anche da cambiamenti più profondi nella gestione del DNA e dell’RNA e in geni di controllo chiave come NNMT e SOX17. In futuro, test su sangue o tessuto che leggano questa rete genica potrebbero aiutare i medici a predire chi trarrà beneficio dalla terapia ormonale conservativa della fertilità. Ancora più promettente, farmaci che inibiscano i geni di resistenza o che potenzino i geni di sensibilità potrebbero un giorno essere combinati con il progesterone per mantenere efficace questa opzione terapeutica più delicata per un maggior numero di persone e per periodi più lunghi.
Citazione: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
Parole chiave: carcinoma endometriale, resistenza al progesterone, screening CRISPR, reti geniche, terapia ormonale