Clear Sky Science · it
Le modifiche m6A dell’ospite modellano il microbiota che induce ferroptosi specifica per cellula come via causale alle malattie respiratorie croniche
Perché i tuoi microbi contano per i polmoni
I problemi respiratori cronici come l’asma e la broncopneumopatia cronica ostruttiva (BPCO) vengono di solito attribuiti al fumo, all’inquinamento o alle allergie. Questo studio suggerisce un altro attore, meno ovvio: i trilioni di microbi che vivono nel nostro intestino e sulla pelle. Utilizzando grandi dataset genetici, gli autori mostrano che certi microbi potrebbero non solo accompagnare le malattie polmonari, ma contribuirne alla causazione—agendo tramite sottili modifiche chimiche nelle nostre cellule e una forma di danno cellulare guidata dal ferro. Comprendere questa rete nascosta potrebbe alla fine portare a nuovi modi di prevenire o trattare le malattie respiratorie croniche, orientando i nostri microbi e le loro vie molecolari verso stati più sani.
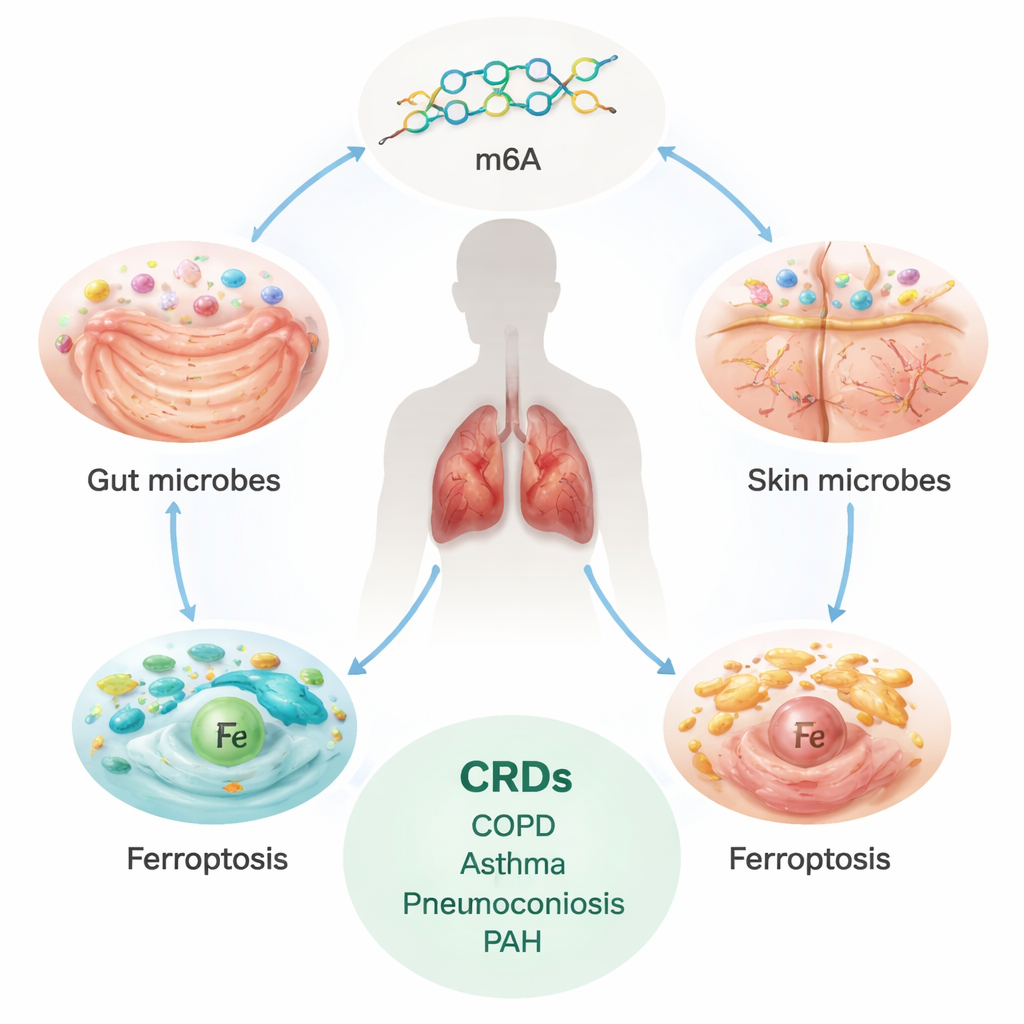
L’onere nascosto delle malattie polmonari croniche
Le malattie respiratorie croniche, tra cui BPCO, asma, malattie polmonari interstiziali (ILD), pneumoconiosi e ipertensione arteriosa polmonare (PAH), colpiscono centinaia di milioni di persone nel mondo e causano milioni di decessi ogni anno. Queste condizioni spesso progrediscono in modo lento ma inesorabile, cicatrizzando o rimodellando polmoni e vasi sanguigni e lasciando le persone affette da dispnea. I trattamenti attuali gestiscono principalmente i sintomi; non arrestano né reversano completamente il danno di base. Questo ha spinto i ricercatori a cercare cause più profonde, a livello elementare, specialmente quelle che potrebbero essere modificate prima che si sviluppi una malattia grave.
Vicini microbici nell’intestino e sulla pelle
Ora sappiamo che intestino e pelle ospitano comunità microbiche complesse che aiutano a educare il sistema immunitario, modellare il metabolismo e mantenere le difese di barriera. Ma questi microbi guidano davvero le malattie polmonari, o semplicemente cambiano quando le persone si ammalano? Per districare causa ed effetto, i ricercatori hanno utilizzato un metodo chiamato randomizzazione mendeliana, che sfrutta differenze genetiche naturali tra individui come una sorta di “esperimento” lifelong. Hanno combinato dati genetici su centinaia di tipi microbici intestinali e cutanei con dati su cinque grandi malattie polmonari croniche provenienti da studi europei di ampia scala, testando se tendenze ereditate verso livelli più alti o più bassi di specifici microbi sono legate al rischio di ciascuna malattia.
Microbi che aiutano o danneggiano i polmoni
L’analisi ha identificato dozzine di microbi intestinali che aumentavano o diminuivano il rischio di ciascuna malattia respiratoria, spesso con schemi specifici per patologia. Per esempio, alcuni batteri intestinali sembravano proteggere da BPCO, asma o PAH, mentre altri aumentavano le probabilità di ILD o BPCO. I microbi cutanei hanno mostrato associazioni più modeste ma ancora rilevabili, con alcune specie correlate a rischio maggiore e altre a rischio minore nelle diverse condizioni. Il gruppo ha anche invertito la direzione dell’analisi, trovando che il rischio genetico per BPCO, asma e altre malattie polmonari prevedeva a sua volta cambiamenti nel microbiota intestinale e cutaneo. Questo traffico bidirezionale suggerisce un circuito di retroazione: i microbi possono contribuire a modellare la malattia polmonare e la malattia polmonare può rimodellare i nostri ecosistemi microbici.
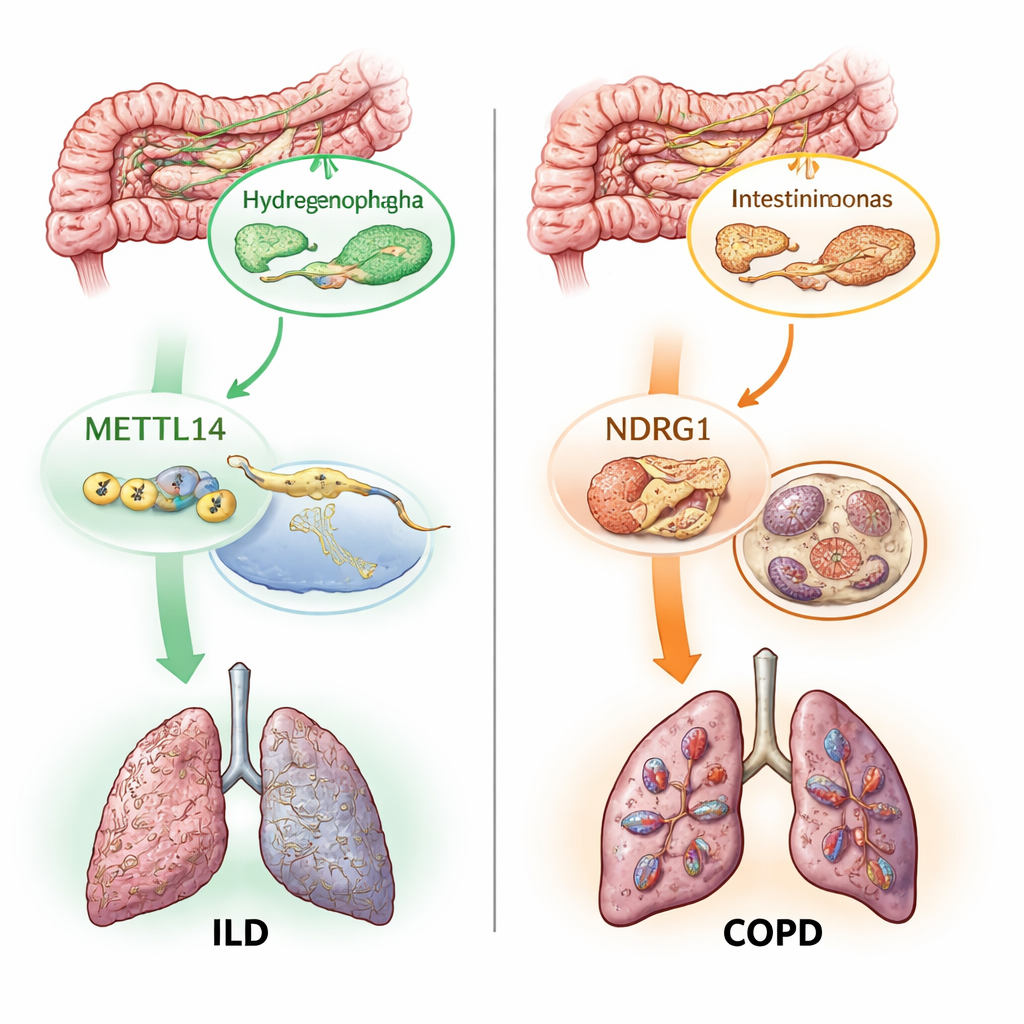
Due interruttori molecolari: marche sull’RNA e morte cellulare indotta dal ferro
Oltre a mappare quali microbi sono rilevanti, gli autori hanno indagato come questi partner microscopici potrebbero influenzare i tessuti polmonari. Si sono focalizzati su due processi molecolari già sospettati nel danno polmonare. Il primo, chiamato modificazione m6A, è un piccolo marcatore chimico aggiunto all’RNA che regola come i geni vengono attivati o disattivati. Il secondo, la ferroptosi, è una forma di morte cellulare dipendente dal ferro guidata da un’ossidazione incontrollata dei lipidi nelle membrane cellulari. Utilizzando proxy genetici per 19 geni correlati a m6A e centinaia di geni legati alla ferroptosi, hanno testato se cambiamenti in queste vie sono causalmente connessi alle malattie polmonari. Hanno trovato che un gene “writer” m6A, METTL14, era collegato a un rischio ridotto di ILD, e diversi geni della ferroptosi, incluso NDRG1, erano associati a un rischio aumentato di BPCO, ILD e asma.
Collegare i punti: dai microbi alle cellule alla malattia
La parte più innovativa del lavoro è stata tracciare come questi pezzi si inseriscono in catene di causa ed effetto. Analisi di mediazione statistiche hanno suggerito che parte dell’effetto protettivo di METTL14 sull’ILD passa attraverso cambiamenti che induce in un particolare microbo intestinale chiamato Hydrogenophaga. In un’altra via, un batterio intestinale specifico, Intestinimonas massiliensis, sembrava influenzare il rischio di BPCO in parte attivando NDRG1 e il programma di morte per ferroptosi. Il gruppo ha quindi verificato i dati di tessuto polmonare umano e ha confermato che sia METTL14 sia NDRG1 vengono espressi in modo diverso nei campioni malati rispetto a quelli sani. Infine, usando mappe genetiche a singola cellula delle cellule immunitarie, hanno localizzato l’effetto dannoso di NDRG1 sulla BPCO a un sottogruppo di cellule immunitarie, un tipo di monociti, suggerendo che farmaci futuri mirati a questo gene potrebbero dover agire in modo specifico per cellula.
Cosa significa per i trattamenti futuri
Per i non specialisti, il messaggio chiave è che la salute polmonare non riguarda solo ciò che respiriamo, ma anche i microbi che vivono dentro e su di noi e gli interruttori molecolari che attivano all’interno delle nostre cellule. Questo studio non può dimostrare sperimentalmente ogni passaggio, ed è limitato principalmente a persone di ascendenza europea, ma offre forti indizi genetici che microbi intestinali, marche sull’RNA come m6A e la morte cellulare indotta dal ferro formano una via connessa che porta al danno polmonare cronico. Sul lungo periodo, questa linea di ricerca potrebbe ispirare nuove strategie che combinano terapie basate sul microbioma con farmaci mirati a METTL14, NDRG1 o alla ferroptosi, con l’obiettivo non solo di alleviare i sintomi ma di interrompere i circuiti biologici che fanno progredire le malattie respiratorie croniche.
Citazione: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Parole chiave: microbioma intestinale, malattia polmonare cronica, asma e BPCO, epigenetica dell'RNA, vie di morte cellulare