Clear Sky Science · it
Analisi integrative del trascrittoma del cancro metastatico rivelano Stati cellulari ed ecosistemi clinicamente distinti
Perché il quartiere intorno ai tumori conta
La maggior parte delle persone sa che il cancro può diffondersi, o metastatizzare, in organi distanti—e che questa diffusione provoca la maggior parte dei decessi per cancro. Tuttavia pochi realizzano che ogni tumore metastatico somiglia più a una città vivace che a un semplice agglomerato di cellule cancerose. Contiene molti tipi di cellule, normali e tumorali, che interagiscono, competono e cooperano in modi che possono rallentare la malattia o favorirne la crescita. Questo studio mappa quei “quartieri” nascosti in migliaia di tumori metastatici, fornendo indizi sul perché alcuni pazienti vivono più a lungo e rispondono meglio alle cure rispetto ad altri.
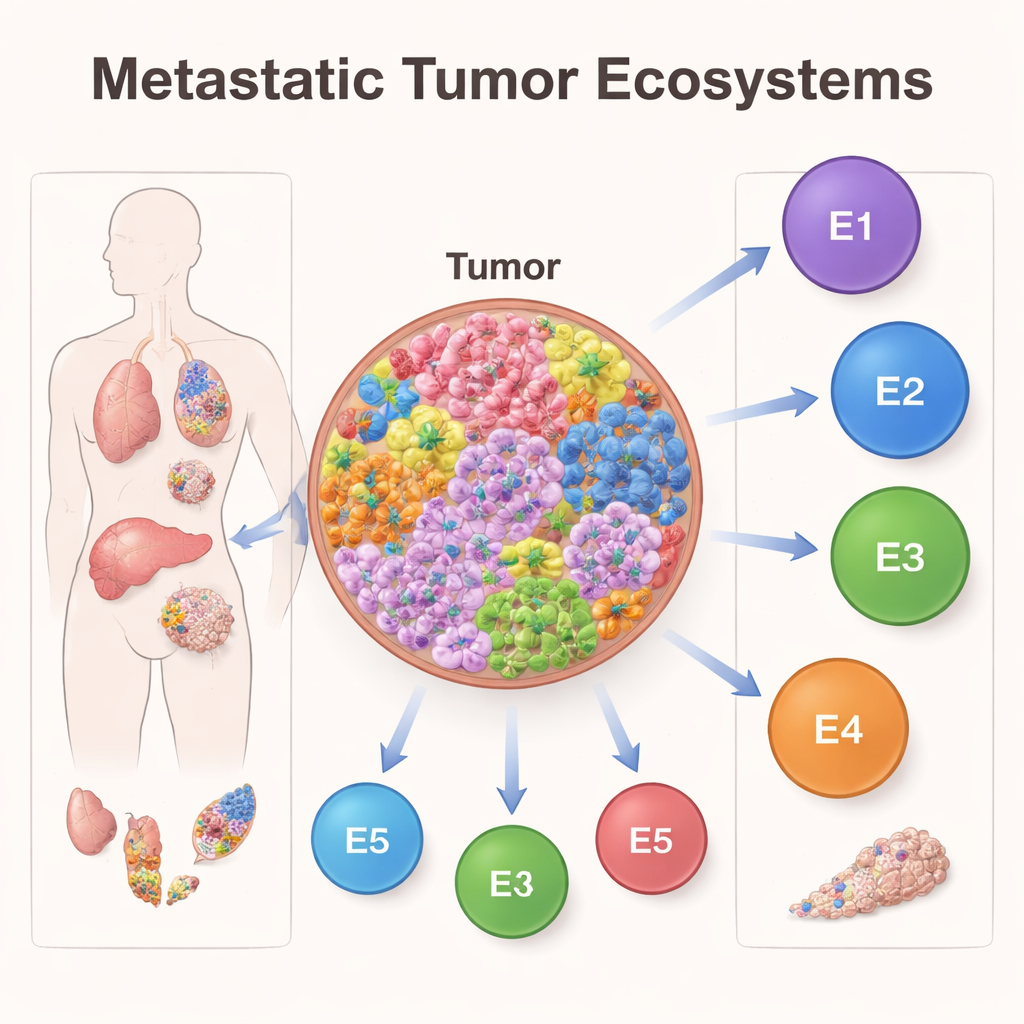
Uno sguardo all’interno di migliaia di tumori metastatici
I ricercatori hanno analizzato dati di attività genica provenienti da 2.822 pazienti con cancro metastatico in 25 tipi di tumore, tra cui tumori della prostata, della pelle e del seno. Invece di esaminare singole cellule al microscopio, hanno usato strumenti computazionali avanzati per “separare” i dati da tessuto bulk, stimando quali tipi cellulari erano presenti e quanto fossero attivi i loro geni. Con un framework di machine learning chiamato EcoTyper, hanno raggruppato le cellule in schemi ricorrenti di attività genica, che chiamano stati cellulari, e poi hanno esaminato come questi stati si organizzano in ecosistemi più ampi all’interno dei tumori.
Molti tipi di cellule, molte personalità
Nei tumori metastatici il team si è concentrato su 12 grandi classi cellulari, come cellule epiteliali tumorali, cellule immunitarie (inclusi linfociti T, linfociti B e cellule natural killer), cellule dei vasi sanguigni e fibroblasti che modellano l’impalcatura tissutale. Tra queste 12 classi hanno identificato 45 stati cellulari distinti—essenzialmente “modalità di personalità” che le cellule possono assumere. Per esempio, alcuni stati dei linfociti T erano orientati all’attacco, mentre altri sembravano esausti e meno capaci di combattere il cancro. Alcuni stati dei fibroblasti erano collegati al rimodellamento del tessuto in modi che possono favorire la diffusione tumorale. Questi stati non comparivano a caso: le loro frequenze variavano a seconda del tipo di tumore di origine e dell’organo in cui si era sviluppata la metastasi, rivelando una forte influenza sia dell’origine tumorale sia dell’ambiente locale.
Cinque ecosistemi tumorali legati alla sopravvivenza
Quando i ricercatori hanno esaminato quali stati cellulari tendevano a comparire insieme, hanno scoperto cinque ecosistemi principali, o “ecotipi”, all’interno dei tumori metastatici. Ogni ecotipo era una combinazione caratteristica di tipi e stati cellulari. Alcuni erano ricchi di cellule immunitarie e stromali, mentre altri erano dominati dalle cellule maligne. Questi ecotipi non erano semplici categorie accademiche: erano strettamente correlati alla durata della sopravvivenza dei pazienti. Un ecotipo, etichettato E5, era associato a esiti relativamente favorevoli, mentre altri, in particolare E2 ed E3, erano legati a una sopravvivenza peggiore. Gli stessi schemi di ecotipo ricorrevano in diversi tumori e organi, suggerendo che catturano regole generali di organizzazione dei tumori metastatici.
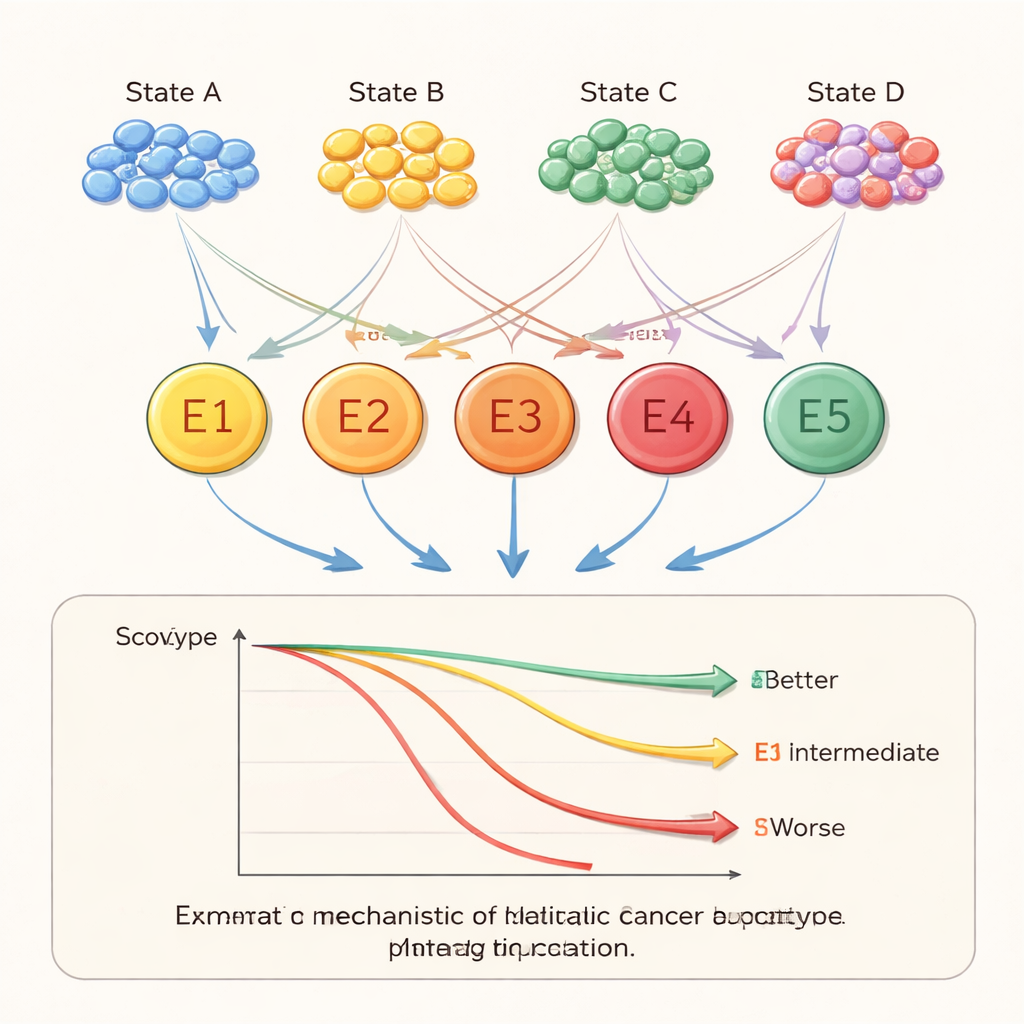
Attività immunitaria, risposta alle terapie e interruttori di controllo
Per capire cosa fanno questi ecosistemi, il gruppo ha analizzato quali vie biologiche erano attive nei loro programmi genici. Molti stati cellulari risultavano arricchiti in funzioni immunitarie o in vie classiche del cancro, come risposte a ipossia o segnali che guidano la divisione e l’invasione cellulare. Un ecotipo (E1) mostrava forte attività immunitaria e infiammatoria e alti livelli di cellule immunitarie e stromali, mentre un altro (E2) era arricchito in vie di crescita e del ciclo cellulare associate a malattia aggressiva. I ricercatori hanno anche esaminato marcatori rilevanti per le immunoterapie moderne. Alcuni ecotipi avevano caratteristiche che suggerivano una possibile elusione dell’attacco immunitario e una scarsa risposta ai farmaci che bloccano i checkpoint, mentre altri sembravano più propensi a beneficiarne. Infine, scansionando i fattori di trascrizione—interruttori principali che controllano programmi genici—hanno evidenziato diversi candidati, tra cui SPIB, SRF e NR1D1, che sembrano contribuire a plasmare questi ecosistemi e risultavano a loro volta associati alla prognosi dei pazienti.
Cosa significa per i pazienti
Per un lettore non specialista, il messaggio chiave è che i tumori metastatici non sono tutti uguali, anche quando condividono la stessa diagnosi. Sono costruiti da combinazioni ricorrenti di “personalità” cellulari ed ecosistemi che possono frenare o accelerare la malattia, e questi schemi lasciano tracce rilevabili nei dati di attività genica. Cartografando 45 stati cellulari e cinque principali ecosistemi tumorali in migliaia di pazienti, questo lavoro offre un atlante ad alta risoluzione del microambiente dei tumori metastatici. In futuro, tali mappe potrebbero aiutare i medici a prevedere quali pazienti sono a maggior rischio, chi è più probabile che tragga beneficio da trattamenti specifici—soprattutto dalle immunoterapie—e quali interruttori cellulari potrebbero essere i bersagli più promettenti per nuovi farmaci.
Citazione: Zhang, C., Li, S., Yu, Y. et al. Integrative analyses of metastatic cancer transcriptome reveal clinically distinct cellular States and ecosystems. Sci Rep 16, 7343 (2026). https://doi.org/10.1038/s41598-026-36512-3
Parole chiave: cancro metastatico, microambiente tumorale, stati cellulari, ecosistema immunitario, oncologia di precisione