Clear Sky Science · it
La fosforilazione di cortactina da parte di NEK7 modula la capacità migratoria delle cellule che esprimono EML4-ALK V3
Perché il movimento cellulare è importante nel cancro ai polmoni
Il cancro diventa pericoloso quando le cellule imparano a spostarsi. Nel carcinoma polmonare non a piccole cellule, alcuni tumori si diffondono nel corpo più rapidamente di altri, e uno dei responsabili è una proteina di fusione difettosa chiamata EML4-ALK. Una versione particolare, nota come variante 3 (V3), è associata a una malattia particolarmente aggressiva e a scarse risposte ai farmaci mirati. Questo studio pone una domanda di base ma cruciale: cosa permette a queste cellule tumorali guidate da V3 di cambiare forma e muoversi con tanta efficienza, e possiamo identificare le parti molecolari che rendono possibile questo comportamento?
Una variante polmonare iper-migratoria
I medici sanno da tempo che solo una minoranza dei tumori polmonari presenta la fusione EML4-ALK, ma i pazienti i cui tumori esprimono la forma V3 tendono ad avere esiti peggiori rispetto a quelli con altre varianti. Al microscopio, le cellule che esprimono V3 appaiono diverse: invece di essere compatte e a scacchiera, si allungano in forme sottili con protrusioni estese, simili a cellule in movimento. Lavori precedenti hanno mostrato che questo comportamento dipende da due enzimi, NEK9 e NEK7, che agiscono come interruttori molecolari nelle cellule. Tuttavia, i bersagli a valle cruciali di questi interruttori—quelli che rimodellano direttamente lo scheletro interno della cellula—non erano ben compresi.
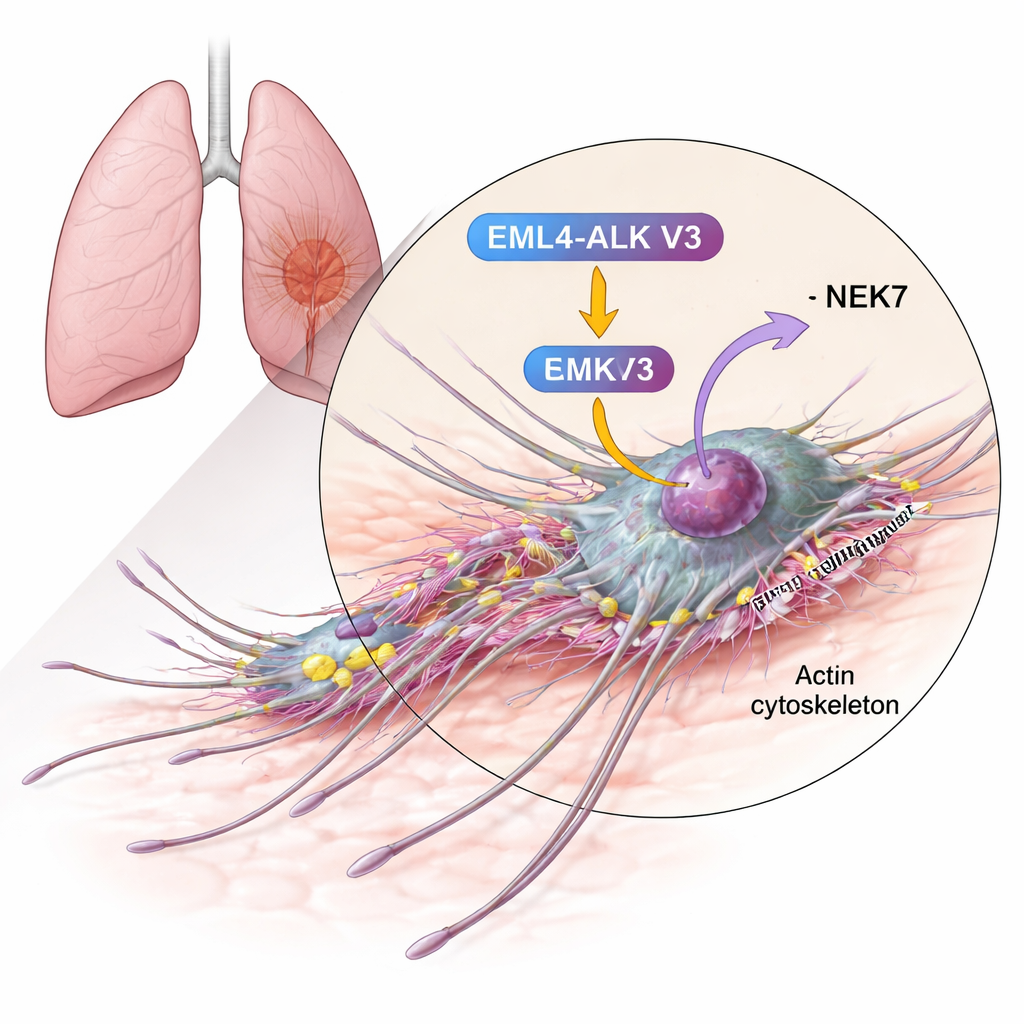
Collegare una proteina del movimento a una fusione aggressiva
Gli autori si sono concentrati sulla cortactina, una proteina già nota per essere abbondante in molti tumori invasivi e per favorire la costruzione delle reti di filamenti di actina che spingono la membrana cellulare in avanti. Attraverso test biochimici, hanno mostrato che la cortactina può essere modificata chimicamente (fosforilata) da NEK6 e, ancor più intensamente, da NEK7. Gli enzimi aggiungono gruppi fosfato a residui di serina specifici all’interno della regione di legame all’actina della cortactina—proprio quel tratto che afferra le fibre di actina e stabilizza le reti ramificate. Quando NEK7 era presente, la cortactina presentava più gruppi fosfato e in più siti rispetto a NEK6, suggerendo che NEK7 sia il regolatore primario in questo contesto.
Spegnere la cortactina arresta la migrazione delle cellule tumorali
Per verificare cosa fa effettivamente la cortactina nelle cellule viventi, i ricercatori l’hanno depletata tramite interferenza a RNA in cellule ingegnerizzate per attivare NEK9 o NEK7, o per esprimere la stessa EML4-ALK V3. In tutti e tre gli assetti, le marcate forme allungate e di tipo mesenchimale crollavano: le cellule diventavano più piatte e tondeggianti, perdevano le lunghe protrusioni e invece formavano spesse e dritte “fibre di stress” di actina che attraversavano la cellula. Molti saggi di migrazione—dal richiudere ferite artificiali in un foglio cellulare al tracciamento di singole cellule e alla misurazione del movimento verso un segnale chimico—hanno mostrato che in assenza di cortactina queste cellule altamente mobili rallentavano drasticamente. Effetti simili sono stati osservati in linee cellulari di carcinoma polmonare stabilite che portano naturalmente EML4-ALK V3, sottolineando la rilevanza clinica della via.
Sottili filamenti e punte affilate all’avanguardia
L’imaging ad alta risoluzione in cellule epiteliali bronchiali ha rivelato un quadro ancora più dettagliato. Le cellule che esprimevano EML4-ALK V3 producevano molte sottili estensioni simili a filopodi, a volte ramificate, che costellavano le loro protrusioni. Alle punte e ai punti di ramificazione di queste strutture, si raggruppavano cortactina, EML4-ALK V3, NEK7 e una forma fosforilata della cortactina. Questa stretta colocalizzazione suggerisce un “cantiere” focalizzato in cui NEK7 modifica la cortactina per costruire e mantenere le reti delicate e ramificate di actina che aiutano a guidare la cellula. Quando la cortactina veniva rimossa, queste estensioni intricate scomparivano e la crescita invasiva da sfere tumorali tridimensionali in un gel circostante era fortemente ridotta.
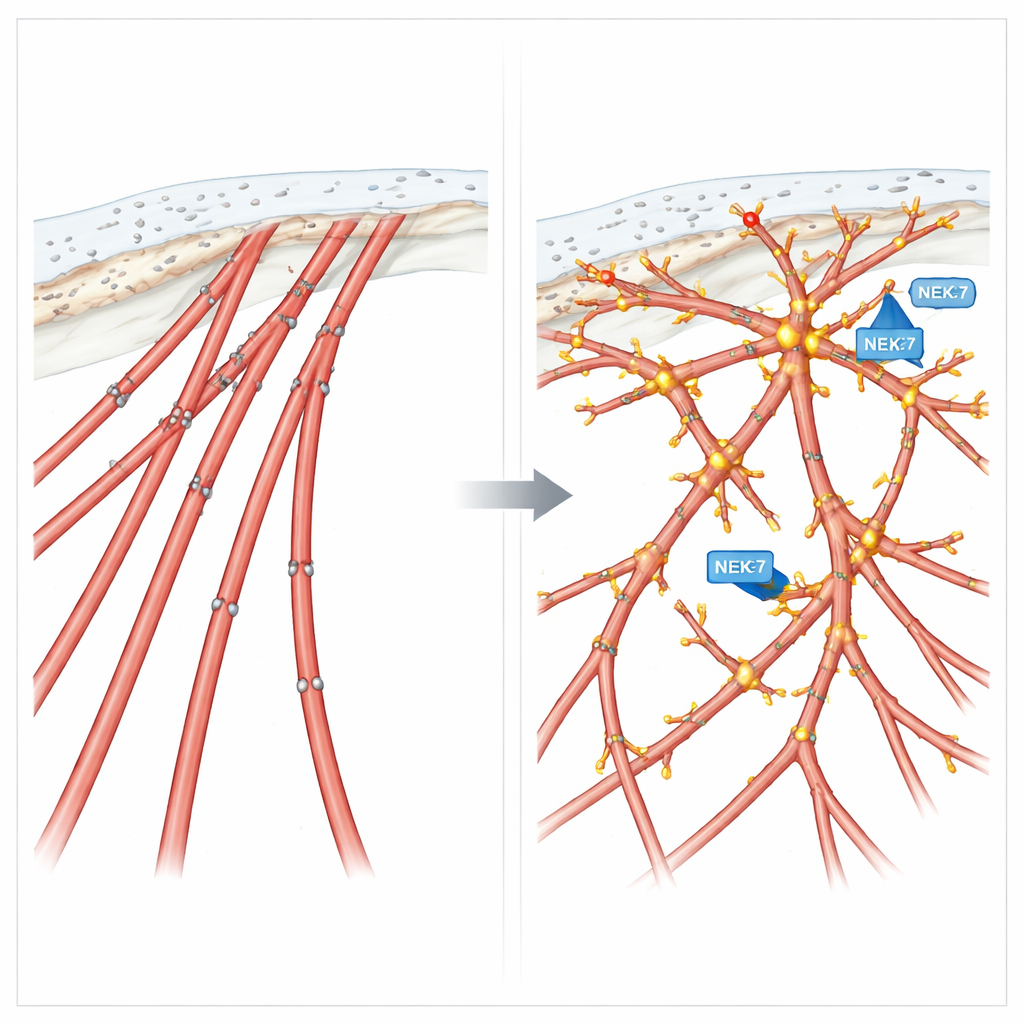
La fosforilazione come manopola della migrazione
Per testare come questi tag chimici sulla cortactina influenzino il comportamento, il gruppo ha creato due versioni ingegnerizzate della proteina: una forma fosfo-mimetica che imita una fosforilazione costante in quattro siti chiave, e una forma fosfo-null che non può essere fosforilata in quei punti. Le cellule che esprimevano la versione mimetica sviluppavano numerose estensioni simili a filopodi e mostravano una migrazione direzionata potenziata, simile a quella delle cellule con NEK7 o EML4-ALK V3 attivi. Al contrario, le cellule che esprimevano la versione non fosforilabile formavano fibre di stress rigide, perdevano quelle sottili estensioni e si muovevano in modo rapido ma senza scopo—buone a vagare, scarse nel seguire un segnale. Nelle colture tridimensionali, questa cortactina fosfo-null promuoveva escrescenze invasive disorganizzate piuttosto che guidate in modo preciso.
Cosa significa per comprendere—e mirare—a diffusione
In parole semplici, lo studio mostra che la variante aggressiva di carcinoma polmonare EML4-ALK V3 dirotta un normale sistema che modella la cellula. Attivando NEK7, provoca la fosforilazione della cortactina in siti specifici all’interno della sua regione di legame all’actina. Questa modifica accorda la cortactina in modo che possa costruire strutture di actina finemente ramificate ed estensioni simili a filopodi che supportano una migrazione e invasione cellulare rapide e dirette. Interrompere la cortactina o la sua fosforilazione capovolge il sistema: le cellule o si muovono a malapena o si muovono in modo caotico e senza direzione. Queste intuizioni rivelano una catena molecolare concreta—da una fusione che guida il cancro, attraverso NEK7, fino alla cortactina e al citoscheletro di actina—that aiuta a spiegare perché alcuni tumori polmonari metastatizzano così efficacemente, e indicano nuove strategie per rallentare o sviare il loro movimento.
Citazione: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Parole chiave: carcinoma polmonare non a piccole cellule, EML4-ALK V3, migrazione cellulare, cortactina, cito scheletro di actina