Clear Sky Science · it
ATF4 regola la disfunzione mitocondriale e la mitofagia, contribuendo all'apoptosi delle cellule endoteliali corneali
Perché la finestra dell'occhio può diventare offuscata
Le nostre cornee—le chiare “finestre” anteriori degli occhi—restano trasparenti grazie a un sottile e operoso strato di cellule sulla loro superficie interna. Nella distrofia endoteliale corneale di Fuchs (FECD), milioni di persone perdono lentamente queste cellule, con conseguente edema, visione offuscata e spesso la necessità di trapianti di cornea. Questo studio indaga una domanda fondamentale ma cruciale: cosa induce queste cellule a morire, e spegnere un singolo “interruttore” molecolare potrebbe aiutarle a sopravvivere?
Uno strato cellulare fragile che mantiene la visione chiara
L'endotelio corneale è un singolo foglio di cellule esagonali che pompa costantemente il fluido fuori dalla cornea per mantenerla trasparente. Nella FECD queste cellule subiscono stress e scompaiono gradualmente, mentre sullo strato di membrana sottostante si accumulano dei rigonfiamenti di materiale anomalo, chiamati guttae. Poiché non esistono farmaci approvati per la FECD e il trattamento principale resta il trapianto di cornea, i ricercatori stanno cercando di capire esattamente come lo stress intracellulare spinga queste cellule verso la morte. Lavori precedenti avevano indicato separatamente tensioni in due compartimenti chiave della cellula—il reticolo endoplasmatico (la fabbrica del ripiegamento delle proteine) e i mitocondri (le centrali energetiche cellulari)—ma non era chiaro come queste due risposte allo stress comunicassero tra loro.
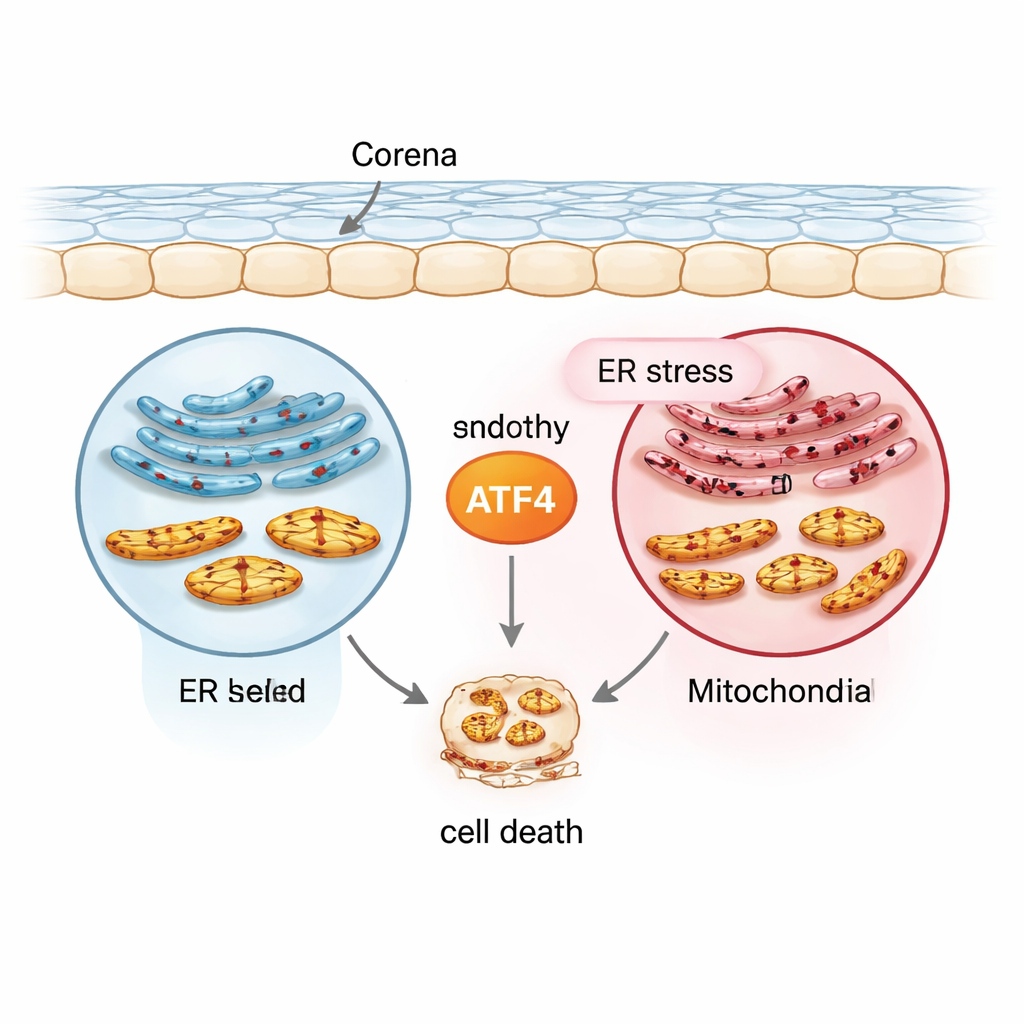
Il messaggero dello stress al centro: ATF4
Il gruppo si è concentrato su una proteina chiamata ATF4, un fattore di trascrizione che accende o spegne molti geni della risposta allo stress. Utilizzando una linea cellulare endoteliale corneale umana normale (21T), una linea simile alla FECD con l'espansione del ripetuto TCF4 collegata alla malattia (F35T), cellule endoteliali corneali umane primarie e modelli murini esposti alla luce UVA, hanno creato una serie di condizioni che imitano lo stress cronico. Hanno indotto lo stress del reticolo endoplasmatico con un farmaco chiamato tunicamycina e quindi misurato ATF4 e altri marcatori. Rispetto alle cellule normali, le cellule simili alla FECD mostravano livelli inizialmente più alti di ATF4 e di proteine dello stress correlate, e ATF4 aumentava ulteriormente sotto stress cronico sia nelle colture cellulari sia nei tessuti corneali umani. Questo schema colloca ATF4 al crocevia tra risposte protettive precoci e segnali autodistruttivi successivi.
Dalla perdita di energia alla morte programmata
Successivamente i ricercatori hanno esaminato come questo stress influenzasse i mitocondri. Nelle cellule simili alla FECD i mitocondri producevano meno ATP, perdevano il potenziale elettrico della membrana e si frammentavano passando da forme lunghe e reticolari a numerosi piccoli frammenti. Questi cambiamenti peggioravano quando lo stress del reticolo endoplasmatico si protraeva. Allo stesso tempo, proteine classiche della morte cellulare—come caspasi attivate e la proteina di riparazione del DNA PARP nella sua forma clivata pro‑morte—diventavano più abbondanti, mentre proteine protettive come Bcl‑2 diminuivano. Nel complesso, queste modificazioni indicano che le cellule endoteliali corneali stressate nella FECD sono spinte verso un'apoptosi guidata dai mitocondri, una forma ordinata ma irreversibile di suicidio cellulare programmato.
Il sistema di pulizia si inceppa sotto stress cronico
Normalmente, i mitocondri gravemente danneggiati vengono rimossi tramite un processo di riciclo chiamato mitofagia, in cui vengono etichettati e racchiusi in piccoli sacchi per lo smaltimento. Il team ha scoperto che le molecole “innescanti” della mitofagia (Parkin e LC3) venivano attivate sia nelle cellule normali sia in quelle simili alla FECD, soprattutto dopo lo stress. Tuttavia, proteine di supporto chiave risultavano ridotte e la microscopia elettronica mostrava un accumulo di mitocondri parzialmente digeriti intrappolati in vescicole. Questo suggerisce che, sebbene il processo di pulizia si avviasse, non riuscisse a completarsi, lasciando le cellule ingombre di centrali difettose che alimentano ulteriormente lo stress e la morte anziché il recupero.
Spegnere ATF4 per salvare le cellule
Per verificare se ATF4 guidasse questa spirale, i ricercatori hanno usato RNA interferente per silenziare parzialmente ATF4 in cellule endoteliali corneali coltivate. Sotto lo stesso stress cronico, le cellule con ATF4 ridotto mostravano livelli inferiori di proteine pro‑morte, un potenziale di membrana mitocondriale più sano, meno frammentazione e una migliore sopravvivenza nei test di vitalità. Importante, il numero di strutture di mitofagia bloccate diminuiva, suggerendo che abbassare ATF4 aiutava a ristabilire un equilibrio più efficace tra danno e pulizia. In topi ingegnerizzati per avere una sola copia funzionante del gene ATF4, l'esposizione a UVA provocava meno attivazione di una proteina partner pro‑morte, CHOP, e preservava più cellule endoteliali di forma normale rispetto ai topi con pieno complemento di ATF4.
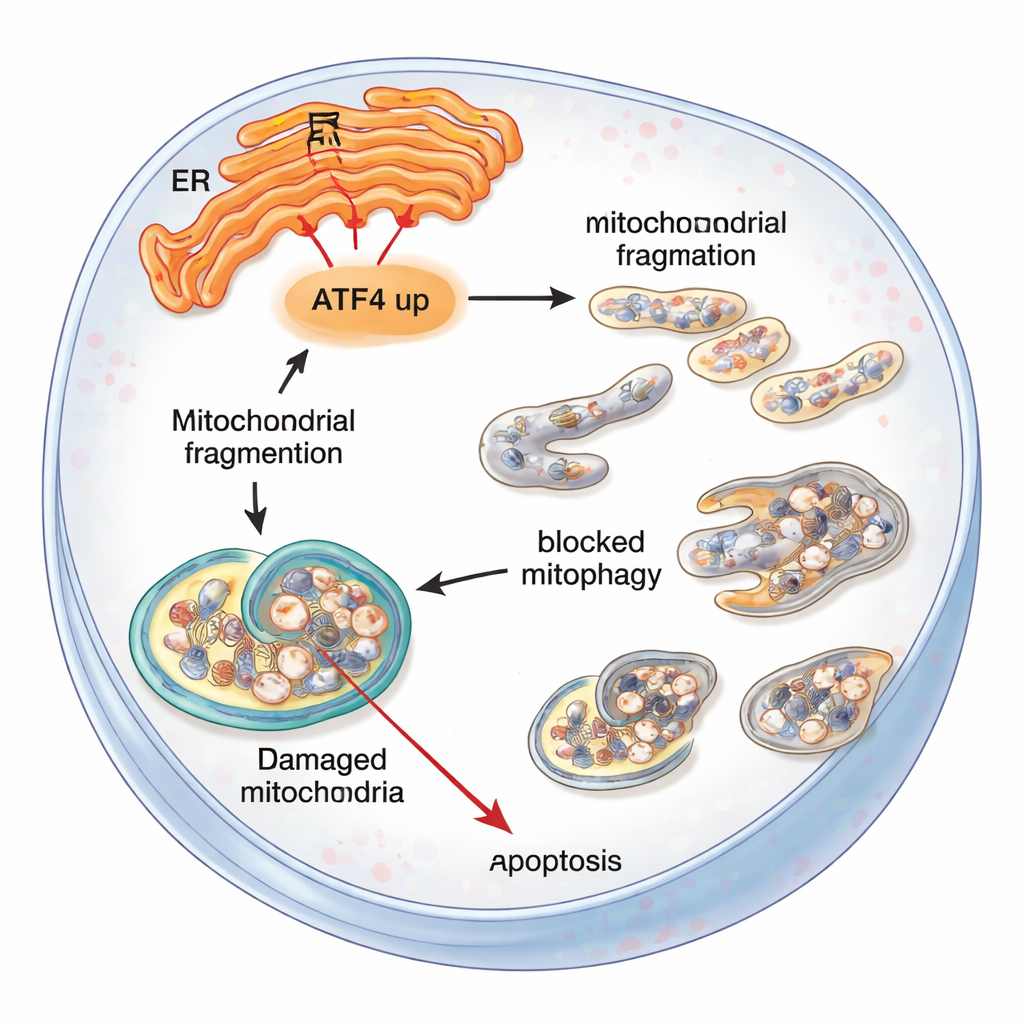
Cosa significa per le persone con FECD
Per i non specialisti, il messaggio è che un singolo messaggero dello stress, ATF4, può far pendere le cellule endoteliali corneali dal coping al collasso. Quando lo stress del reticolo endoplasmatico è prolungato, ATF4 contribuisce a compromettere i mitocondri, blocca la macchina cellulare di smaltimento e infine favorisce l'autodistruzione di queste cellule vitali. Ridurre l'attività di ATF4—sia geneticamente nei topi sia con strumenti molecolari mirati nelle cellule—protegge i mitocondri, migliora la rimozione dei rifiuti e mantiene più cellule in vita. Sebbene questo lavoro sia ancora a livello di laboratorio e animale, mette in luce ATF4 e le vie di stress correlate come promettenti bersagli farmacologici che potrebbero un giorno rallentare o prevenire la progressione della distrofia di Fuchs e ridurre la necessità di trapianto corneale.
Citazione: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Parole chiave: Distrofia endoteliale corneale di Fuchs, endotelio corneale, stress mitocondriale, mitofagia, ATF4