Clear Sky Science · it
Focolai di peste suina africana negli allevamenti di suini tedeschi – esperienze, considerazioni epidemiologiche e sequenze genomiche
Perché un virus dei maiali ci riguarda tutti
La peste suina africana è una malattia virale mortale dei suini che non infetta gli esseri umani ma può devastare gli allevamenti, le forniture alimentari e le economie rurali. Una volta che il virus entra in un Paese, è notoriamente difficile da eliminare. Questo studio esamina da vicino nove focolai di peste suina africana in allevamenti tedeschi tra il 2021 e il 2024, chiedendosi come il virus sia entrato, come si sia diffuso tra i capi e cosa possano rivelare le analisi genetiche dettagliate del virus sui suoi spostamenti.
La battaglia della Germania contro una malattia costosa per i suini
Dopo che la peste suina africana è arrivata in Europa dalla regione del Caucaso nel 2007, si è diffusa ampiamente tra cinghiali e suini domestici. La Germania ha rilevato i primi cinghiali infetti nel 2020 e, entro la fine del 2025, aveva registrato 18 focolai in allevamenti di suini domestici. Questo articolo si concentra su nove di quei focolai verificatisi al di fuori di un particolare cluster del 2024, offrendo la prima panoramica completa delle loro circostanze. Gli allevamenti andavano da recinti familiari con due maiali fino a grandi unità commerciali con migliaia di animali e in genere buone pratiche igieniche. Nonostante queste differenze, ogni focolaio sollevava la stessa domanda scomoda: come ha fatto un virus veicolato principalmente dai cinghiali e dai movimenti di persone a violare le difese aziendali?
Allevamenti diversi, punti deboli simili
I nove focolai delineano un quadro variegato. Nella Germania orientale, diversi allevamenti si trovavano dentro o vicino a zone dove erano già noti cinghiali infetti. Nei piccoli allevamenti familiari con quasi nessuna barriera protettiva, gli investigatori hanno ritenuto molto probabile che erba contaminata, lettiere o terra portata dalle scarpe abbiano trasportato il virus dal selvatico ai recinti dei suini. Al contrario, alcuni grandi allevamenti ben recintati e lontani da casi noti di cinghiali sono comunque risultati infetti. In questi casi gli autori sospettano quelle che chiamano “introduzioni puntuali” legate all’attività umana: forse una piccola negligenza igienica, un oggetto di attrezzatura contaminato o visitatori e lavoratori stagionali provenienti da Paesi colpiti. Spesso la via esatta non poteva essere provata, solo classificata dal più al meno probabile.
Cosa rivelano le impronte genetiche del virus
Per andare oltre le congetture informate, i ricercatori hanno utilizzato il sequenziamento dell’intero genoma—la lettura completa del codice genetico del virus. Confrontando ciascuna variante di focolaio con un virus di riferimento e con quelli trovati nei cinghiali, hanno potuto raggrupparle in distinti “lineaggi” genetici e identificare mutazioni caratteristiche che funzionano come codici a barre. Molti focolai in allevamenti del Brandeburgo e del Meclemburgo-Pomerania Anteriore portavano gli stessi marcatori genetici dei virus dei cinghiali vicini, confermando l’idea che la pressione infettiva dal paesaggio circostante abbia giocato un ruolo chiave. In un caso notevole nel sud della Germania, tuttavia, il virus era privo di tutti i marcatori osservati nei cinghiali del Paese e invece corrispondeva strettamente a ceppi della Moldavia e dell’Italia, indicando un’introduzione separata dall’estero piuttosto che una diffusione silente all’interno della Germania.
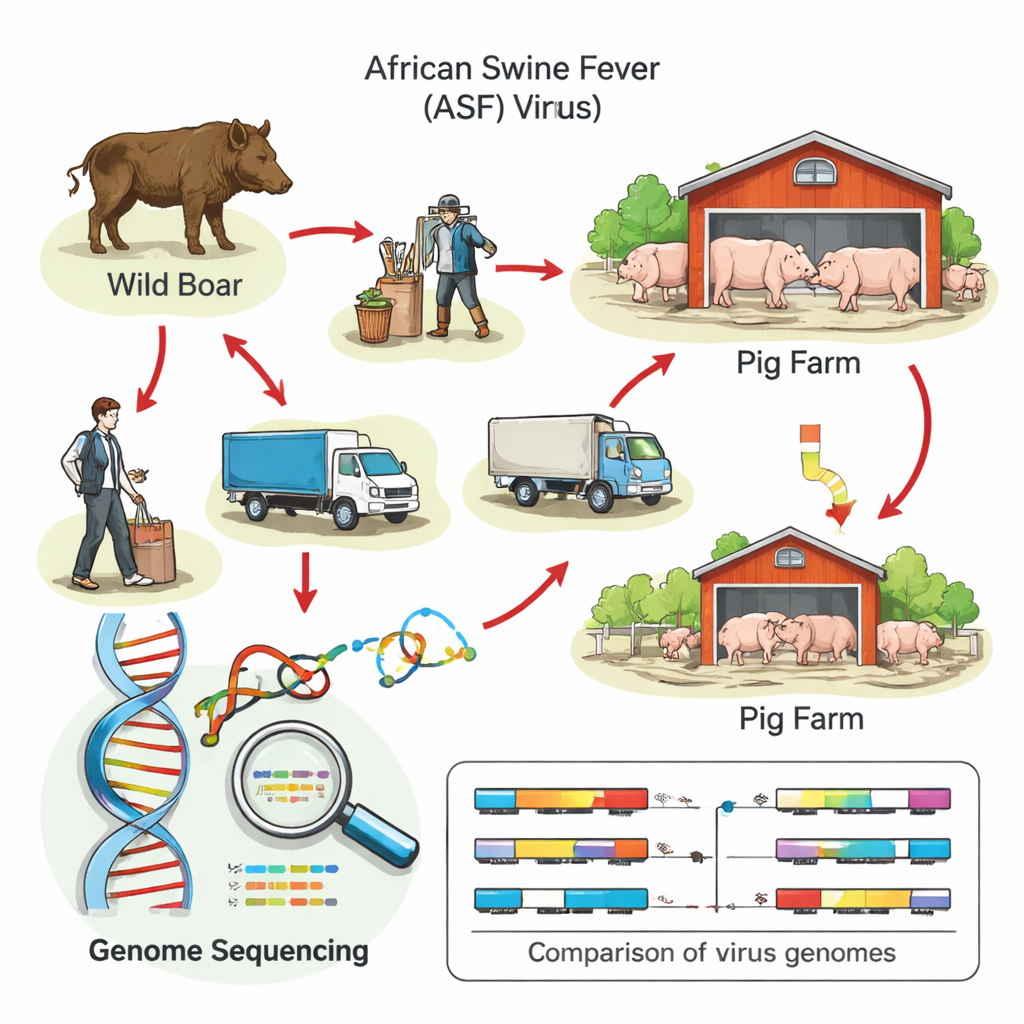
Diffusione lenta dentro gli allevamenti, conseguenze rapide all’esterno
Lo studio mette anche in discussione l’immagine della peste suina africana come malattia “veloce e furiosa”. In diversi allevamenti è stato colpito soltanto un compartimento o un singolo gruppo di suini—even settimane o mesi dopo l’arrivo probabile del virus. Dove i suini erano divisi in unità chiaramente separate e si rispettavano semplici misure di igiene interna, il virus si è mosso sorprendentemente lentamente tra di esse. Al contrario, nei piccoli allevamenti in cui tutti i suini si mescolavano liberamente, ogni animale si è presto infettato. In più casi i veterinari hanno prima curato i maiali malati per presunte infezioni batteriche, ritardando i test per la peste suina africana. Quel ritardo non solo ha aumentato il rischio di ulteriore diffusione, ma ha anche offuscato i ricordi degli allevatori sui movimenti di persone e materiali, rendendo più difficile ricostruire come il virus sia entrato in primo luogo.
Lezioni per proteggere gli allevamenti
Per i lettori non specialisti di veterinaria, la conclusione principale è insieme sobria e piena di speranza. Non esiste ancora un vaccino contro la peste suina africana, quindi la prevenzione si basa quasi interamente sulla biosicurezza—le abitudini quotidiane che impediscono a fango, scarti di carne o utensili carichi di virus di oltrepassare il cancello dell’allevamento. Questo studio mostra che i focolai possono colpire sia i piccoli recinti domestici sia le strutture all’avanguardia, spesso attraverso piccole negligenze facilmente trascurabili. Allo stesso tempo, il preciso confronto dei genomi virali tra cinghiali e suini domestici dimostra che gli strumenti genetici moderni possono aiutare gli investigatori a tracciare le probabili vie di infezione e a distinguere i salti locali da introduzioni a lunga distanza. Gli autori concludono che regole igieniche severe e seguite con costanza, formazione e sensibilizzazione continue e l’uso intelligente del sequenziamento genomico insieme offrono la migliore possibilità di proteggere gli allevamenti di suini—e i mezzi di sussistenza che ne dipendono—da questa malattia costosa.
Citazione: Schulz, K., Calvelage, S., Rogoll, L. et al. African swine fever outbreaks in German pig holdings – experiences, epidemiological considerations and genome sequences. Sci Rep 16, 4350 (2026). https://doi.org/10.1038/s41598-026-36441-1
Parole chiave: Peste suina africana, allevamenti di suini, cinghiali, biosicurezza, sequenziamento del genoma