Clear Sky Science · it
Un approccio integrativo per identificare nuove reti di interazione miRNA-mRNA nella cardiomiopatia da LMNA
Perché contano i piccoli regolatori del cuore
La cardiomiopatia dilatativa è una condizione grave in cui il cuore si dilata e si indebolisce, spesso portando a insufficienza cardiaca, ritmi cardiaci pericolosi e persino morte improvvisa. In molte famiglie questa malattia è ereditaria, e le varianti nel gene chiamato LMNA sono un colpevole frequente. Questo studio pone una domanda apparentemente semplice ma dalle grandi conseguenze: nei cuori danneggiati da mutazioni di LMNA, quali geni vengono attivati o disattivati e quali piccole molecole di RNA stanno tirando questi interruttori? Mappando queste conversazioni molecolari in dettaglio, il lavoro indica nuove vie per prevedere, monitorare e forse un giorno trattare questa forma aggressiva di malattia cardiaca.
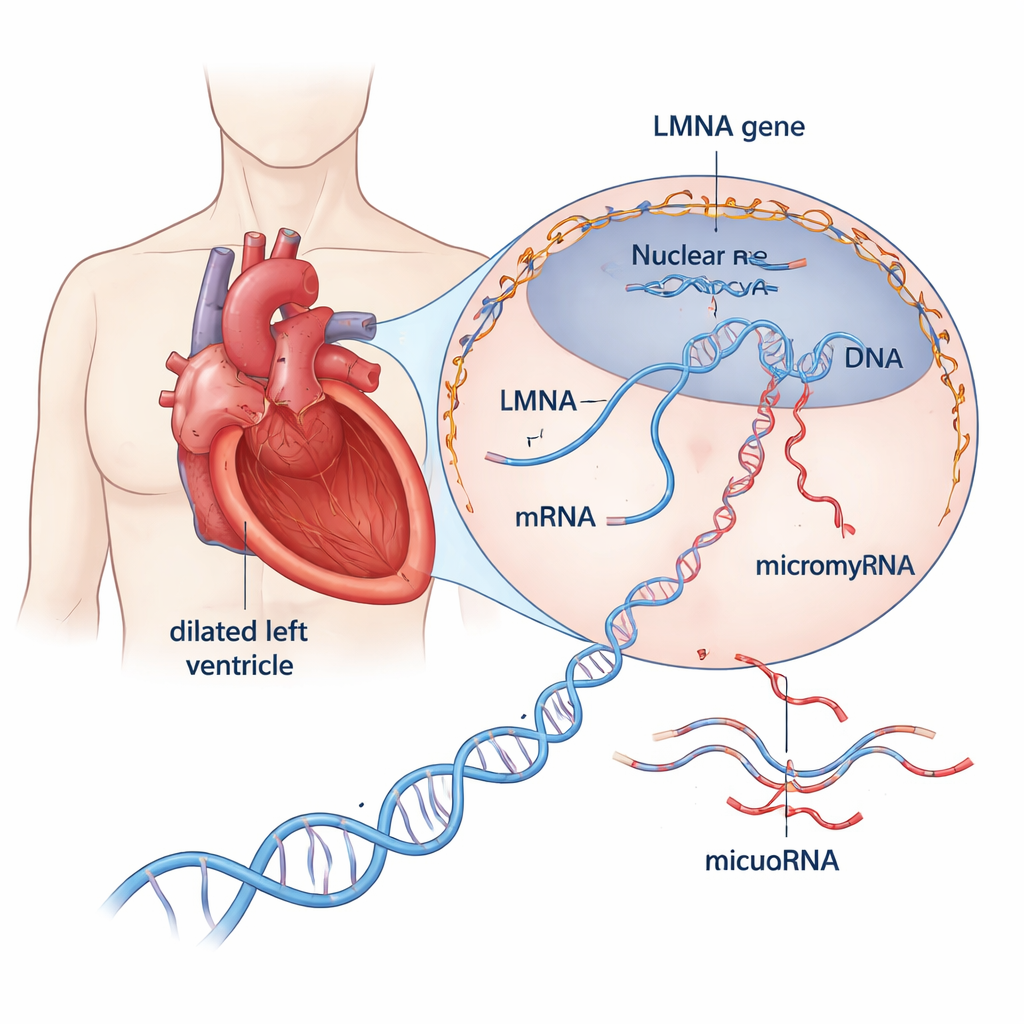
Uno sguardo ravvicinato a una malattia cardiaca pericolosa
La cardiomiopatia dilatativa allunga e assottiglia la principale camera pompante del cuore, indebolendone la capacità di spingere il sangue nel corpo. Circa un terzo fino a metà dei casi un tempo definiti “idiopatici” risulta oggi avere una base genetica. Tra i più di 30 geni coinvolti, LMNA spicca: varianti dannose in questo gene spiegano circa il 10% dei casi ereditari e sono associate a rapida progressione della malattia, problemi di ritmo precoci e un alto rischio di morte cardiaca improvvisa. LMNA codifica per proteine strutturali che formano un’impalcatura attorno al DNA della cellula, contribuendo a mantenere la forma del nucleo e influenzando quali geni sono attivi. Tuttavia, come le proteine LMNA difettose spingano il cuore verso l’insufficienza è rimasto poco chiaro.
Seguire i messaggi all’interno dei cuori di topo
Per esplorare questo, i ricercatori hanno utilizzato un modello murino portatore di una nota mutazione di LMNA (R249W) che sviluppa una forma di cardiomiopatia dilatativa simile alla malattia umana. A 50 settimane di età — quando i topi mostrano ventricoli ingranditi, funzione di pompaggio ridotta e cicatrici fibrotiche — il gruppo ha estratto tessuto cardiaco ed esaminato due tipi di RNA: l’RNA messaggero (mRNA), che porta istruzioni per la produzione di proteine, e il microRNA (miRNA), brevi filamenti non codificanti che regolano finemente l’attività genica bloccando o degradando mRNA specifici. Usando sequenziamento ad alto rendimento e filtri statistici rigorosi, hanno identificato 2.148 geni la cui attività è cambiata nei cuori mutanti e 53 miRNA aumentati o diminuiti rispetto ai topi sani.
Cosa cambia nelle cellule cardiache malate
Quando i ricercatori hanno raggruppato i geni alterati in percorsi biologici sono emersi diversi temi. Molti dei geni modificati erano legati al modo in cui le cellule muscolari cardiache si contraggono, a come si attaccano tra loro e alla matrice di supporto circostante, a come i segnali elettrici si propagano nel cuore e a come le cellule processano i grassi per generare energia. Questi risultati si accordano con il quadro clinico della malattia correlata a LMNA: tessuto rigido e fibrotico; conduzione elettrica disturbata che favorisce aritmie; e squilibrio energetico. Le analisi dei pathway usando database consolidati hanno confermato l’arricchimento nel rimodellamento della matrice extracellulare, nei canali ionici voltaggio-dipendenti, nella comunicazione di tipo sinaptico nel cuore e nel metabolismo degli acidi grassi — suggerendo che la mutazione LMNA interrompe più sistemi interconnessi piuttosto che un singolo passaggio difettoso.
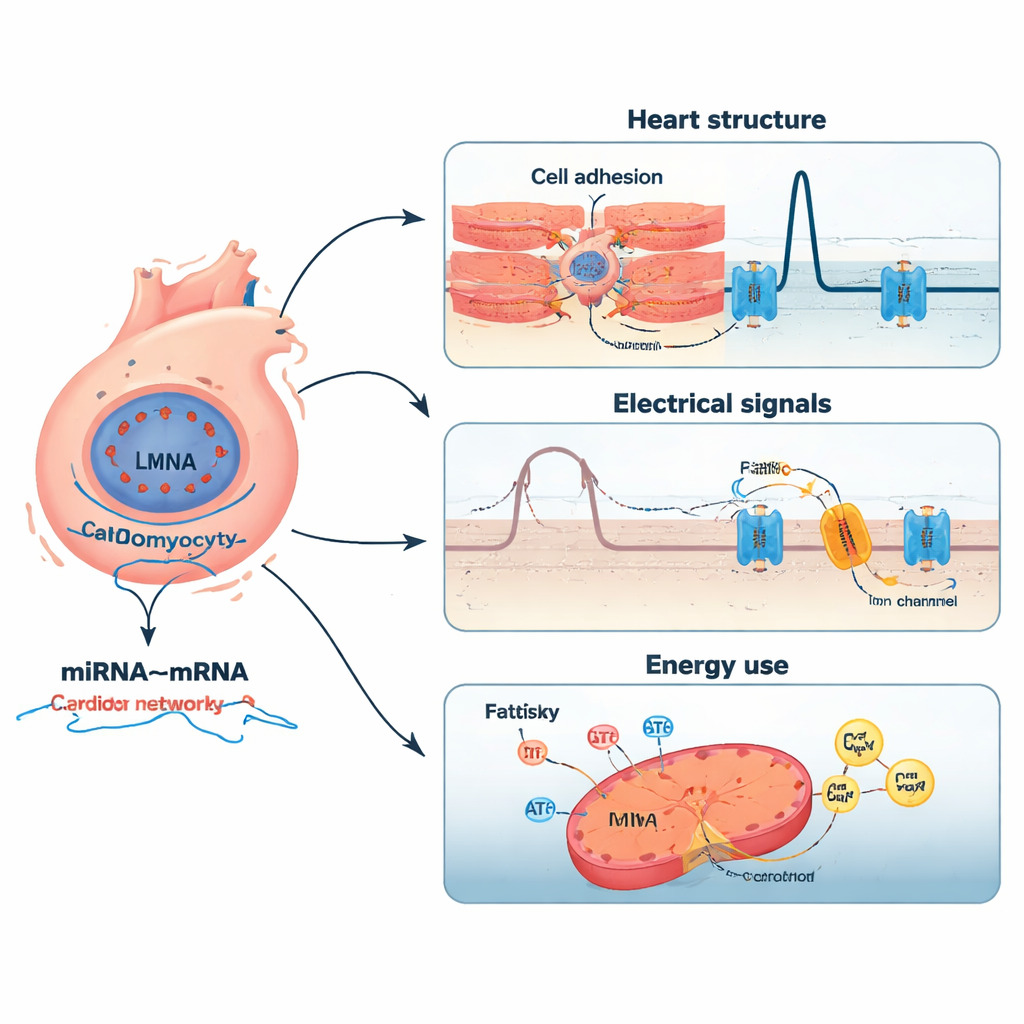
Reti di piccoli interruttori e dei loro bersagli
Lo studio è andato oltre abbinando i miRNA ai loro probabili bersagli mRNA. Utilizzando analisi di correlazione e verifiche incrociate con ampi database di interazioni validate sperimentalmente, gli autori hanno assemblato una rete ad alta affidabilità di 2.197 coppie miRNA–mRNA che coinvolgono 12 miRNA chiave. Alcuni miRNA risultavano più attivi e sembravano attenuare geni critici per lo sviluppo cardiaco, la gestione del calcio e le risposte allo stress ossidativo. Altri erano meno attivi, potenzialmente rilasciando i freni su geni coinvolti nell’adesione cellulare, nell’infiammazione e nel rimodellamento dell’impalcatura strutturale del cuore. Per esempio, un miRNA (miR-183-5p) è stato collegato a un recettore nella via di segnalazione Wnt, che influenza la comunicazione cellula-cellula, mentre un altro (miR-3473a) si connetteva a un canale di rilascio del calcio centrale per il ritmo cardiaco. Insieme, queste reti delineano come spostamenti sottili in piccoli regolatori di RNA possano amplificare l’impatto di una mutazione LMNA.
Dalle mappe molecolari alle terapie future
Per i non specialisti, il punto è che questo studio offre una mappa dettagliata di come una mutazione di LMNA rimodelli il cablaggio interno del cuore a livello di controllo genico. Piuttosto che un singolo “gene cattivo”, la malattia riflette una cascata di messaggi alterati — molti orchestrati dai miRNA — che influenzano la struttura cardiaca, la stabilità elettrica e l’uso di energia. Sebbene il lavoro sia stato condotto nei topi e faccia ampio uso di analisi computazionali, mette in evidenza coppie miRNA–gene specifiche come candidati promettenti per futuri biomarcatori ematici o terapie mirate. A lungo termine, modulare questi piccoli interruttori di RNA potrebbe aiutare i medici a prevedere meglio chi è a maggior rischio, monitorare più precisamente la progressione della malattia e progettare trattamenti più personalizzati per le famiglie colpite da cardiomiopatia correlata a LMNA.
Citazione: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Parole chiave: cardiomiopatia dilatativa, gene LMNA, microRNA, regolazione genica, insufficienza cardiaca