Clear Sky Science · it
L'attività antitumorale di QAL333 e la modellizzazione predittiva: analisi integrata trascrittomica-bioinformatica rivela citotossicità selettiva e determinanti di sensibilità
Perché questo nuovo candidato farmacologico è importante
I farmaci antitumorali funzionano spesso bene per alcuni pazienti ma falliscono per altri, principalmente perché i tumori differiscono nella loro rete biologica interna. Questo studio presenta un composto di nuova progettazione, QAL333, che sembra colpire con maggiore forza alcuni tumori del colon-retto rispetto ad altri, risparmiando nel contempo molte cellule normali. Altro elemento importante, i ricercatori mostrano come i modelli di attività genica nelle cellule tumorali potrebbero aiutare a prevedere chi è più probabile che tragga beneficio, suggerendo strategie di trattamento più precise e personalizzate.
Un attacco mirato su tipi tumorali specifici
Il team ha iniziato testando QAL333, una molecola sintetica correlata a una famiglia di composti già noti per danneggiare le cellule cancerose, su un ampio pannello di 15 linee cellulari tumorali umane e tre linee non cancerose. Hanno scoperto che le cellule del cancro del colon-retto, in particolare una linea chiamata SW620, erano altamente sensibili, con il farmaco che le uccideva a dosi relativamente basse. Al contrario, le cellule del carcinoma mammario triplo negativo risultavano molto più resistenti e richiedevano dosi oltre dieci volte superiori, difficili da raggiungere in sicurezza. È interessante che non tutte le cellule non cancerose reagissero allo stesso modo: alcune erano sensibili, mentre altre, come una linea cellulare renale ampiamente usata, risultavano sorprendentemente resistenti. Questo schema indica che gli effetti di QAL333 dipendono più dalla biologia interna di una cellula che dall'essere etichettata come “cancerosa” o “normale”.
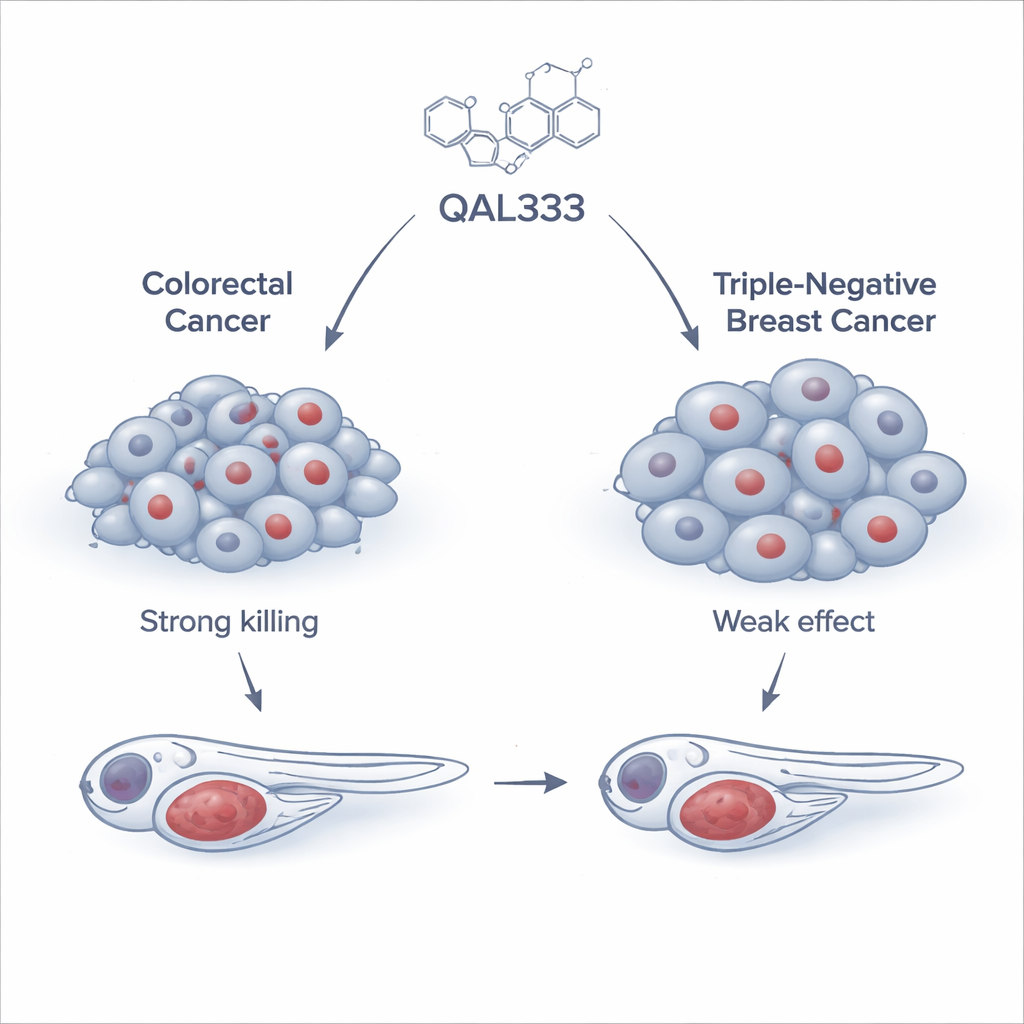
Testare il farmaco in organismi viventi
Per verificare se i promettenti risultati in coltura cellulare si mantenessero in un organismo vivente, i ricercatori si sono rivolti allo zebrafish, un piccolo pesce trasparente ampiamente utilizzato per modellare le malattie umane. Hanno impiantato cellule tumorali umane etichettate con fluorescenza in embrioni di zebrafish e le hanno trattate con QAL333. Nei pesci portatori di cellule del cancro del colon-retto, il farmaco ha chiaramente rallentato la crescita tumorale, avvicinandosi all'effetto di una combinazione chemioterapica standard usata in clinica. Al contrario, i tumori formati dalle cellule di carcinoma mammario triplo negativo hanno risposto a malapena, nonostante un farmaco comune per il cancro al seno, il paclitaxel, abbia funzionato bene nello stesso modello. Questi test in vivo hanno rafforzato l'idea che la forza di QAL333 risieda in un sottoinsieme di tumori piuttosto che in tutti i tipi di cancro.
Scrutare all'interno delle cellule per capire come agisce QAL333
Per comprendere perché alcune cellule muoiono e altre resistono, gli scienziati hanno misurato come migliaia di geni modificavano i loro livelli di attività dopo il trattamento con QAL333. Nelle cellule sensibili del cancro del colon-retto, geni chiave che guidano il ciclo di divisione e la crescita cellulare risultavano soppressi, e importanti vie di sopravvivenza erano attenuate. Anche i segnali legati allo stress ossidativo e a una forma di morte cellulare distinta dall'apoptosi classica erano alterati, suggerendo che QAL333 sovraccarichi sistemi già fragili che gestiscono il danno all'interno di queste cellule. Le cellule resistenti del seno, al contrario, attivavano programmi di stress e infiammazione controllati da fattori come NF-κB, noti per aiutare le cellule a fronteggiare condizioni dannose. Questo confronto affiancato dipinge il quadro di QAL333 che sopraffà difese deboli in alcune cellule mentre altre mettono in atto una risposta di controffensiva efficace.
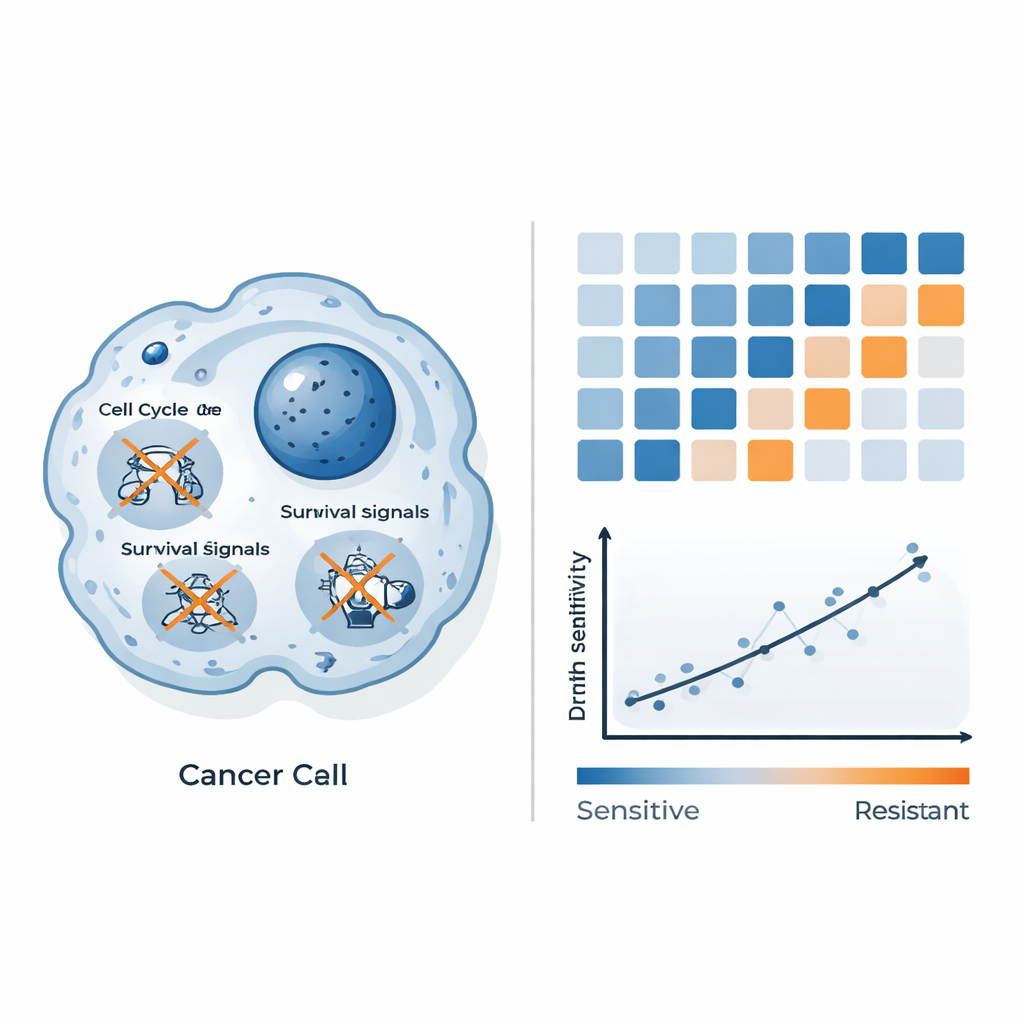
Usare i modelli genici per prevedere chi risponderà
Oltre a catalogare i cambiamenti genici, i ricercatori si sono chiesti se questi schemi potessero essere trasformati in uno strumento predittivo pratico. Hanno combinato i dati di espressione genica di base del pannello di linee cellulari con la loro sensibilità misurata al farmaco e hanno usato l'apprendimento automatico per cercare i segnali più informativi. Piuttosto che fare affidamento su singoli geni, hanno raggruppato i geni in vie biologiche e creato un “punteggio di via” combinato costruito su tre sistemi: come le cellule elaborano energia e sostanze chimiche (vie metaboliche), come organizzano il loro ambiente esterno (proteoglicani e strutture correlate nel cancro) e come è disposto il loro scheletro interno. Questo punteggio composito si associava fortemente alla quantità di QAL333 necessaria per uccidere ciascuna linea cellulare: punteggi più bassi si allineavano a maggiore sensibilità, punteggi più alti a resistenza. In altre parole, il modo in cui queste reti sono regolate all'interno di un tumore può prevedere quanto bene funzionerà QAL333.
Indizi inaspettati di effetti biologici più ampi
Sebbene l'attenzione principale fosse il cancro, QAL333 ha mostrato anche la capacità di disturbare il “quorum sensing”, un sistema di comunicazione che i batteri usano per coordinare comportamenti come la formazione di biofilm. A dosi minime, il composto ha ridotto la formazione di biofilm da parte di un batterio responsabile di malattie gengivali e ha attenuato certi segnali infiammatori nelle cellule immunitarie. Gli autori considerano questi risultati come preliminari ed esplorativi, ma suggeriscono che QAL333 o molecole affini potrebbero un giorno avere impieghi al di là della terapia antitumorale, per esempio nelle infezioni in cui le comunità batteriche sono difficili da eradicare.
Cosa potrebbe significare per i pazienti futuri
Nel complesso, lo studio pone QAL333 come un candidato farmacologico selettivo che colpisce tumori vulnerabili del colon-retto risparmiando molte altre tipologie cellulari, e lo collega a una roadmap per prevedere quali tumori sono più probabili a rispondere. Se confermati in modelli animali più avanzati e infine nei pazienti, un semplice test di espressione genica potrebbe aiutare i medici a decidere quando QAL333 è una buona scelta, in linea con l'obiettivo più ampio di adattare il trattamento del cancro al wiring specifico di ogni tumore. Allo stesso tempo, il lavoro sottolinea che anche i farmaci promettenti hanno limiti: i tumori mammari e altri tumori resistenti potrebbero richiedere combinazioni intelligenti o strategie completamente diverse.
Citazione: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Parole chiave: cancro del colon-retto, terapia mirata, espressione genica, modellizzazione della sensibilità ai farmaci, xenotrapianto in zebrafish