Clear Sky Science · it
Dalla modellizzazione QSAR in silico al saggio MTT in vitro: validazione sperimentale di nuovi candidati uPAR per il carcinoma mammario triplo negativo (TNBC) e il cancro della pelle
Perché questa ricerca è importante
Tumori come il carcinoma mammario triplo‑negativo e alcuni tumori cutanei sono notoriamente difficili da trattare perché si diffondono rapidamente e spesso resistono alle terapie standard. Questo studio esplora un promettente nuovo bersaglio sulla superficie delle cellule tumorali — chiamato uPAR — e mostra come la combinazione di progettazione di farmaci basata sul computer e esperimenti di laboratorio possa individuare nuovi candidati farmacologici in grado di rallentare o fermare la diffusione di questi tumori aggressivi.
Una porta che favorisce la diffusione del cancro
Perché un tumore diventi letale, le sue cellule devono staccarsi dal sito originale, degradare i tessuti circostanti, entrare nel flusso sanguigno e colonizzare organi lontani. uPAR è un aiuto chiave in questo processo. È presente sulla superficie delle cellule tumorali e collabora con proteine partner per attivare enzimi che dissolvono la struttura di supporto circostante, facilitando il movimento e l’invasione cellulare. uPAR è particolarmente abbondante nelle cellule del carcinoma mammario triplo‑negativo e in alcuni tumori cutanei, e la sua presenza è associata a crescita più rapida, maggiore invasività e peggiori outcome per i pazienti. Perciò uPAR rappresenta un bersaglio interessante — sebbene finora poco sfruttato — per farmaci anticancro.
Estrazione di grandi dati chimici con algoritmi intelligenti
I ricercatori hanno iniziato assemblando un ampio insieme di oltre 500 molecole note per bloccare uPAR, tratte da un database pubblico. La struttura di ciascuna molecola è stata tradotta in migliaia di descrittori numerici che catturano caratteristiche come dimensione, forma, distribuzione delle cariche e flessibilità. Con questi dati, il team ha costruito un modello QSAR (quantitative structure–activity relationship) — un tipo di strumento matematico che apprende quali caratteristiche strutturali tendono a rendere una molecola un inibitore più efficace di uPAR. Dopo una convalida attenta per evitare l’overfitting, il modello ha mostrato elevata capacità predittiva su composti non visti in precedenza, evidenziando diverse caratteristiche chiave che rafforzano o indeboliscono il blocco di uPAR. Queste intuizioni hanno guidato la ricerca di nuove molecole progettate meglio.
Dai virtual screen alle provette reali
Con il modello QSAR addestrato, il team ha eseguito uno screening virtuale su una libreria focalizzata di circa 30.000 molecole mirate alle proteasi. Il modello ha rapidamente ristretto questo vasto insieme a un piccolo sottoinsieme di probabili inibitori di uPAR. Parallelamente, simulazioni di docking computazionale sono state impiegate per valutare quanto bene ogni candidato potesse adattarsi al sito di legame di uPAR, e simulazioni di dinamica molecolare hanno testato la stabilità nel tempo di questi complessi legati. Da questa campagna in silico combinata sono emerse due molecole di rilievo: D685‑0061, indicata dal modello QSAR come altamente potente, e C878‑1660, evidenziata da docking e simulazioni per formare interazioni particolarmente stabili con uPAR.
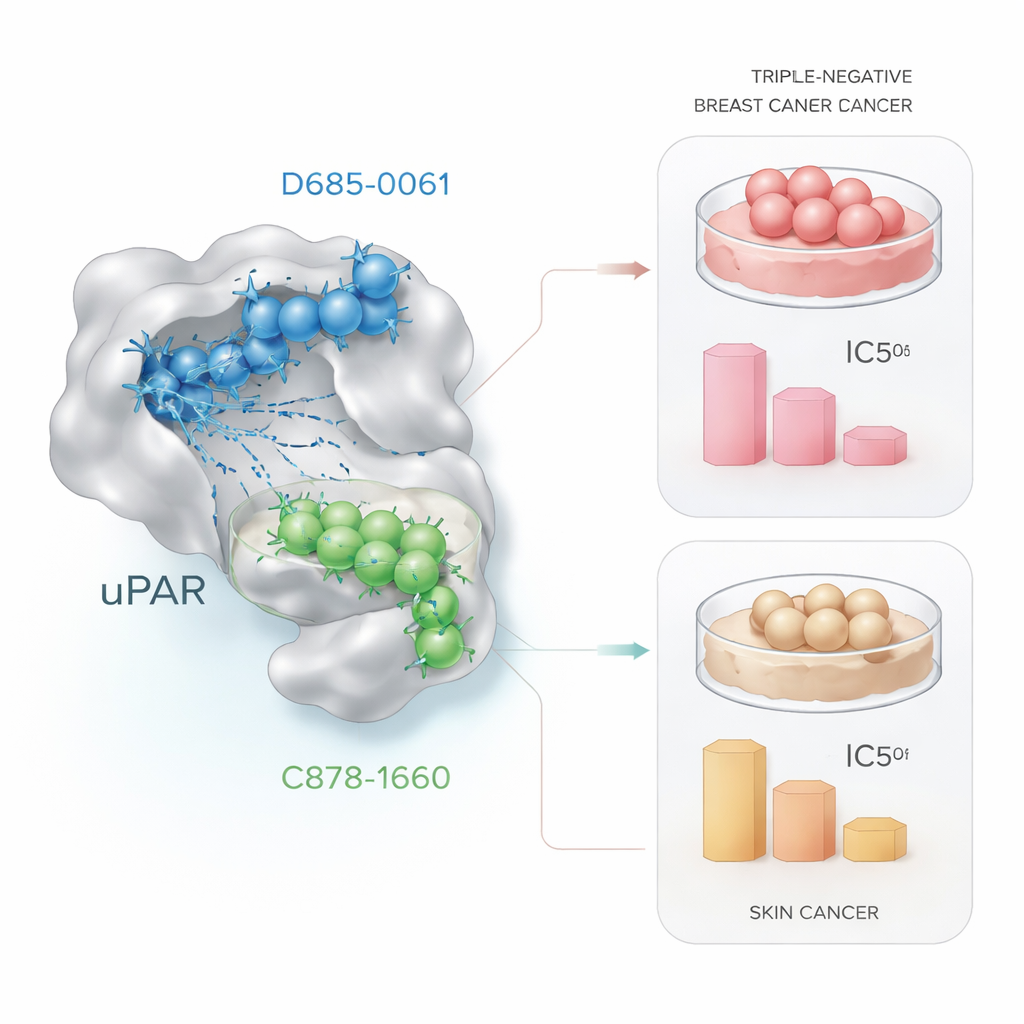
Mettere alla prova i candidati nelle cellule tumorali
Le promesse computazionali hanno valore solo se si traducono in effetti biologici reali. Per testarlo, i ricercatori hanno esposto cellule tumorali vive a dosi crescenti dei due composti principali e hanno misurato la sopravvivenza cellulare mediante un metodo di laboratorio standard chiamato saggio MTT. Nelle cellule del carcinoma mammario triplo‑negativo (MDA‑MB‑231), D685‑0061 ha ucciso le cellule con maggiore efficacia, dimezzando la vitalità a circa 21 micromoli, mentre C878‑1660 ha richiesto approssimativamente quattro volte tale concentrazione. Al microscopio, le cellule trattate con D685‑0061 mostravano segnali chiari di morte cellulare programmata, come arrotondamento, distacco dalla superficie e frammentazione. Al contrario, nelle cellule del cancro della pelle (A431), C878‑1660 si è dimostrato il più potente, raggiungendo il 50% di morte cellulare a circa 19 micromoli rispetto ai circa 28 micromoli per D685‑0061, sempre con danni visibili dipendenti dalla dose.
Cosa significa per i futuri trattamenti contro il cancro
Questo lavoro non fornisce un nuovo farmaco immediato, ma fornisce due punti di partenza promettenti e, altrettanto importante, una solida strategia per trovarne altri. Collegando modellizzazione su larga scala, simulazioni 3D ed esperimenti cellulari ben controllati, lo studio dimostra che uPAR può essere mirato in modo selettivo con piccole molecole capaci di danneggiare cellule aggressive di tumori mammari e cutanei. D685‑0061 e C878‑1660 fungono ora da composti guida che i chimici possono ottimizzare per aumentare la potenza, migliorare la sicurezza e affinare le proprietà farmacocinetiche. A lungo termine, farmaci sviluppati con questo approccio potrebbero contribuire a bloccare la diffusione dei tumori guidati da uPAR, trasformando alcuni degli odierni tumori più pericolosi in malattie più gestibili.
Citazione: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Parole chiave: inibitori uPAR, carcinoma mammario triplo negativo, cancro della pelle, progettazione di farmaci assistita dal computer, saggio di vitalità cellulare MTT