Clear Sky Science · it
Uno studio tramite teoria del funzionale della densità sull'adsorbimento di ciclofosfamide e purinethol su un framework triazino covalente (CTF-2) per applicazioni di somministrazione di farmaci
Perché una chemioterapia più intelligente è importante
I farmaci chemioterapici salvano vite, ma spesso agiscono come un faro invece che come un riflettore puntato—attaccando le cellule sane oltre a quelle tumorali. Questo può provocare effetti collaterali gravi, dalla stanchezza e infezioni fino a danni agli organi. Lo studio qui discusso esplora un materiale ultrasottile e altamente poroso chiamato framework triazino covalente (CTF-2) come una “spugna intelligente” in grado di trasportare due farmaci antitumorali di lunga impiego—ciclofosfamide e purinethol—in modo più sicuro ed efficiente verso il sito d’azione, rilasciandoli poi in condizioni simili a quelle tumorali.
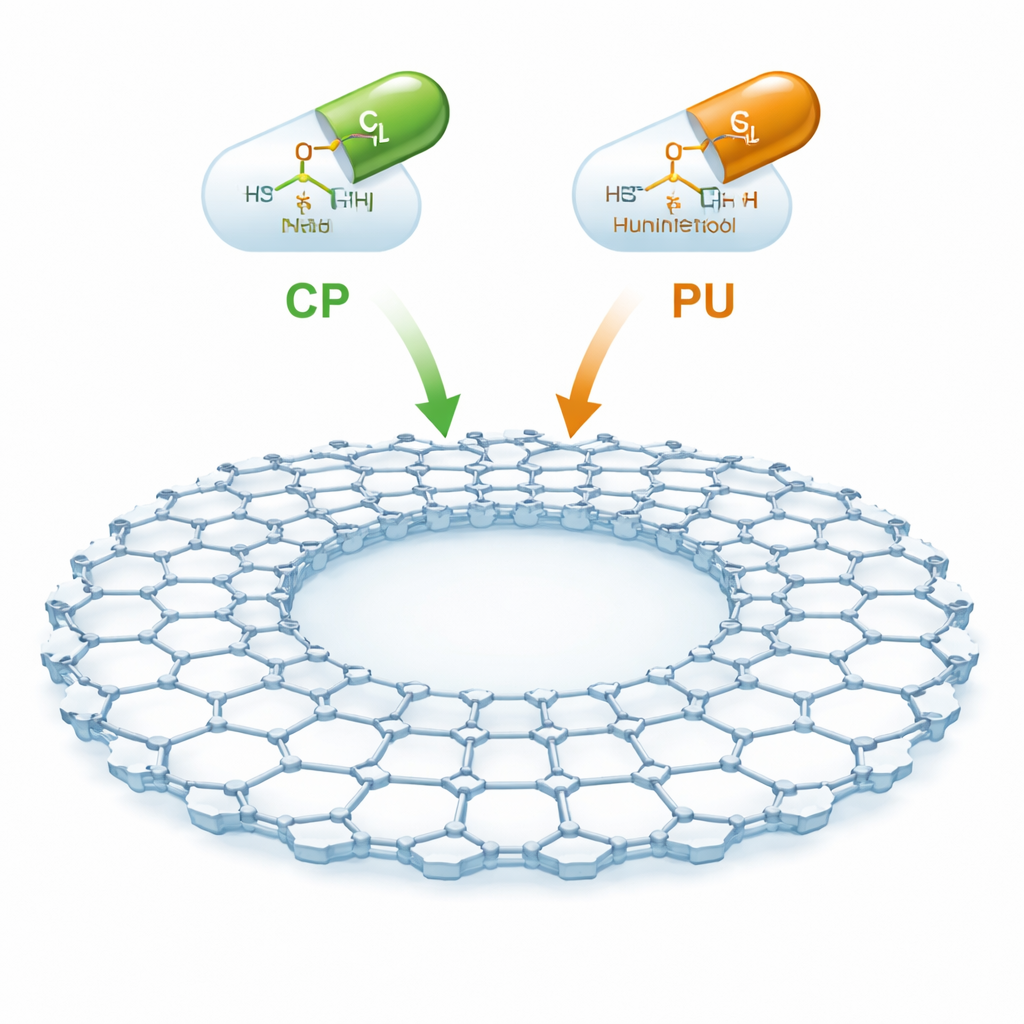
Un nuovo tipo di spugna molecolare
CTF-2 è un materiale artificiale costruito da anelli di carbonio e azoto collegati in una rete piatta a foglio con una grande cavità centrale e molto spazio libero. Essendo sottile, stabile e ricco di pori, offre una grande area superficiale interna per intrappolare molecole farmacologiche. Gli autori si sono concentrati su due importanti medicinali antitumorali: la ciclofosfamide, ampiamente usata per tumori del sangue e tumori solidi, e il purinethol (chiamato anche mercaptopurina), utilizzato contro leucemie e alcune malattie infiammatorie intestinali. L’idea è ancorare questi farmaci in modo delicato alla superficie del CTF-2 affinché possano essere trasportati nel flusso sanguigno e rilasciati in modo più selettivo, riducendo il danno ai tessuti sani.
Esplorare l’invisibile con esperimenti al computer
Invece di lavorare in laboratorio umido, il gruppo ha usato calcoli quantistici avanzati a livello di elettroni (teoria del funzionale della densità e metodi correlati) per valutare quanto intensamente ciascun farmaco aderirebbe al CTF-2 e cosa mantiene insieme i complessi. Hanno ottimizzato le geometrie di CTF-2 con ciascun farmaco, misurato le distanze tra gli atomi in contatto e calcolato l’energia guadagnata quando un farmaco si fissa al framework. Per la ciclofosfamide, l’energia di adsorbimento calcolata era di circa −1,04 electronvolt, leggermente più forte rispetto ai −0,82 electronvolt trovati per il purinethol. Questi valori, che rimangono nettamente favorevoli anche dopo correzioni tecniche e simulazione dell’acqua come solvente, indicano che entrambi i farmaci si legano con sufficiente forza per essere caricati ma non così fortemente da impedire un successivo rilascio.
Forze delicate che svolgono un lavoro importante
Lo studio mostra che il “collante” tra i farmaci e il CTF-2 non è un legame chimico forte ma una rete di forze non covalenti e delicate. Usando analisi specializzate della densità elettronica—fondamentalmente mappe di dove risiedono gli elettroni condivisi—i ricercatori hanno rilevato che le attrazioni di van der Waals (le stesse forze deboli che permettono ai gechi di arrampicarsi) e interazioni elettrostatiche lievi dominano. Queste interazioni avvengono a distanze corte ma non di legame tra atomi di idrogeno, azoto, ossigeno, zolfo e carbonio presenti sui farmaci e sul framework. Calcoli aggiuntivi che scompongono l’attrazione totale nei suoi componenti hanno confermato che le forze elettrostatiche e di dispersione (van der Waals) forniscono la maggior parte della stabilizzazione, mentre forze repulsive evitano che il farmaco si infili troppo profondamente o si leghi in modo irreversibile.
Segnali di caricamento stabile e rilascio modulabile
Il team ha anche esaminato come si ridistribuiscono gli elettroni quando i farmaci sono appoggiati sul CTF-2 e come questo cambia le proprietà elettriche di base. Hanno osservato piccoli ma chiari trasferimenti di carica tra ciascun farmaco e il framework e un lieve restringimento del gap energetico che separa gli stati elettronici occupati da quelli vuoti. Questo implica che la reattività e la conducibilità del materiale sono sottilmente modulate al momento del caricamento, una caratteristica utile per eventuali applicazioni future di rilevamento o teranostica. Fondamentale, quando hanno simulato l’ambiente più acido tipico delle vicinanze tumorali aggiungendo protoni in più, il legame calcolato si è indebolito e le distanze di contatto sono aumentate. In termini semplici, le simulazioni suggeriscono che il CTF-2 può trattenere i farmaci in condizioni normali simili al sangue, ma tende a rilasciarli più facilmente in ambienti acidi simili a quelli tumorali—esattamente il comportamento desiderato per una somministrazione mirata.
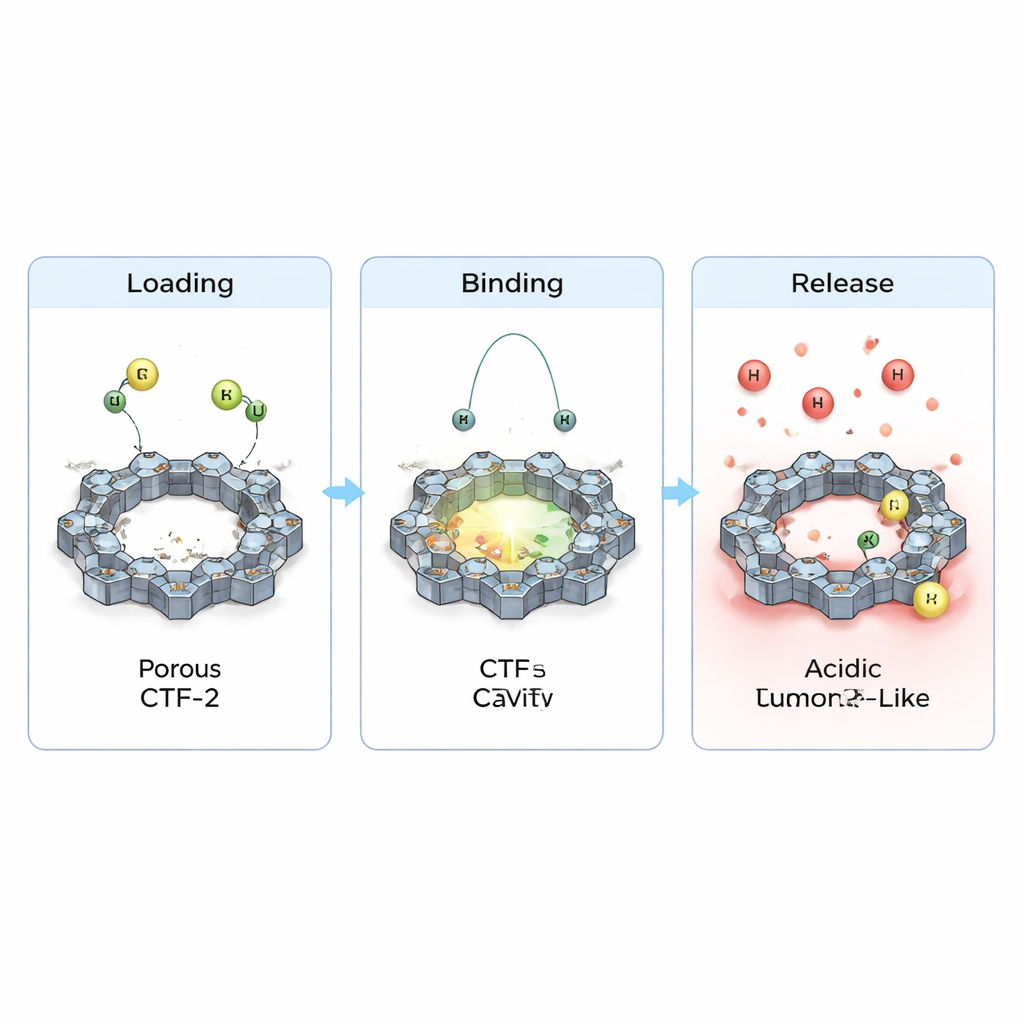
Cosa significa questo per i trattamenti oncologici futuri
Mettendo insieme i risultati, questi calcoli dipingono il CTF-2 come un vettore promettente per ciclofosfamide e purinethol: può caricarli sulla sua superficie porosa in modo stabile, proteggerli durante la circolazione e poi rilasciarli quando la chimica locale cambia attorno a un tumore. Sebbene il lavoro sia teorico e necessiti di conferme sperimentali, suggerisce che framework finemente progettati e ricchi di azoto come il CTF-2 potrebbero contribuire a trasformare farmaci chemioterapici vecchi ma efficaci in medicinali più intelligenti—somministrando dosi potenti dove servono di più riducendo al contempo i danni collaterali alle cellule sane.
Citazione: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Parole chiave: nanocarrier, consegna di farmaci, chemioterapia oncologica, framework triazino covalente, modellizzazione computazionale