Clear Sky Science · it
Un framework interattivo a cascata di deep learning con raffinamento esperto per una segmentazione accurata delle sottoregioni striatali
Perché mappare piccole regioni cerebrali è importante
Lo striato, una piccola struttura situata in profondità nel cervello, svolge un ruolo centrale nel movimento e nella motivazione ed è fortemente coinvolto in malattie come la malattia di Parkinson. I medici spesso usano scansioni PET e MRI per misurare i cambiamenti chimici in quest’area, ma lo striato è suddiviso in molte piccole sottoregioni difficili da visualizzare e delineare con precisione. Questo articolo presenta un nuovo metodo assistito dal computer, chiamato StriaSeg‑iARM, che aiuta gli specialisti a tracciare questi confini in modo più accurato ed efficiente, anche in persone il cui cervello è alterato dall’invecchiamento o dalla malattia.
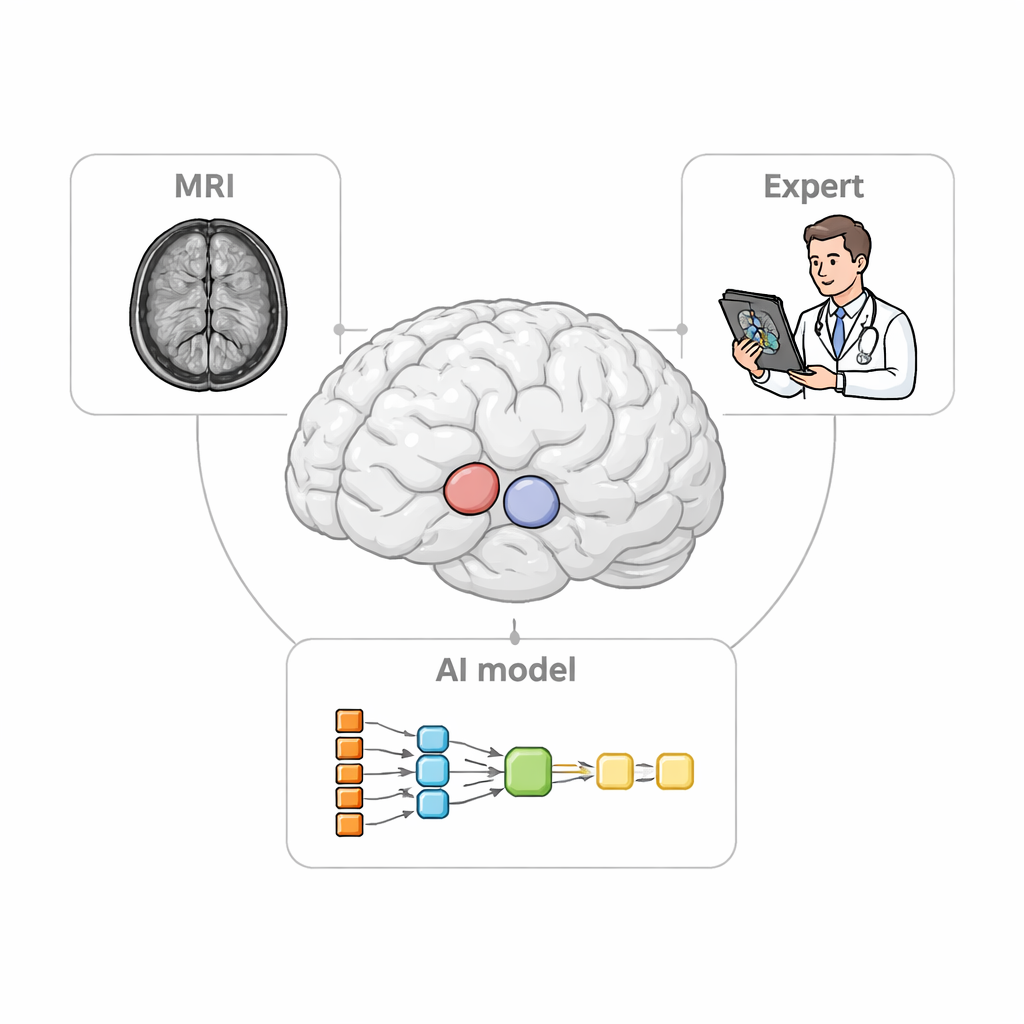
Il problema clinico sotto gli occhi
Quando i neurologi valutano condizioni come la malattia di Parkinson, si basano sulle scansioni PET per seguire come i segnali legati alla dopamina variano nelle diverse parti dello striato. Per farlo correttamente devono prima definire piccole “regioni di interesse” tridimensionali sulla MRI, che fungono da misurini per i dati PET. Delineare manualmente queste regioni è un lavoro lento e noioso e può variare da un esperto all’altro. Il software esistente individua automaticamente solo le strutture più grandi e spesso fatica nei pazienti con cervelli rimpiccioliti o distorti, situazione comune nelle fasi avanzate delle malattie neurodegenerative. Queste limitazioni possono offuscare il vero schema del danno e ridurre l’efficacia dell’imaging come strumento diagnostico.
Un assistente più intelligente in due passaggi
I ricercatori hanno progettato StriaSeg‑iARM come un sistema di deep learning in due fasi che lavora direttamente nello spazio cerebrale del singolo individuo anziché forzare la scansione in un modello standard. Nella prima fase il programma individua l’intero striato su una MRI tridimensionale. Nella seconda fase suddivide questa struttura in 12 sottoregioni definite anatomicamente su entrambi gli emisferi. Tra le due fasi sta l’innovazione chiave: un passaggio interattivo in cui un esperto può rapidamente verificare e, se necessario, correggere il contorno approssimativo prodotto dalla prima fase prima che venga eseguita la suddivisione più fine. Questo approccio combina la velocità dell’automazione con il giudizio di un osservatore umano formato.
Addestramento e test su cervelli del mondo reale
Per insegnare al sistema cosa cercare, il team ha raccolto centinaia di scansioni MRI provenienti da più ospedali e tipi di scanner, e ha creato accurate delineazioni manuali delle 12 sottoregioni striatali. Hanno quindi testato il modello su due dataset esterni contenenti sia MRI che scansioni PET legate alla dopamina: uno su pazienti con Parkinson in fase relativamente precoce e volontari sani, e un altro su un gruppo clinico più anziano e più gravemente compromesso con marcata atrofia cerebrale e diagnosi miste. In questi casi difficili, StriaSeg‑iARM ha costantemente riprodotto le delineazioni manuali degli esperti meglio dei metodi tradizionali basati su atlanti e di un modello di deep learning a singola fase, con maggiore sovrapposizione, confini più accurati e misurazioni di volume stabili.
Misurazioni più nitide per le scansioni chimiche cerebrali
Poiché l’obiettivo finale è quantificare i segnali PET, gli autori hanno anche esaminato come i diversi metodi di segmentazione influenzassero le letture PET. Utilizzando una misura standard del legame del tracciante in ciascuna sottoregione, hanno confrontato i risultati automatici con quelli basati su delineazioni manuali. Il metodo basato su atlante tendeva a sottostimare il legame, soprattutto nei pazienti con cambiamenti più severi, mentre il modello di deep learning di base mostrava ancora un bias evidente in alcune regioni. Al contrario, i modelli a cascata—soprattutto quando veniva usato il passaggio interattivo di correzione—producevano valori PET che seguivano da vicino il riferimento degli esperti, con bias e dispersione minimi. Il team ha inoltre dimostrato che un semplice punteggio di incertezza della prima fase può segnalare circa un quarto dei casi più difficili dove il raffinamento esperto è davvero necessario, lasciando il resto completamente automatico.
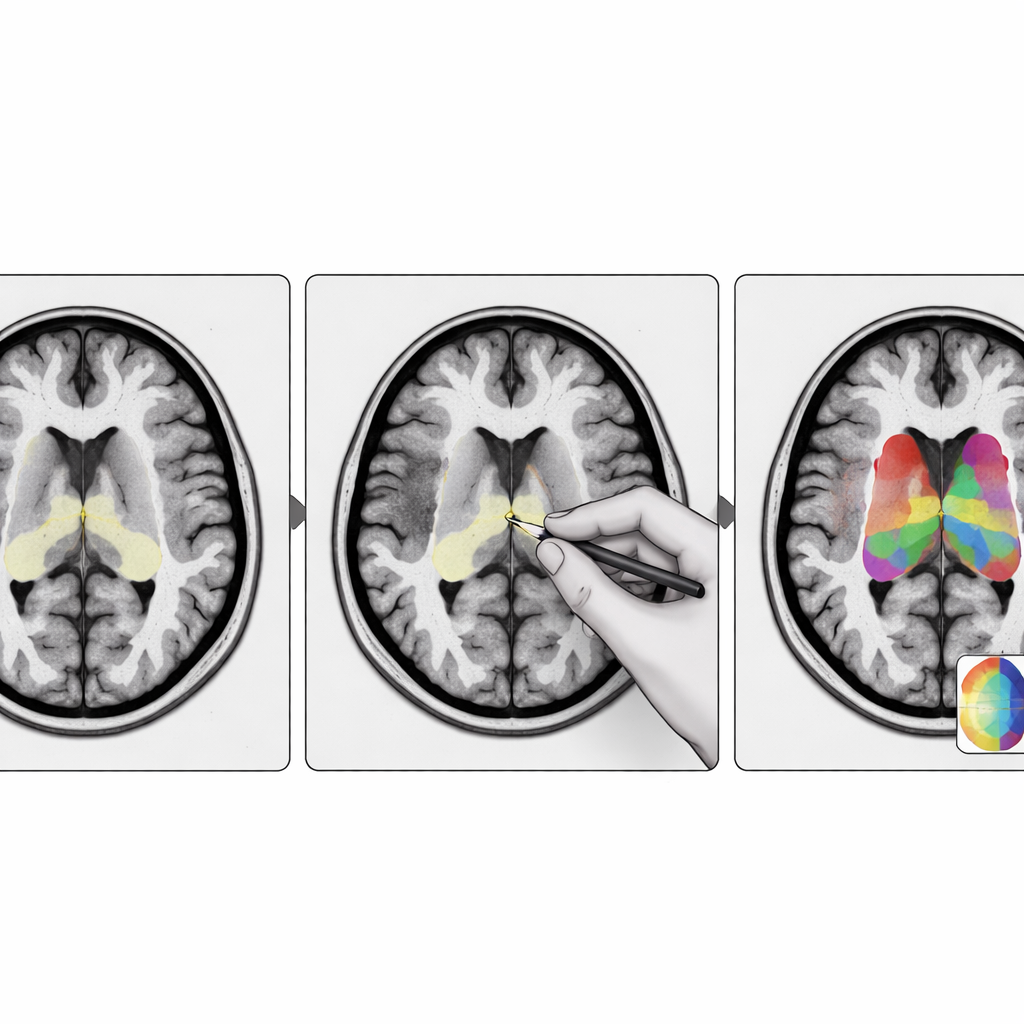
Cosa significa per pazienti e clinici
Per i non specialisti, il messaggio è che mappe digitali migliori delle piccole regioni cerebrali possono rendere le scansioni chimiche del cervello più affidabili. StriaSeg‑iARM offre un framework flessibile in cui un modello di deep learning svolge la maggior parte del lavoro, ma gli specialisti possono comunque intervenire per correggere i casi problematici senza dover riaddestrare il sistema. Questa combinazione di automazione e supervisione esperta migliora la precisione delle misurazioni usate per diagnosticare e monitorare malattie come la malattia di Parkinson, e potrebbe essere adattata ad altri organi e patologie in cui piccole strutture difficili da vedere contengono indizi rilevanti.
Citazione: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Parole chiave: Imaging della malattia di Parkinson, segmentazione dello striato, deep learning in radiologia, PET e MRI cerebrale, biomarcatori neurodegenerativi