Clear Sky Science · it
Impiego dell'approccio di screening virtuale ad alto rendimento (HTVS) per l'identificazione di nuovi inibitori della lattato deidrogenasi (LDH) con proprietà anticancro
Perché questa ricerca è importante per il trattamento del cancro
Le cellule tumorali spesso riorganizzano il modo in cui producono energia, e questo cambiamento può essere sfruttato per progettare farmaci più intelligenti e selettivi. Questo studio esplora un enzima metabolico chiave chiamato lattato deidrogenasi (LDH), che aiuta i tumori a prosperare in condizioni avverse e a resistere ai trattamenti. Utilizzando avanzati metodi di screening computerizzato e test di laboratorio, i ricercatori hanno identificato due nuove piccole molecole che bloccano la LDH e mostrano promettenti effetti anticancro in linee cellulari di carcinoma prostatico.
Il metabolismo anomalo delle cellule tumorali
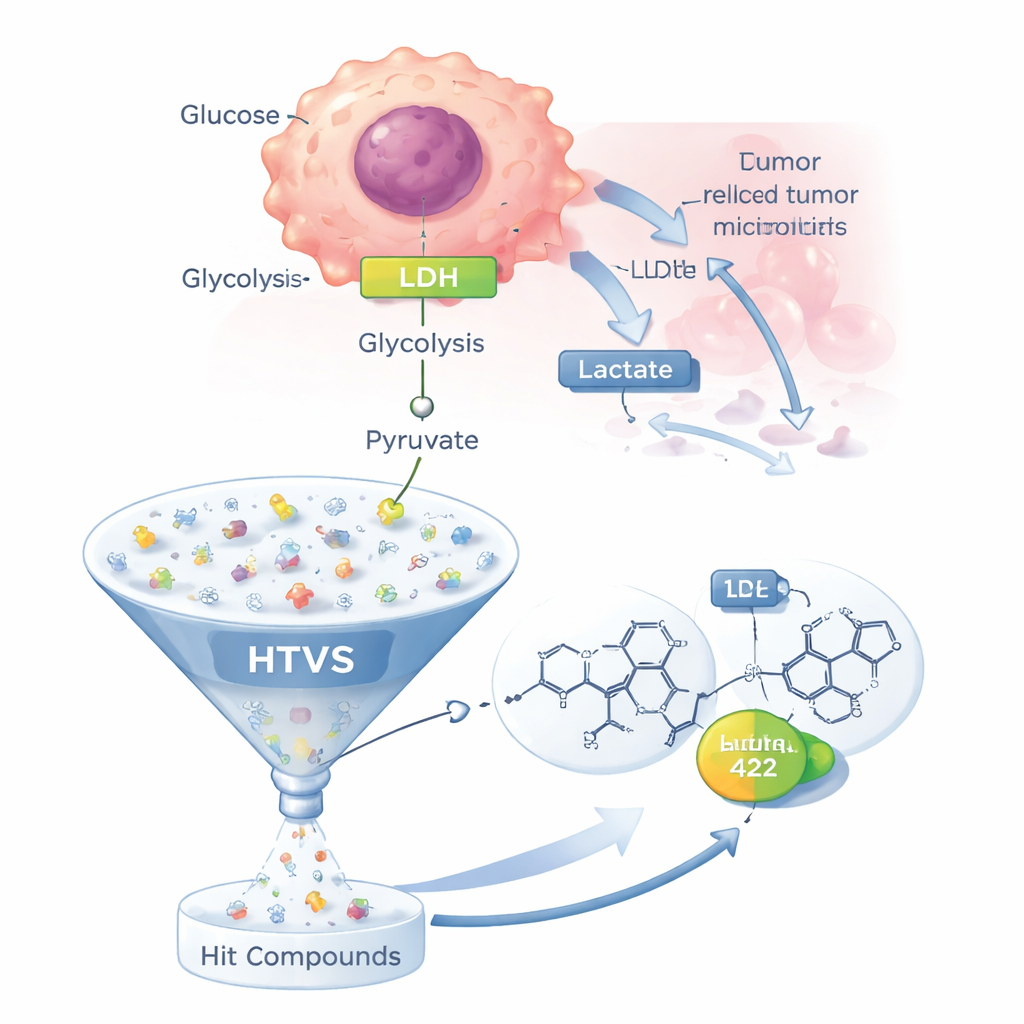
La maggior parte delle cellule sane utilizza l'ossigeno in modo efficiente nei mitocondri per generare energia. Molte cellule cancerose, invece, dipendono fortemente da una via meno efficiente chiamata glicolisi, anche quando l'ossigeno è abbondante — un fenomeno noto come effetto Warburg. In questo percorso più breve, il glucosio viene degradato a piruvato, che viene quindi convertito in lattato dalla LDH invece di essere inviato nei mitocondri. Il lattato viene espulso dalla cellula, acidificando l'ambiente tumorale, aiutando le cellule cancerose a eludere la morte cellulare, indebolire l'azione del sistema immunitario e persino attenuare gli effetti di molti chemioterapici. Poiché la LDH si trova al centro di questo metabolismo alterato e nessun farmaco mirato alla LDH è ancora stato approvato, è diventata un obiettivo prioritario per nuove terapie anticancro.
Usare i computer per setacciare mezzo milione di molecole
Invece di testare potenziali farmaci uno alla volta in laboratorio, il team ha utilizzato una strategia di screening virtuale ad alto rendimento (HTVS). Hanno iniziato con 28 molecole note per bloccare la LDH riportate in letteratura scientifica e ne hanno estratto un "farmacoforo" — un modello 3D astratto di caratteristiche che un buon inibitore della LDH è probabile condivida. Hanno poi applicato questo modello a una libreria commerciale di circa 500.000 molecole con caratteristiche da farmaco, chiedendosi quali candidati corrispondessero alle caratteristiche essenziali. Circa 110.000 molecole hanno superato questo primo filtro, e una selezione ulteriore basata su regole standard di "drug-likeness" ha ridotto la lista a 2.337 candidati più realistici per il docking sull'enzima LDH.
Focus sui migliori leganti
Il passaggio successivo è stato stimare quanto strettamente questi candidati potessero adattarsi al sito attivo della LDH. Utilizzando diversi livelli di docking computazionale, i ricercatori hanno calcolato come ciascuna molecola potrebbe interagire con specifici amminoacidi all'interno della tasca dell'enzima. Questo processo a più stadi ha progressivamente ridotto il pool da migliaia di candidati a sole 59 molecole promettenti, e poi a cinque chiari "hit" con un legame predetto particolarmente forte. Due di queste, etichettate composti 15 e 422, si sono distinte perché le simulazioni dinamiche molecolari suggerivano che formassero complessi insolitamente stabili con la LDH nel tempo, mantenendo contatti chiave con residui critici nel sito attivo pur preservando una ragionevole struttura proteica complessiva.
Dallo screening alle cellule tumorali reali
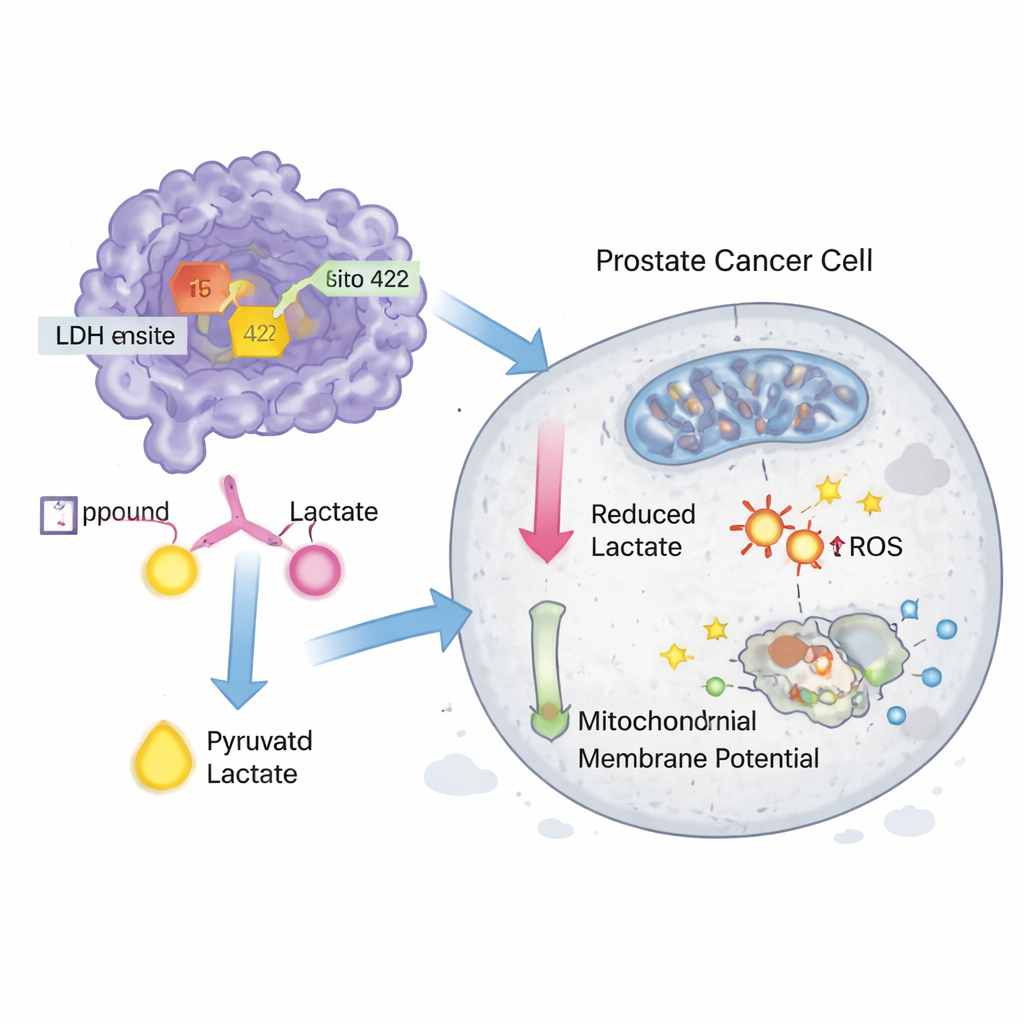
Per verificare se questi hit avessero effetti nei sistemi viventi, gli scienziati hanno acquistato i composti 15 e 422 e li hanno testati in linee cellulari di carcinoma prostatico DU-145 e PC-3. Entrambe le molecole inibivano l'attività della LDH nelle cellule a concentrazioni nanomolari e rallentavano anche direttamente l'attività di un enzima LDH purificato, sebbene fossero leggermente meno potenti rispetto a un noto inibitore sperimentale chiamato GNE‑140. Nei saggi di proliferazione, i composti hanno ridotto la sopravvivenza delle cellule tumorali a dosi micromolari basse, avvicinandosi nuovamente alle prestazioni di GNE‑140. Esperimenti aggiuntivi hanno mostrato che i trattamenti aumentavano leggermente lo stress ossidativo, perturbavano il potenziale di membrana mitocondriale — segno di mitocondri compromessi — e attivavano la morte cellulare programmata (apoptosi) nelle cellule DU‑145, con il composto 15 risultato essere il più attivo dei due.
Cosa potrebbe significare per i futuri farmaci anticancro
Pur non essendo ancora farmaci pronti all'uso, queste molecole forniscono punti di partenza preziosi per la progettazione di nuovi farmaci. Sia i composti 15 sia 422 possiedono proprietà chimiche che suggeriscono migliore solubilità, permeabilità e generale "drug-likeness" rispetto ad alcuni inibitori della LDH esistenti, rendendoli candidati interessanti per ulteriori ottimizzazioni. Lo studio dimostra come lo screening computazionale su larga scala, guidato da caratteristiche strutturali note, possa scoprire nuovi inibitori della LDH che indeboliscono le cellule tumorali privandole della loro fonte energetica alterata. Con lavori futuri volti a perfezionare le loro strutture, testare il legame diretto in modo più rigoroso e studiarne il comportamento negli animali, questi composti potrebbero contribuire a una nuova classe di agenti anticancro che attaccano i tumori attraverso le loro vulnerabilità metaboliche uniche.
Citazione: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Parole chiave: inibitori della lattato deidrogenasi, metabolismo del cancro, screening virtuale, cancro alla prostata, scoperta di farmaci anticancro