Clear Sky Science · it
Decifrare la patogenesi della BPCO: un approccio multi-omico per identificare metaboliti e legami genetici
Perché la malattia polmonare e la chimica del corpo sono legate
La broncopneumopatia cronica ostruttiva (BPCO) è nota soprattutto come malattia del fumatore, ma questo studio mostra che ciò che accade nella chimica del nostro sangue può essere altrettanto importante di ciò che respiriamo. Combinando grandi dataset genetici, misurazioni dettagliate di piccole molecole nel sangue ed esperimenti di laboratorio su cellule delle vie aeree umane, i ricercatori hanno scoperto come un alterato trattamento dei grassi nell’organismo potrebbe contribuire alla BPCO — e come un farmaco inalatorio familiare, il Salbutamolo, potrebbe aiutare in un modo sorprendente.
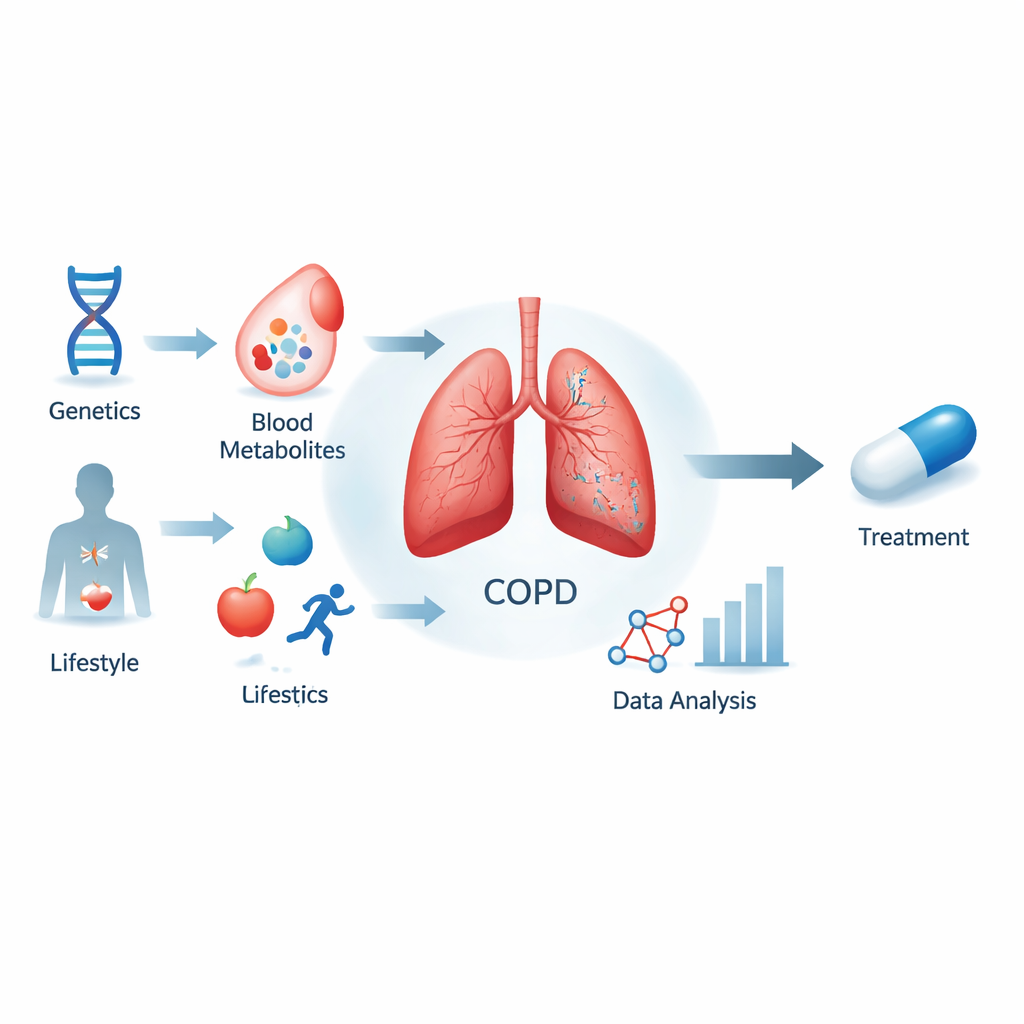
Guardare dentro la BPCO oltre il fumo
La BPCO colpisce centinaia di milioni di persone nel mondo ed è destinata a diventare la terza causa di morte. Sebbene fumo e inquinamento atmosferico siano responsabili principali, non spiegano del tutto chi sviluppa la BPCO o quanto rapidamente progredisce. Il team dietro questo lavoro si è chiesto se specifiche molecole nel sangue, chiamate metaboliti, non siano solo segnali di danno ma attori attivi nella malattia. Si sono concentrati su oltre 1.400 metaboliti misurati in grandi studi europei e li hanno collegati al rischio di BPCO usando le differenze genetiche delle persone come una specie di esperimento naturale.
Usare i geni per testare causa ed effetto
Per andare oltre la semplice correlazione, i ricercatori hanno utilizzato una tecnica chiamata randomizzazione mendeliana. In termini semplici, hanno verificato se le persone nate con varianti genetiche che aumentano o diminuiscono certi metaboliti hanno anche maggiori o minori probabilità di sviluppare la BPCO. Questo approccio aiuta a separare le cause vere dalle abitudini di vita che possono confondere il quadro, come il consumo di caffè o il fumo. Su 1.400 metaboliti, sei sono risultati inizialmente legati al rischio di BPCO. Tuttavia, un secondo test genetico più stringente ha mostrato che solo due — la Carnitina C14 e la 3-idrossioleilcarnitina — condividono lo stesso segnale genetico di base della BPCO. Entrambe sono correlate al modo in cui l’organismo gestisce gli acidi grassi a catena lunga, suggerendo che il metabolismo dei grassi, non solo l’infiammazione e il flusso d’aria, è al centro della BPCO.
Dalle molecole agli interruttori di controllo chiave
Una volta identificati i due metaboliti affidabili, i ricercatori li hanno ricondotti alle “strade” metaboliche che percorrono. Queste strade convergevano sul metabolismo degli acidi grassi e hanno evidenziato un insieme di enzimi che funzionano come semafori, controllando quanto grasso viene sintetizzato o degradato — in particolare gli enzimi ACACA e ACACB. Esplorando banche dati esistenti su farmaci e interazioni proteina-proteina, il team ha scoperto che questi enzimi fanno parte della stessa rete di ADRB2, il bersaglio proteico del Salbutamolo, un comune inalatore di salvataggio per la BPCO. Le analisi di tessuto polmonare di pazienti hanno mostrato che ACACA e ACACB erano aumentati, mentre ADRB2 risultava diminuito, coerente con uno stato di sovraccarico di acidi grassi nei polmoni malati.
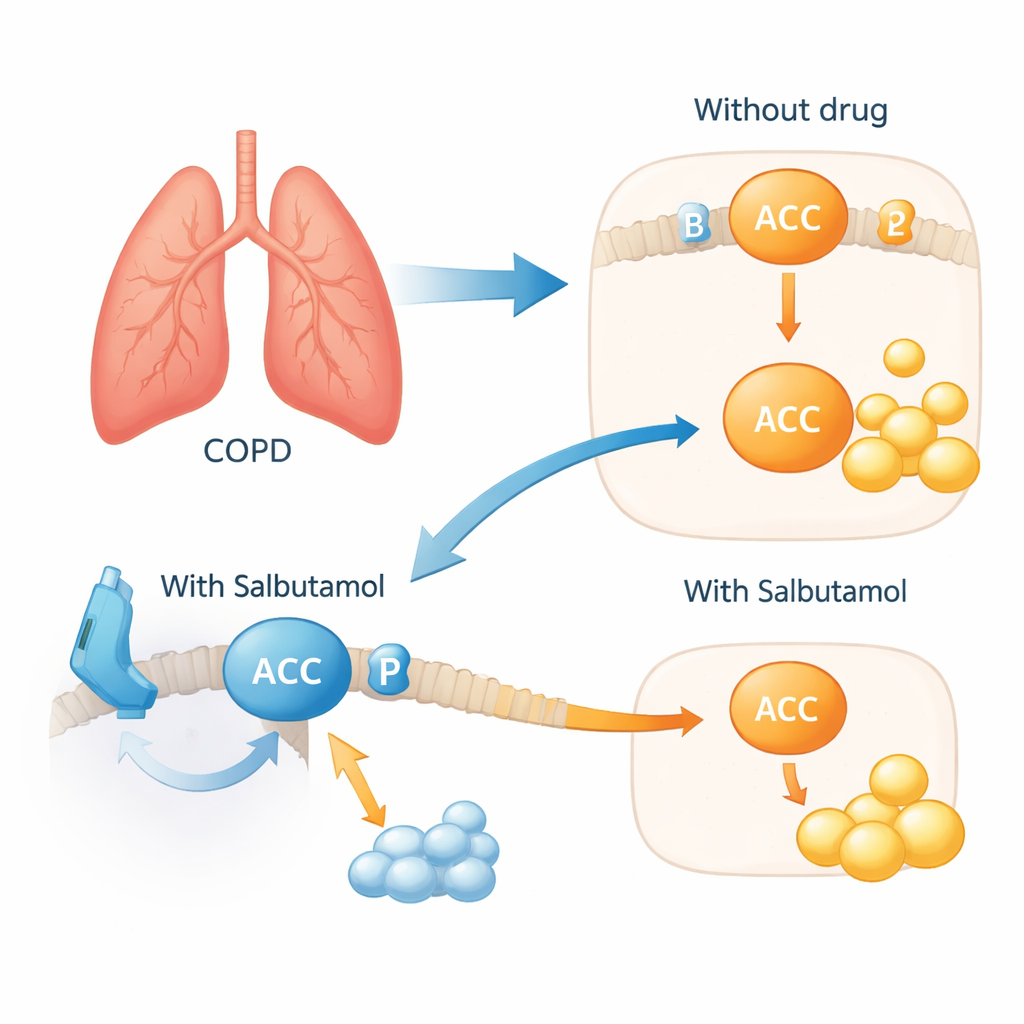
Un inalatore che calma anche i grassi fuori controllo
Per verificare se questa rete è importante nelle cellule vive, gli scienziati hanno esposto cellule bronchiali umane a estratto di fumo di sigaretta per mimare lo stress simile alla BPCO. Le cellule hanno risposto aumentando ACACA e ACACB e riducendo un marcatore chimico protettivo su ACACA che normalmente limita la produzione di grassi. Quando è stato aggiunto il Salbutamolo, questo schema dannoso si è invertito: il marcatore protettivo su ACACA è stato ripristinato e i segnali di sintesi lipidica eccessiva sono diminuiti. In termini semplici, il farmaco sembra aver messo i freni alla macchina che costruisce i grassi nelle cellule delle vie aeree, agendo attraverso l’interruttore ADRB2 sulla superficie cellulare. Analisi genetiche basate su stili di vita hanno inoltre sostenuto l’idea che i due metaboliti chiave siano legati alla biologia sottostante piuttosto che solo ad abitudini come il consumo di caffè, che ha spiegato via via diversi altri candidati.
Cosa significa per i pazienti e i trattamenti futuri
Per i non specialisti, il messaggio principale è che la BPCO potrebbe essere in parte guidata da un ingorgo metabolico nel modo in cui le cellule polmonari elaborano i grassi, e che un broncodilatatore ampiamente usato potrebbe anche contribuire a sbloccare quell’ingorgo. La Carnitina C14 e la 3-idrossioleilcarnitina emergono come forti marcatori ematici che un giorno potrebbero aiutare a segnalare le persone a rischio maggiore o a monitorare la progressione della malattia. Gli enzimi ACACA e ACACB, posti in punti di snodo chiave del metabolismo lipidico e collegati al bersaglio del Salbutamolo ADRB2, offrono nuove leve per gli sviluppatori di farmaci. Sebbene siano necessari ulteriori studi in popolazioni diverse e approfondimenti metabolici, questo approccio multi-omico apre una strada verso trattamenti per la BPCO che fanno più che aprire le vie aeree: potrebbero anche ripristinare un uso più sano del carburante all’interno dei polmoni.
Citazione: Zeng, M., Liu, J., Cao, X. et al. Unraveling COPD pathogenesis: a multi-omics approach to identify metabolites and genetic links. Sci Rep 16, 6013 (2026). https://doi.org/10.1038/s41598-026-36368-7
Parole chiave: BPCO, metabolismo degli acidi grassi, Salbutamolo, biomarcatori carnitina, multi-omica