Clear Sky Science · it
Valutazione traslazionale di BUB1B come marcatore di medicina di precisione per il carcinoma epatocellulare
Perché un gene della divisione cellulare conta per il cancro al fegato
La maggior parte delle persone pensa al cancro in termini di masse visibili nelle immagini diagnostiche, ma all’interno di quei tumori operano sistemi di controllo microscopici che decidono come e quando le cellule si dividono. Questo studio si concentra su uno di questi interruttori di controllo, un gene chiamato BUB1B, e mostra come possa aiutare i medici a prevedere quali pazienti con cancro al fegato avranno esiti peggiori, chi potrebbe rispondere a certi farmaci e perché alcuni tumori sfuggono al sistema immunitario. Trasformando un regolatore fondamentale del ciclo cellulare in una sorta di “cruscotto” del comportamento del carcinoma epatocellulare, il lavoro indica la strada verso trattamenti più precisi e personalizzati.
Un cancro al fegato comune ha bisogno di migliori indicatori
Il carcinoma epatocellulare, la forma primaria del cancro al fegato più frequente, viene spesso scoperto in fase avanzata, quando compaiono i sintomi e le opzioni terapeutiche sono limitate. I test ematici e i marcatori tissutali attuali, come l’alfa-fetoproteina o Ki-67, sono imperfetti: non individuano in modo affidabile la malattia precoce né guidano terapie su misura. Gli autori hanno quindi cercato un diverso tipo di marcatore—uno che rifletta il cablaggio interno delle cellule tumorali anziché la sola presenza del tumore. Si sono concentrati su BUB1B, una proteina che aiuta a garantire la corretta separazione dei cromosomi durante la divisione cellulare. Quando questo sistema viene compromesso, si accumulano errori genetici che possono alimentare tumori aggressivi.
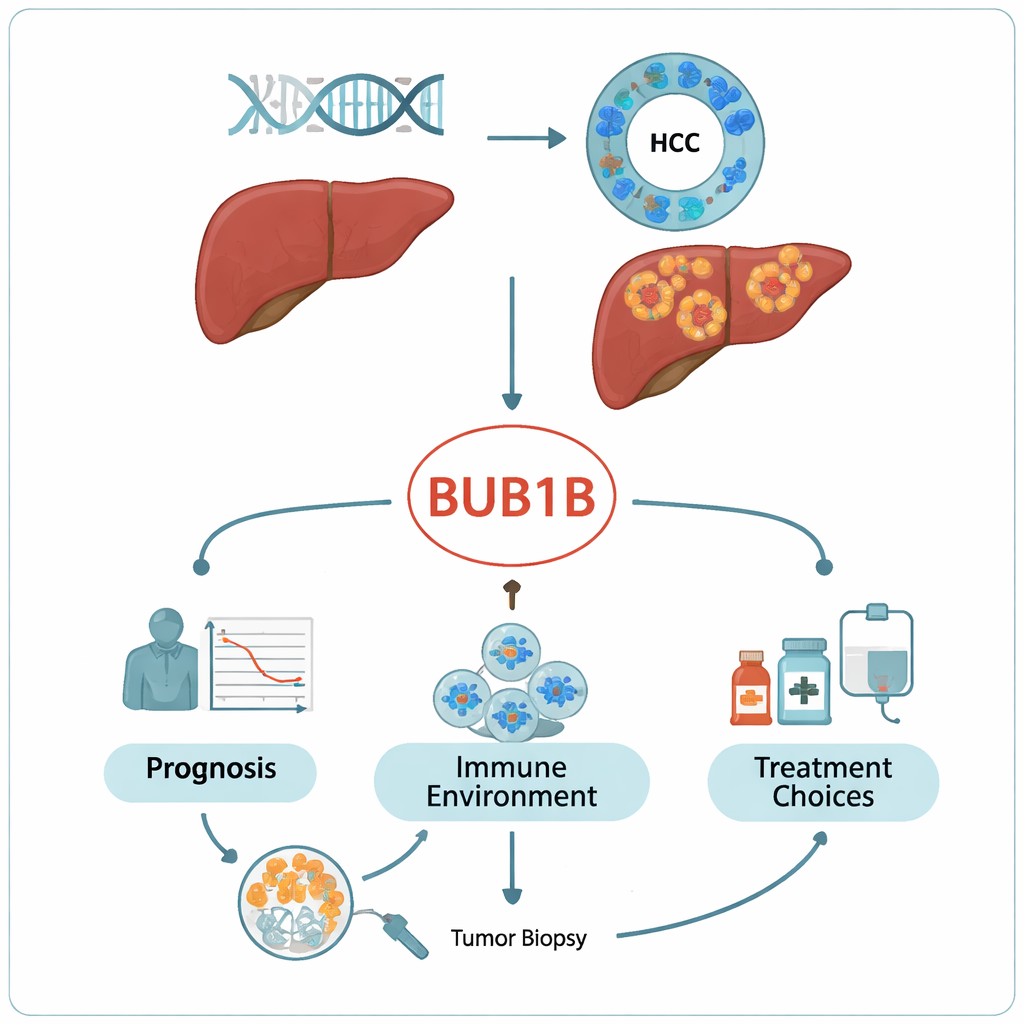
Tracciare BUB1B nei tumori e nei pazienti reali
Usando grandi banche dati pubbliche sul cancro, incluso The Cancer Genome Atlas, i ricercatori hanno prima analizzato l’attività di BUB1B in molti tipi di tumore. Hanno riscontrato che è sovraespresso in 19 diversi tumori, con una sovraattivazione particolarmente marcata nei tumori epatici rispetto al tessuto sano circostante. I pazienti il cui carcinoma epatocellulare presentava livelli elevati di BUB1B tendevano ad avere una sopravvivenza più breve, anche dopo aver corretto per lo stadio della malattia, rendendo BUB1B un indicatore prognostico indipendente. Una revisione approfondita di 50 pazienti con cancro del fegato trattati nel loro ospedale ha confermato il modello: i tumori mostravano un’intensa colorazione per BUB1B al microscopio, soprattutto nel citoplasma cellulare, e livelli elevati si associavano a tumori più grandi, stadio più avanzato e peggior sopravvivenza.
Caos genetico, risposta ai farmaci e un sistema immunitario confuso
Un’elevata espressione di BUB1B non segnalava solo che un tumore era pericoloso; era correlata a una più profonda instabilità del DNA canceroso. I tumori con BUB1B più alto mostravano segni di difetti nella riparazione del DNA e forme sottili di instabilità microsatellite, segni distintivi di caos genomico che possono accelerare l’evoluzione tumorale e influenzare la risposta alle terapie. Modelli computazionali che collegano pattern genici ai test farmacologici suggerivano che i carcinomi epatocellulari ad alto BUB1B potrebbero essere più vulnerabili ad alcuni farmaci, inclusi il farmaco mirato sorafenib e chemioterapici classici come paclitaxel e doxorubicina, pur mostrando relativa resistenza a farmaci diretti sulla via EGFR. Allo stesso tempo, questi tumori contenevano numerose cellule immunitarie, in particolare linfociti T, ma risultavano comunque elevati negli indici di disfunzione e di esclusione immunitaria—cioè il sistema immunitario era presente ma di fatto disarmato, rendendo meno probabile una risposta alle immunoterapie comuni che bloccano PD-1 o PD-L1.
Come BUB1B alimenta i segnali di crescita nelle cellule tumorali
Per andare oltre i legami statistici, il gruppo ha testato cosa accade quando BUB1B viene chimicamente inibito in cellule di carcinoma epatocellulare coltivate in laboratorio. L’inibizione di questo gene ha ridotto un’intera catena di segnali di crescita comunemente raggruppati nelle vie MAPK. Attori chiave a diversi livelli—compresi RAS, alcuni membri della famiglia RAF, ERK e molte chinasi correlate come p38—sono risultati fortemente ridotti. Poiché queste vie funzionano come una staffetta che istruisce le cellule tumorali a continuare a dividersi e a resistere allo stress, la loro attenuazione suggerisce che BUB1B non è solo un marcatore passeggero ma un driver attivo che contribuisce a mantenere il cablaggio interno del cancro. Alcuni componenti hanno mostrato rimbalzi inaspettati, suggerendo circuiti di retroazione intrinseci, ma l’effetto complessivo è stata un’attenuazione diffusa della segnalazione pro-crescita.
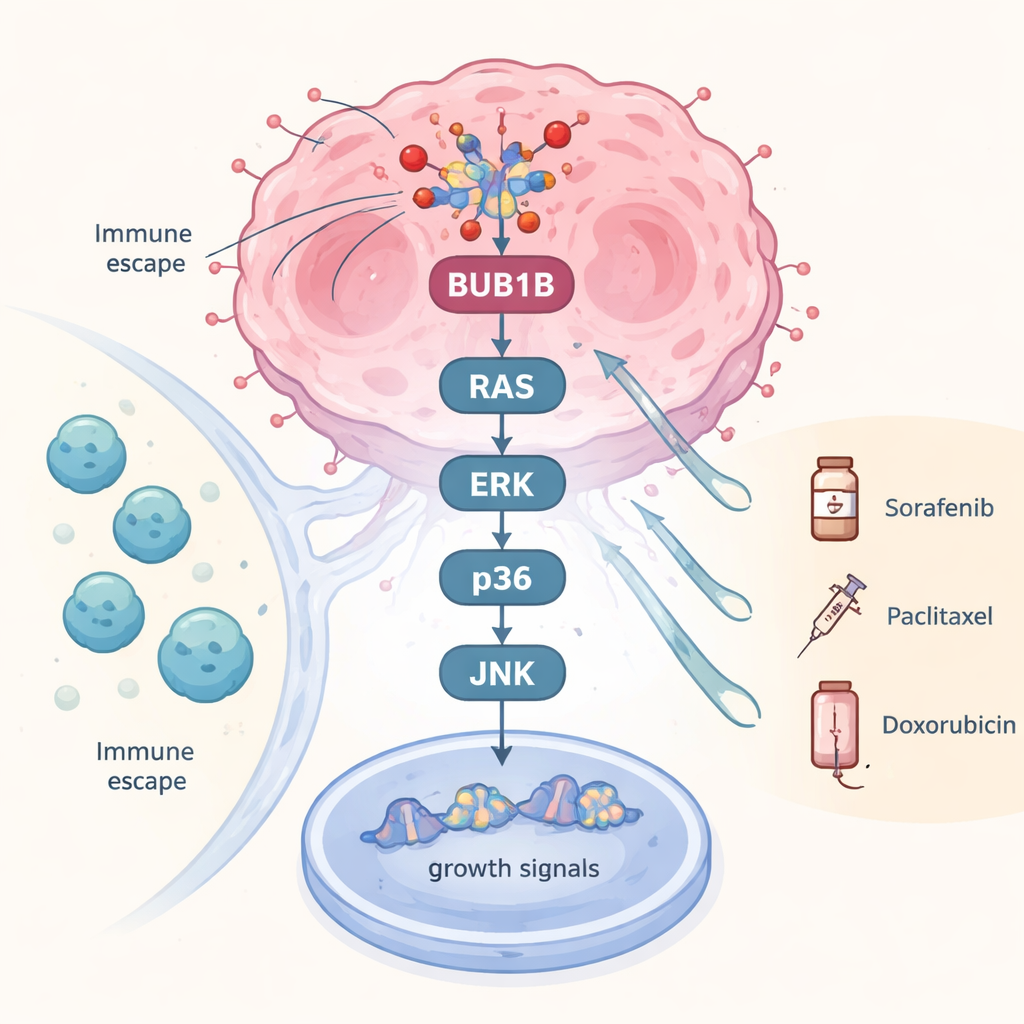
Cosa significa per i pazienti e per le cure future
Per i non specialisti, la conclusione è che un singolo gene della divisione cellulare, BUB1B, sembra trovarsi al crocevia di tre caratteristiche cruciali del carcinoma epatocellulare: quanto è instabile il DNA del tumore, come comunica con il sistema immunitario e come risponde a diversi farmaci chiave. Misurare BUB1B nei campioni tumorali potrebbe aiutare i medici a raggruppare i pazienti per rischio, stimare la sopravvivenza con maggiore precisione e scegliere trattamenti che sfruttino le debolezze del tumore—pur riconoscendo quando l’immunoterapia standard è improbabile che funzioni. Poiché i tumori del fegato dipendono da BUB1B per mantenere i segnali di crescita e di risposta allo stress, farmaci che prendono di mira questa proteina, da soli o in combinazione con terapie esistenti, potrebbero aprire nuove strade verso cure più precise ed efficaci per il carcinoma epatocellulare.
Citazione: Sun, Cy., Yu, X., Deng, Lq. et al. Translational evaluation of BUB1B as a precision medicine biomarker for hepatocellular carcinoma. Sci Rep 16, 5301 (2026). https://doi.org/10.1038/s41598-026-36364-x
Parole chiave: carcinoma epatocellulare, BUB1B, marcatore, segnalizzazione MAPK, oncologia di precisione