Clear Sky Science · it
La downregulation di CDC25C sopprime la crescita dell’HCC attraverso autofagia e apoptosi indotte da stress mitocondriale
Perché questo studio sul cancro al fegato è importante
Il cancro al fegato è uno dei tumori più letali a livello globale e molti pazienti vengono diagnosticati troppo tardi perché chirurgia o trattamenti standard siano efficaci. Questo studio esplora un singolo “interruttore” cellulare, una proteina chiamata CDC25C, che sembra favorire la crescita del tumore epatico pur essendo meno critica per le cellule epatiche sane. Riducendo l’attività di questo interruttore, i ricercatori hanno osservato che è possibile stressare e infine eliminare le cellule tumorali tramite i meccanismi di autolimpieza e autodistruzione della cellula, indicando una strategia terapeutica promettente e più selettiva.
Un interruttore di crescita all’interno dei tumori epatici
Ogni cellula deve decidere quando dividersi e quando fermarsi. CDC25C è una delle proteine chiave che spingono la cellula attraverso il ciclo di divisione. Nel carcinoma epatocellulare questo interruttore è spesso bloccato in posizione “on”, favorendo la crescita e la diffusione del tumore. Il gruppo ha usato cellule di carcinoma epatico murino e cellule epatiche normali di topo, oltre a topi portatori di tumore, per ridurre artificialmente i livelli di CDC25C. Hanno confermato, con test genetici e proteici standard, che CDC25C era fortemente ridotta nel gruppo sperimentale rispetto ai controlli, stabilendo un modello solido per studiare cosa accade quando questo interruttore di crescita viene attenuato.
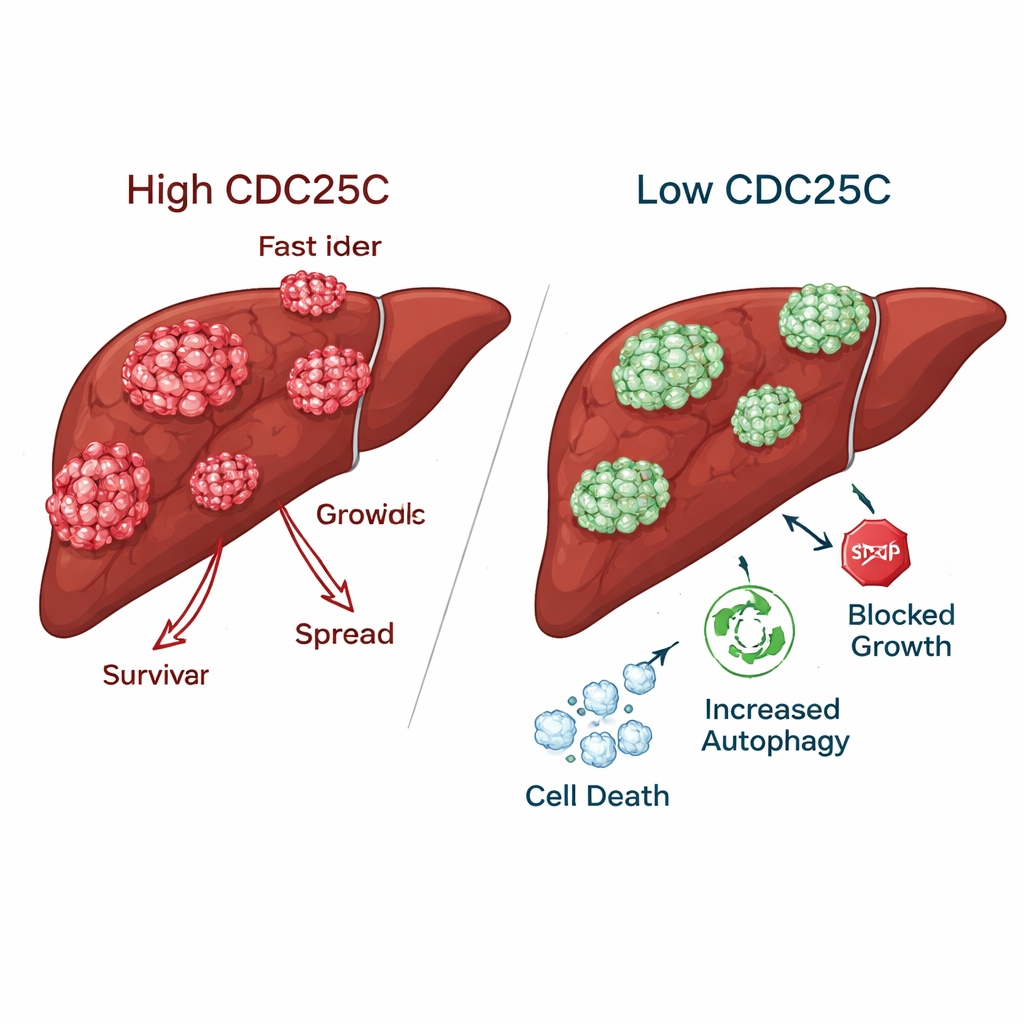
Rallentare il cancro risparmiando le cellule sane del fegato
Quando CDC25C è stata ridotta nelle cellule tumorali epatiche, i tumori hanno perso molte delle loro caratteristiche aggressive. Le cellule tumorali hanno formato molte meno colonie, hanno migrato più lentamente attraverso “ferite” artificiali e sono state meno capaci di attraversare e invadere barriere nei test di laboratorio. Al contrario, le cellule epatiche normali hanno mostrato una crescita e una mobilità migliorate quando CDC25C è stata abbassata, suggerendo che il tessuto sano può tollerare o addirittura beneficiare dell’inibizione di CDC25C. Nei topi, i tumori ingegnerizzati con CDC25C ridotta hanno mostrato livelli inferiori di questa proteina sia nelle misurazioni geniche sia proteiche, confermando che lo stesso effetto si verifica negli animali viventi.
Stress dei “centri energetici” e la squadra di pulizia della cellula
Osservando le cellule al microscopio elettronico, i ricercatori hanno visto che le cellule tumorali con CDC25C bassa contenevano mitocondri gonfi e danneggiati — i piccoli impianti energetici della cellula — insieme a strutture a bolla chiamate autofagosomi che indicano l’attivazione del sistema interno di riciclo della cellula, l’autofagia. Hanno poi misurato segnali chiave dello stress mitocondriale: i livelli di calcio e le specie reattive dell’ossigeno (ROS), entrambi elevati nelle cellule tumorali dopo la riduzione di CDC25C. Anche i marker della risposta allo stress mitocondriale, inclusi proteine helper come HSP60 e due enzimi mitocondriali di “controllo qualità”, sono aumentati, così come CHOP, un fattore legato allo stress che collega i problemi mitocondriali a risposte cellulari più ampie. Colpisce il fatto che questi segnali di stress si muovessero nella direzione opposta nelle cellule epatiche normali, rafforzando l’idea che cellule tumorali e cellule sane rispondono in modo molto diverso alla perdita di CDC25C.
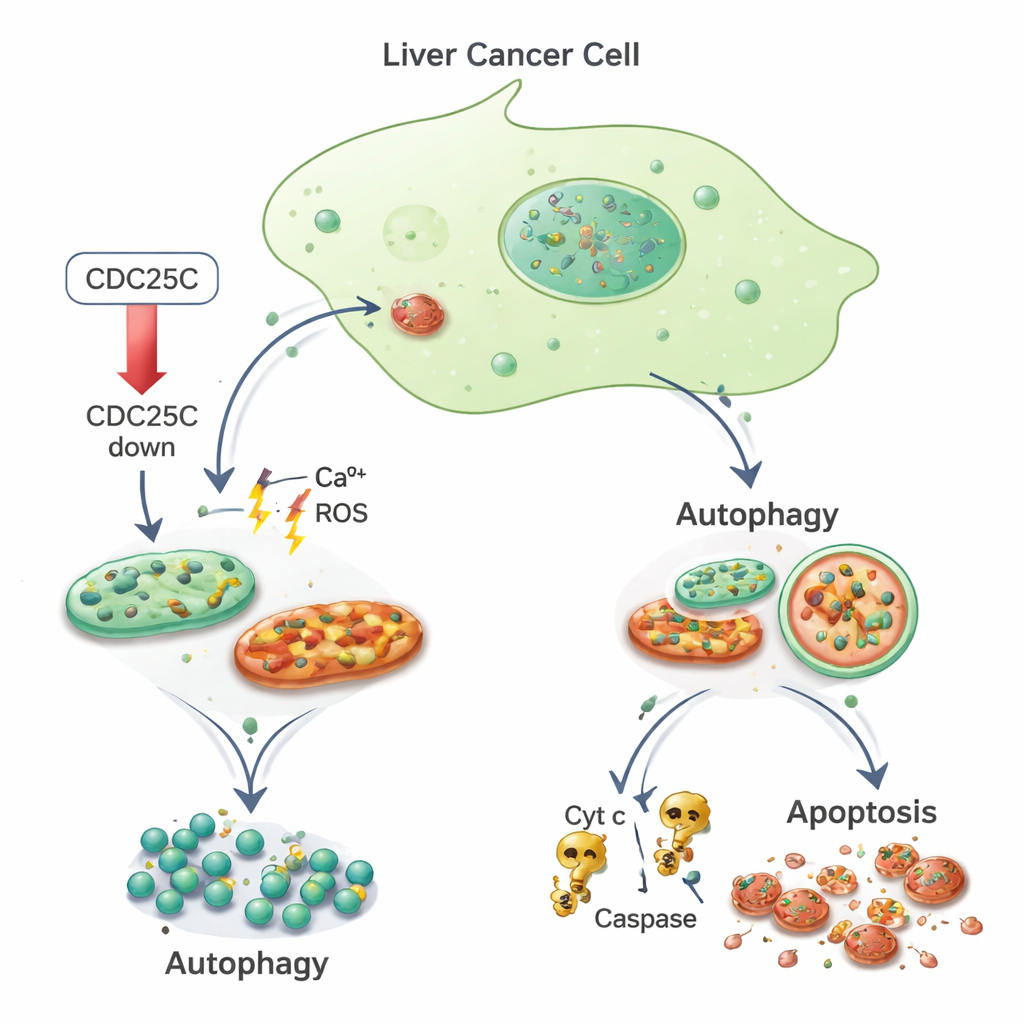
Dallo stress all’autodigestione e alla morte cellulare
Il gruppo ha poi indagato come queste cellule tumorali stressate stessero reagendo. Hanno riscontrato che i marker dell’autofagia aumentavano sia nelle cellule tumorali sia in quelle normali quando CDC25C veniva ridotta. Proteine come LC3 e p62, che riflettono la formazione e l’attività degli autofagosomi, sono aumentate, indicando che le cellule stavano potenziando la loro macchina di pulizia. Allo stesso tempo, solo nelle cellule tumorali il danno mitocondriale sembra spingere le cellule oltre la riparazione verso la morte programmata. Mediante colorazioni fluorescenti e citometria a flusso, i ricercatori hanno osservato più cellule tumorali con nuclei frammentati e intensamente colorati — un segno distintivo dell’apoptosi — e una ridotta potenziale di membrana mitocondriale. Hanno anche trovato livelli aumentati di citocromo c e degli enzimi Caspasi-3 e Caspasi-9, componenti classici della via di morte guidata dai mitocondri. Le cellule epatiche normali, al contrario, hanno mostrato meno apoptosi nelle stesse condizioni di riduzione di CDC25C.
Cosa potrebbe significare per i trattamenti futuri
Per un lettore non specialista, il messaggio chiave è che abbassare CDC25C sembra colpire le cellule del carcinoma epatocellulare nei loro punti deboli, sovraccaricando i loro “centri energetici”, spingendo i sistemi di riciclo oltre misura e infine innescando un’autodistruzione pulita — risparmiando per lo più le cellule epatiche normali. Gli autori concludono che CDC25C è più di un semplice interruttore di crescita; modula anche il modo in cui le cellule gestiscono stress, pulizia e morte. Poiché le cellule tumorali dipendono fortemente da CDC25C e rispondono alla sua perdita con stress mitocondriale fatale e apoptosi, farmaci che prendono di mira questa proteina, o le vie di stress a essa correlate, potrebbero un giorno offrire un modo più selettivo per trattare il cancro al fegato con meno danni al tessuto epatico sano.
Citazione: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Parole chiave: carcinoma epatocellulare, CDC25C, stress mitocondriale, autofagia, apoptosi