Clear Sky Science · it
Superare la resistenza dei biofilm di Candida albicans ai farmaci tramite la sinergia azolo–sofrolipidi
Perché le infezioni fungine ostinate sono importanti
Chiunque abbia avuto un’infezione da lievito persistente, un catetere centrale in ospedale o un impianto medico è potenzialmente a rischio per Candida albicans, un fungo comune che può diventare pericoloso quando forma comunità difficili da trattare chiamate biofilm. Questi strati vischiosi proteggono i microrganismi da molti dei nostri migliori antifungini, permettendo alle infezioni di persistere e talvolta diventare pericolose per la vita. Lo studio descritto qui cerca un nuovo modo per infrangere queste difese accoppiando farmaci esistenti con una molecola naturale simile a un sapone prodotta da lieviti.
Uno scudo nascosto sulle superfici mediche
Candida albicans può aderire ai tessuti e ai dispositivi medici e poi accumularsi in biofilm strutturati—strati densi di cellule tenute insieme da una matrice autoprodotta di zuccheri, proteine e DNA. All’interno di questa fortezza il fungo rallenta il suo metabolismo e espelle i farmaci, quindi i medicinali che uccidono facilmente le cellule libere hanno scarso effetto su quelle che vivono nel biofilm. Gli azoli, come il fluconazolo e l’itraconazolo, sono pilastri della terapia antifungina, ma contro biofilm maturi spesso richiedono dosi molto maggiori, che possono causare effetti collaterali e comunque non riuscire a eliminare completamente l’infezione. I medici si confrontano sempre più con infezioni basate su biofilm e resistenti, sottolineando l’esigenza di molecole ausiliarie in grado di indebolire il biofilm stesso.
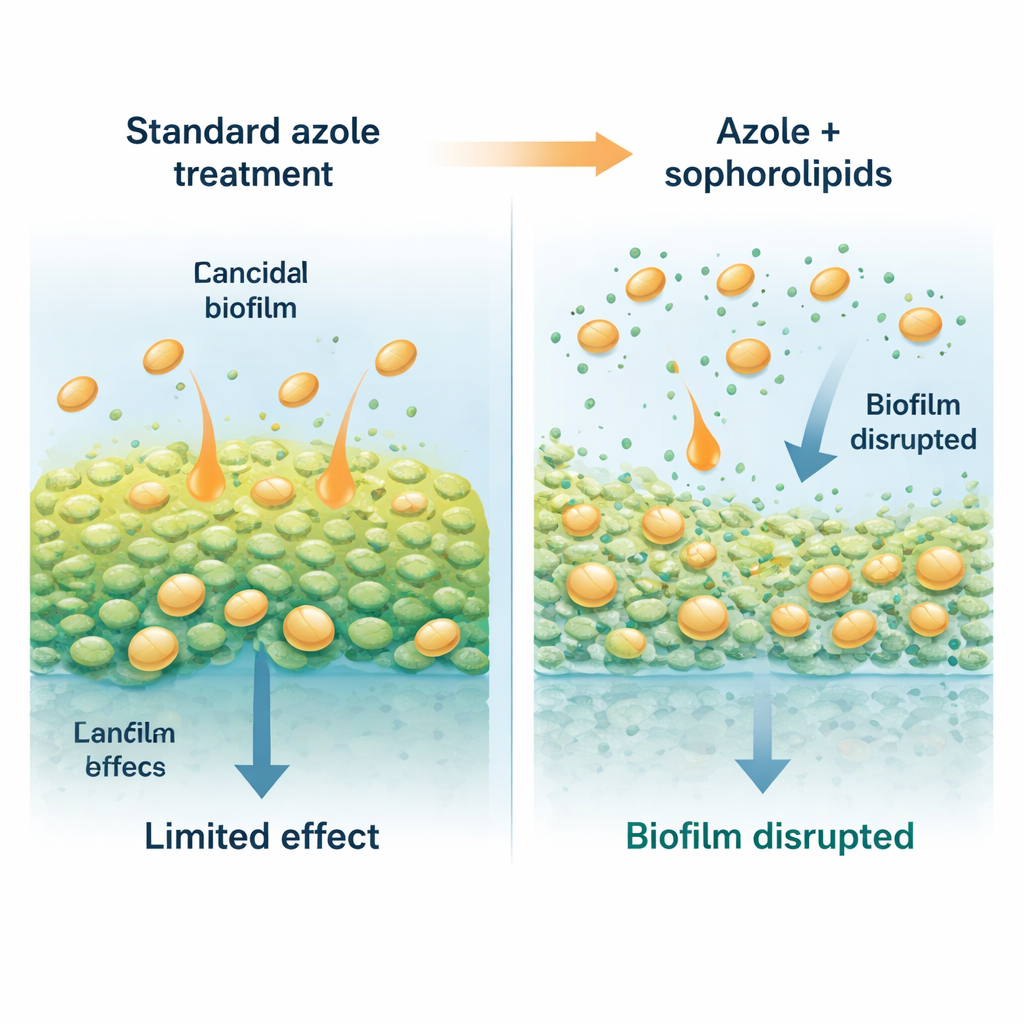
Aiutanti simili a saponi da un lievito amichevole
I ricercatori si sono rivolti ai sofrolipidi, tensioattivi naturali e biodegradabili—molecole che agiscono un po’ come detergenti molto delicati—prodotti da certi lieviti non patogeni. Queste molecole hanno una testa zuccherina idrofila e una coda oleosa, che permette loro di posizionarsi sulle superfici e alle interfacce. In questo studio è stato utilizzato un lievito chiamato Starmerella riodocensis per produrre una miscela di sofrolipidi, poi purificata e analizzata. Da soli, questi sofrolipidi non uccidevano le cellule di Candida in sospensione nemmeno a dosi elevate, ma interferivano fortemente con la capacità del fungo di formare e mantenere i biofilm. I biofilm giovani, in fase di formazione, erano particolarmente sensibili, e anche biofilm consolidati di 24 ore potevano essere assottigliati e indeboliti quando esposti a sofrolipidi purificati.
Collaborare con antifungini già in uso
La domanda centrale era se i sofrolipidi potessero migliorare l’efficacia degli azoli standard. Il team ha testato combinazioni di sofrolipidi con tre azoli ampiamente usati: fluconazolo, itraconazolo e ketoconazolo. Quando hanno esposto i biofilm a queste miscele, hanno scoperto che alcune coppie facevano più che sommare i loro effetti—agivano in sinergia, cioè la combinazione era più potente di quanto ci si attenderebbe dai singoli componenti. La partnership più efficace è stata itraconazolo più sofrolipidi. Contro biofilm difficili e già formati, la quantità di itraconazolo necessaria per dimezzare il biofilm è diminuita fino a sedici volte, mentre anche la dose di sofrolipidi richiesta è calata di diversi fattori rispetto all’uso dei soli sofrolipidi. Le combinazioni con fluconazolo e ketoconazolo hanno mostrato miglioramenti più modesti, suggerendo che la natura chimica di ciascun farmaco influisce su quanto benefici dall’“aiuto” del tensioattivo.
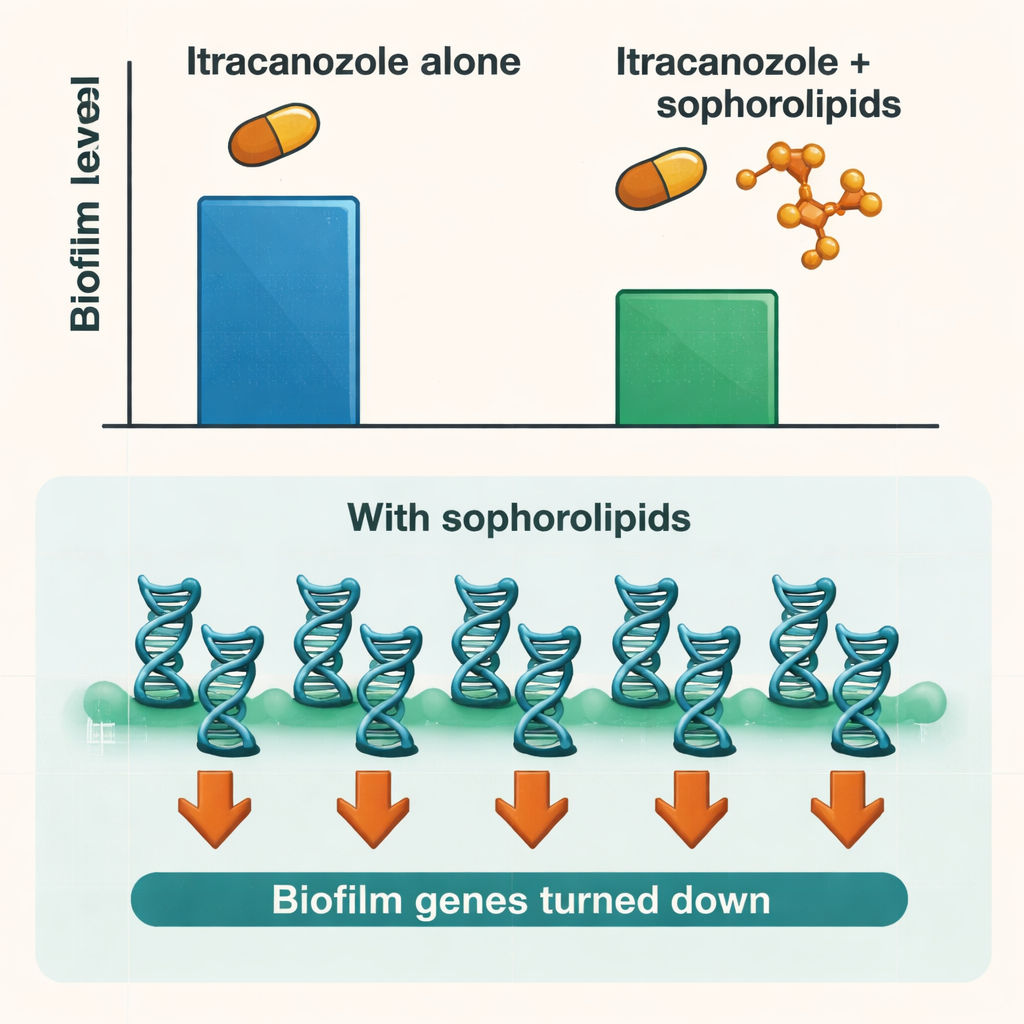
Spegnere il programma biofilm del fungo
Per capire cosa accadeva all’interno delle cellule fungine, i ricercatori hanno esaminato l’attività di geni chiave di Candida coinvolti nell’adesione alle superfici, nella crescita filamentosa e nella costruzione della matrice del biofilm. Il trattamento con i sofrolipidi da soli ha ridotto l’espressione di molti di questi geni, in particolare quelli che controllano i primi passi dell’adesione e il passaggio dalla forma simile al lievito a quella filamentosa. Quando le cellule erano sincronizzate in una fase specifica del ciclo cellulare che favorisce la formazione del biofilm, gli effetti di silenziamento genico erano ancora più marcati. Ciò suggerisce che i sofrolipidi non si limitano a rimuovere il biofilm; interferiscono anche con il programma biologico del fungo per costruire e mantenere la sua comunità protettiva.
Promessa per terapie più efficaci e più miti
Lo studio conclude che i sofrolipidi di Starmerella riodocensis possono agire come partner sicuri e mirati ai biofilm per gli azoli, con la combinazione itraconazolo–sofrolipidi particolarmente potente. Poiché i sofrolipidi mostrano bassa tossicità nelle cellule dei mammiferi e indeboliscono principalmente la struttura del biofilm e le reti geniche piuttosto che avvelenare direttamente il fungo, potrebbero permettere ai medici di usare dosi più basse di farmaci convenzionali pur eliminando infezioni ostinate su dispositivi e tessuti. Per i pazienti, questo tipo di terapia combinata intelligente potrebbe un giorno tradursi in trattamenti sia più efficaci contro i biofilm resistenti di Candida sia più gentili per il resto dell’organismo.
Citazione: Jayasekara, L.C.B., Watchaputi, K., Butkinaree, C. et al. Overcoming Candida albicans biofilm drug resistance via azole-sophorolipid synergy. Sci Rep 16, 5963 (2026). https://doi.org/10.1038/s41598-026-36278-8
Parole chiave: biofilm di Candida, antifungini azolici, sofrolipidi, sinergia farmacologica, resistenza antimicrobica