Clear Sky Science · it
Diversità genetica nell'antigene candidato vaccinale PfCyRPA per la fase ematica di Plasmodium falciparum in Senegal
Perché questo studio sulla malaria è importante
La malaria continua a uccidere centinaia di migliaia di persone ogni anno, la maggior parte in Africa e molti di loro bambini. I vaccini attualmente in fase di distribuzione salvano vite, ma la loro protezione diminuisce nel tempo e non è completa. Questo studio esamina un nuovo bersaglio vaccinale che il parassita della malaria usa per entrare nei globuli rossi. Valutando quanto questo bersaglio vari nelle infezioni reali in Senegal, i ricercatori pongono una domanda cruciale per i vaccini futuri: si tratta di un “tallone d’Achille” stabile del parassita o di un bersaglio che cambia?
Un nuovo punto debole sul parassita
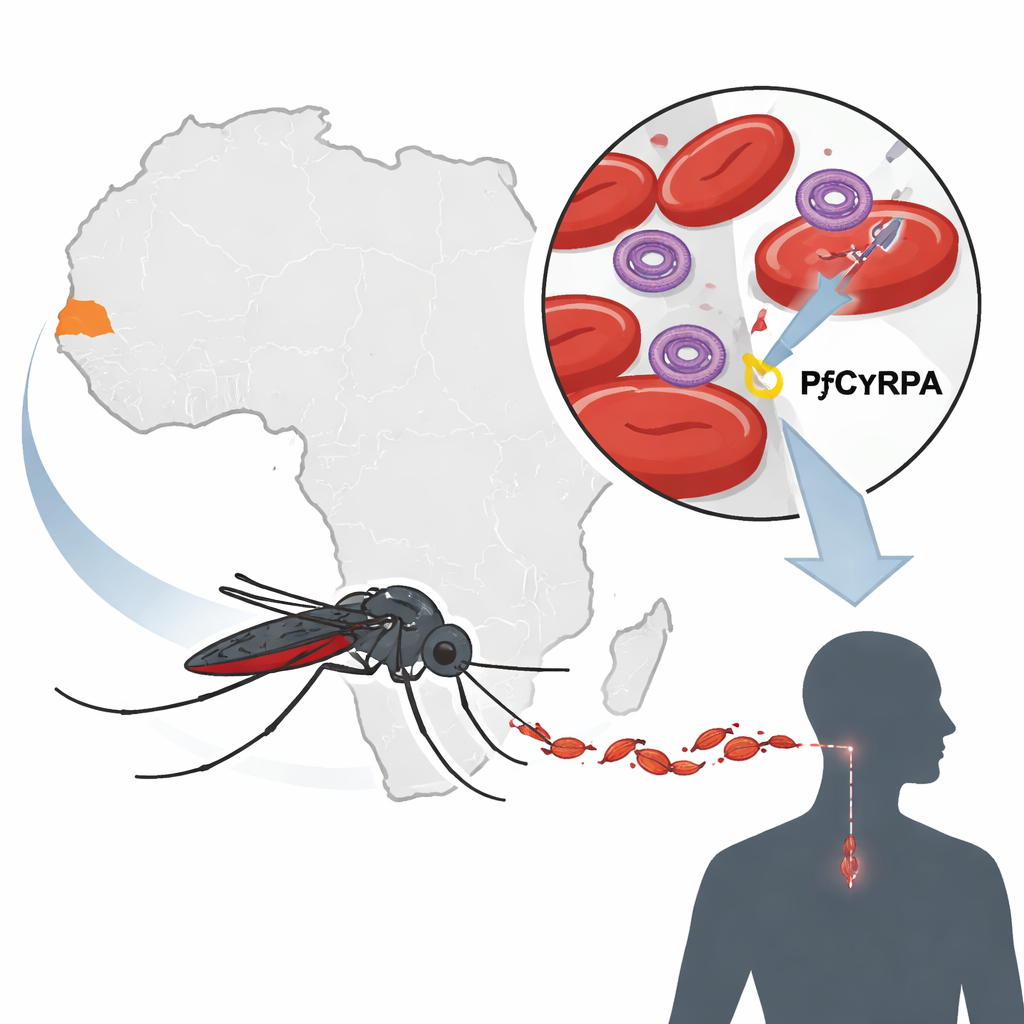
Quando i parassiti della malaria invadono il flusso sanguigno, devono penetrare nei globuli rossi per moltiplicarsi. Per farlo usano un piccolo insieme di proteine che si ancorano alla superficie della cellula, come una chiave nella serratura. Una di queste proteine, chiamata PfCyRPA, agisce insieme a PfRh5 e PfRipr in un complesso d'invasione strettamente collegato. Poiché i parassiti non possono invadere senza questo complesso, e perché PfCyRPA sembra variare poco tra ceppi diversi, è diventata una candidata di primo piano per i vaccini di nuova generazione per la fase ematica, attualmente in trial clinici iniziali. Un vaccino che prende di mira una proteina così essenziale e stabile potrebbe bloccare la malattia attraverso molti ceppi di parassiti e regioni diverse.
Uno scatto genetico in Senegal
Per capire quanto questa proteina sia davvero stabile in natura, il team ha studiato 93 infezioni malariche in pazienti di Kédougou, una regione nel sud-est del Senegal con trasmissione stagionale intensa. Molti pazienti ospitavano più ceppi di parassita contemporaneamente, il che rende difficile individuare cambiamenti genetici rari. Per superare questo limite, i ricercatori hanno usato il deep sequencing, un metodo ad alta produttività che legge il gene PfCyRPA migliaia di volte per campione e può rilevare varianti anche a bassa frequenza. Hanno quindi confrontato ogni sequenza con il ceppo di laboratorio di riferimento, noto come 3D7, e hanno catalogato le sostituzioni di singole lettere del DNA che alterano i mattoni proteici.
Poche variazioni e per lo più rare
I risultati mostrano che la versione di riferimento di PfCyRPA domina in questa popolazione di parassiti: circa il 72% delle infezioni portava soltanto la forma standard del gene. Complessivamente, gli scienziati hanno trovato appena 15 mutazioni distinte che cambiano la proteina, e due terzi di esse sono apparse in una sola infezione ciascuna. Solo una variazione, chiamata V292F, ha raggiunto quasi il 10% delle infezioni. Misurando quanto spesso ciascuna mutazione appariva tra i numerosi genomi di parassiti all'interno di un singolo paziente, hanno mostrato che la maggior parte di queste varianti era presente ad alta frequenza nelle infezioni in cui si trovava. Ciò suggerisce che, quando una variante emerge, può diventare la versione dominante all'interno di quell'infezione—ma tali varianti rimangono comunque poco comuni nella comunità.
Cosa rivela la struttura sulla funzione
Le differenze genetiche contano per i vaccini solo se modificano il modo in cui la proteina si ripiega, come funziona o come gli anticorpi la riconoscono. Per esplorare questo aspetto, il team ha utilizzato strutture 3D di PfCyRPA legata al partner PfRh5 e a diversi anticorpi umani. Hanno «inserito» ciascuna mutazione su queste strutture e impiegato strumenti computazionali per prevederne gli effetti su forma, stabilità e legame. La maggior parte delle mutazioni è stata prevista avere solo conseguenze minori sulla forma complessiva di PfCyRPA o sui suoi contatti con PfRh5 e gli anticorpi noti. Alcune variazioni, come D236V e N270T, potrebbero influenzare sottilmente flessibilità o stabilità interrompendo legami a idrogeno o creando piccoli clash nella proteina. Altre, incluse R50C e F187L, si trovano vicino all'area di contatto con PfRh5 e potrebbero modificare tale interazione. Un piccolo gruppo di mutazioni giace in prossimità di regioni dove tendono a legarsi anticorpi fortemente neutralizzanti, ma anche lì gli effetti previsti sul riconoscimento da parte degli anticorpi erano lievi.
Cosa significa per i vaccini futuri
Per i non specialisti, il messaggio chiave è che questa proteina cruciale del parassita appare notevolmente stabile in un contesto reale ad alta trasmissione: la maggior parte dei parassiti porta la stessa versione, e le varianti rare che si riscontrano sono previste modificare solo leggermente il comportamento della proteina o il modo in cui gli anticorpi vi si legano. Questo rende PfCyRPA un bersaglio promettente per vaccini antimalarici durevoli. Allo stesso tempo, il lavoro mette in evidenza un piccolo numero di variazioni rare che, in linea teorica, potrebbero conferire un vantaggio al parassita sotto la pressione vaccinale. Individuare ora questi siti permette agli scienziati di progettare candidati vaccinali e test di laboratorio che li tengano presenti, contribuendo a garantire che i vaccini per la fase ematica del domani rimangano efficaci anche mentre il parassita continua a evolversi.
Citazione: Ba, A., Thiam, L.G., Pouye, M.N. et al. Genetic diversity in the Plasmodium falciparum next-generation blood stage vaccine candidate antigen PfCyRPA in Senegal. Sci Rep 16, 5661 (2026). https://doi.org/10.1038/s41598-026-36257-z
Parole chiave: vaccini contro la malaria, Plasmodium falciparum, PfCyRPA, diversità genetica, Senegal