Clear Sky Science · it
Sorveglianza genomica nazionale di Klebsiella pneumoniae resistente a carbapenemi e colistina isolata da sangue in Thailandia (2020–2024)
In aumento le infezioni ematiche letali
Gli ospedali di tutto il mondo affrontano una tendenza preoccupante: batteri comuni che una volta si piegavano ai nostri antibiotici più potenti stanno diventando quasi impossibili da trattare. Questo studio si concentra su Klebsiella pneumoniae, un microbo che può invadere il torrente ematico e causare infezioni potenzialmente fatali, e traccia come si è evoluto in tutta la Thailandia per resistere anche ai farmaci di ultima istanza. Comprendere dove si diffondono questi super-batteri e come eludono i medicinali è cruciale per proteggere i pazienti, orientare le scelte dei medici e definire politiche di sanità pubblica.
Tracciare un super-batterio ospedaliero attraverso una nazione
I ricercatori hanno analizzato 227 campioni di Klebsiella pneumoniae prelevati dal sangue di pazienti in ospedali thailandesi tra il 2020 e il 2024. Questi campioni provenivano da una rete nazionale di sorveglianza che raccoglie routinariamente dati sulle infezioni resistenti ai farmaci. I test di laboratorio hanno mostrato che oltre il 93% di questi isolati ematici erano resistenti ai carbapenemi, una potente classe di antibiotici spesso usata quando altri farmaci falliscono. Preoccupante è che quasi un terzo degli isolati resistenti ai carbapenemi era anche resistente alla colistina, una delle ultime opzioni a cui i medici ricorrono quando tutto il resto non funziona. Abbinando i test farmacologici standard al sequenziamento dell’intero genoma, il team ha potuto vedere non solo quali farmaci fallivano, ma anche quali stratagemmi genetici i batteri usavano per sopravvivere.
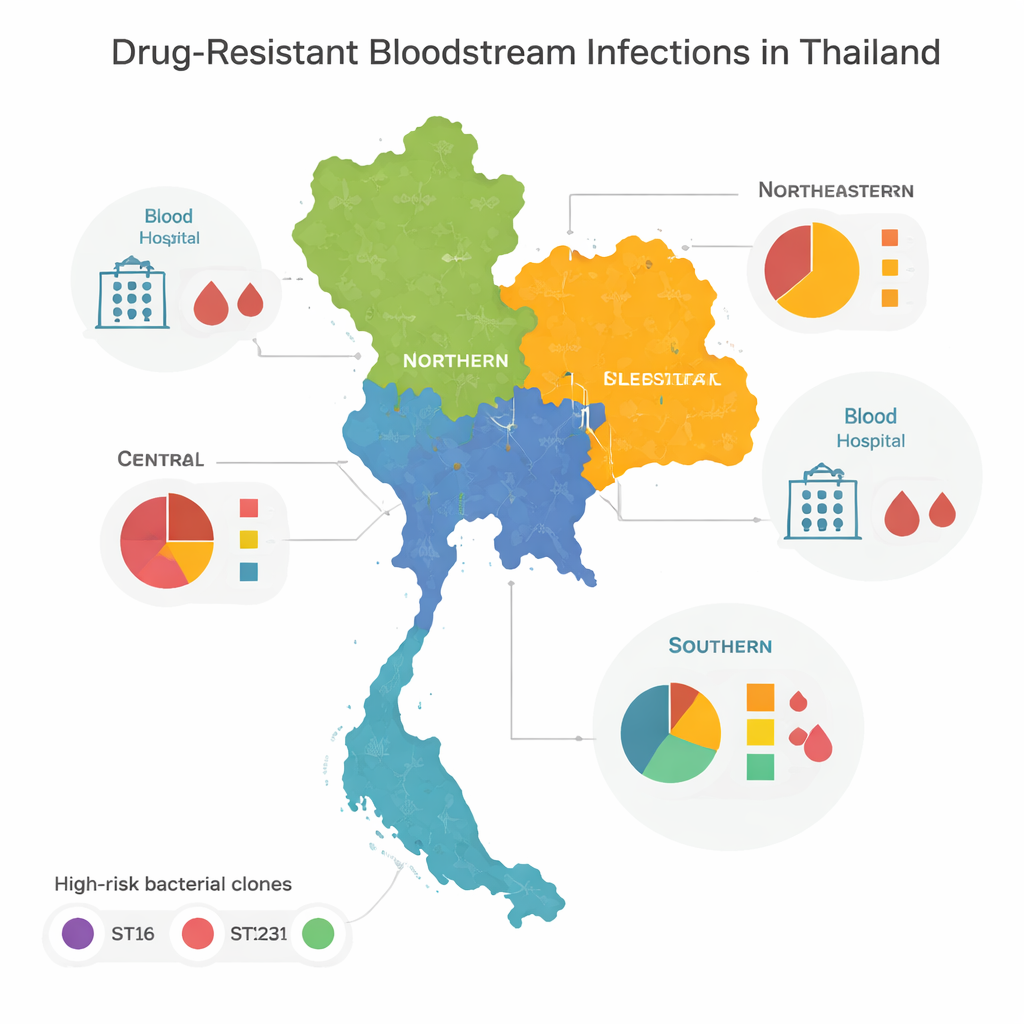
Cloni ad alto rischio e pattern regionali
Confrontando i genomi, il team ha scoperto che la maggior parte dei batteri resistenti apparteneva a poche famiglie «ad alto rischio», o cloni, note a livello globale per causare focolai ospedalieri. Tre in particolare—denominati ST16, ST147 e ST231—dominavano rispettivamente nel centro, nel nord e nel nord-est della Thailandia. Questi cloni si erano diffusi ampiamente tra le regioni, suggerendo frequenti spostamenti di pazienti, personale o batteri tra gli ospedali. Il Sud del paese appariva diverso: invece di essere dominato da pochi tipi, ospitava una grande varietà di lignaggi batterici, molti osservati una sola volta. Questa diversità suggerisce un mix più complesso di focolai locali, fonti ambientali e movimenti transfrontalieri piuttosto che uno o due cloni fuori controllo.
Come i batteri eludono gli antibiotici
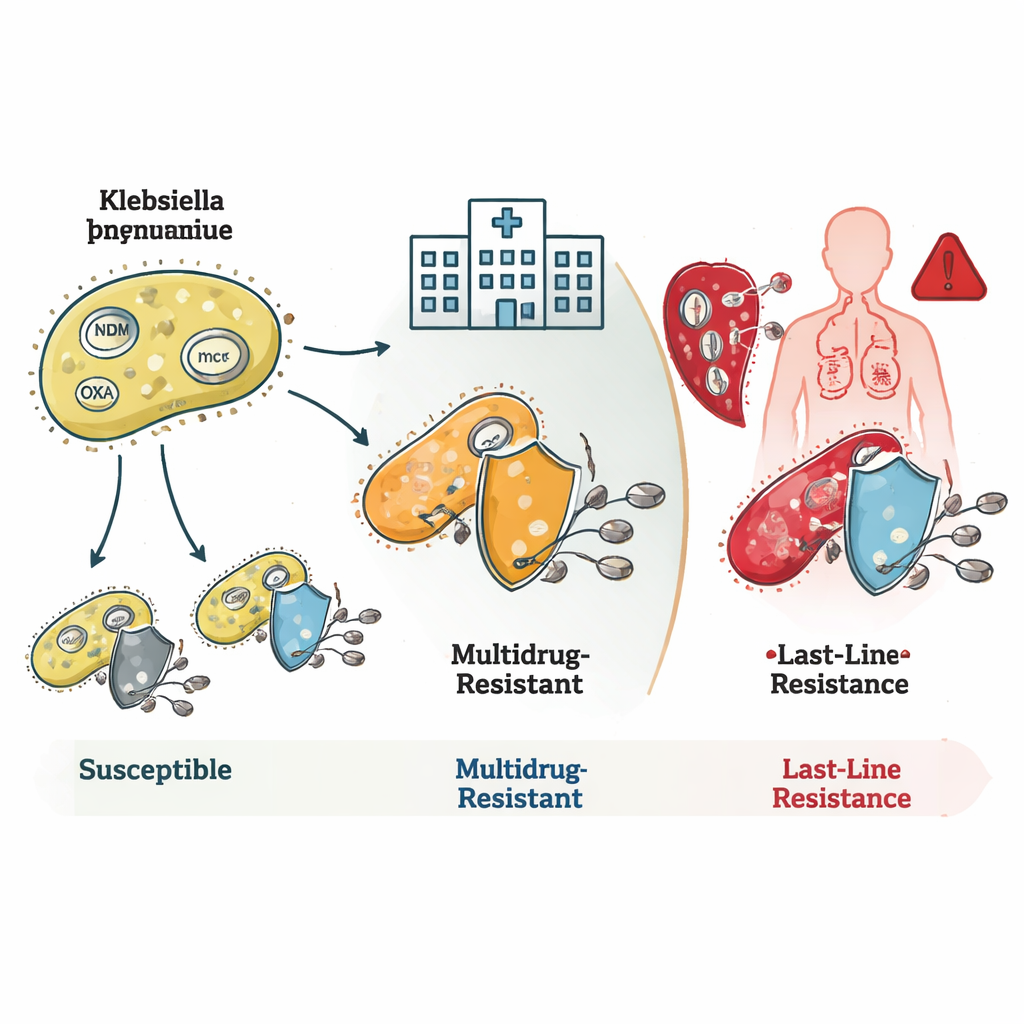
Lo studio ha rivelato come questi batteri accumulino molteplici meccanismi di resistenza. Molti ceppi ST16 e ST231 portavano geni noti come blaNDM e blaOXA, che codificano enzimi capaci di degradare i carbapenemi prima che possano agire. Alcuni presentavano anche modifiche nella membrana esterna che riducono l’ingresso dei farmaci, combinando più strategie per creare resistenze di livello molto elevato. I ceppi ST231 spesso portavano un gene aggiuntivo, rmtF1, che inattiva un gruppo importante di farmaci chiamati aminoglicosidi, restringendo ulteriormente le opzioni terapeutiche. ST147 si distingueva per la sua flessibilità genetica: mescolava e combinava diversi geni di resistenza e plasmidi—anelli di DNA mobili—facendone un potenziale hub per la diffusione di tratti di resistenza ad altri batteri.
Fallimenti dell’ultima linea e pericoli nascosti
La scoperta più allarmante riguardava la resistenza alla colistina, un farmaco che i medici riservano per situazioni disperate. Alcune famiglie batteriche rare portavano geni mcr, che possono saltare tra specie su plasmidi e causare direttamente resistenza alla colistina. Altre, in particolare all’interno del clone ST16, erano resistenti alla colistina pur non presentando alcun gene o mutazione di resistenza conosciuta. Ciò suggerisce che gli scienziati non hanno ancora mappato completamente tutte le vie con cui i batteri possono neutralizzare questo farmaco di ultima istanza. Il team ha anche identificato ceppi ipervirali—batteri particolarmente aggressivi nel causare malattia—incluso un lignaggio che combinava alta virulenza con resistenza a tutti i carbapenemi testati, una combinazione particolarmente pericolosa.
Perché la sorveglianza genomica è importante
Per capire come le modifiche genetiche si traducessero in fallimenti terapeutici nel mondo reale, i ricercatori hanno usato modelli statistici per collegare specifici geni di resistenza ai risultati dei test di laboratorio. Geni come blaNDM-1 e suoi parenti stretti hanno mostrato associazioni estremamente robuste con la resistenza ai carbapenemi, confermandone il ruolo centrale nel guidare il fallimento terapeutico. Tuttavia, per la colistina, la maggior parte dei batteri resistenti non aveva marcatori di resistenza riconosciuti, indicando meccanismi nascosti ancora da scoprire. Gli autori sostengono che l’uso routinario del sequenziamento dell’intero genoma nella sorveglianza ospedaliera può funzionare come un radar di allerta precoce, individuando i cloni ad alto rischio emergenti, tracciandone lo spostamento attraverso regioni e confini e guidando risposte rapide di controllo delle infezioni.
Cosa significa per i pazienti e per le politiche
Per il pubblico, il messaggio è netto ma chiaro: alcune infezioni ematiche in Thailandia sono ormai causate da batteri che resistono a quasi tutti i farmaci a disposizione dei medici, e poche famiglie pericolose di questi microbi si stanno diffondendo ampiamente. Allo stesso tempo, lo studio dimostra che con gli strumenti giusti—campionamento nazionale, analisi genetica e condivisione rapida dei dati—i sistemi sanitari possono prevedere queste minacce e adattarsi. Ampliare la sorveglianza genomica, sviluppare test molecolari rapidi e rafforzare il controllo delle infezioni potrebbe contribuire a rallentare l’avanzata di questi super-batteri e a guadagnare tempo per lo sviluppo di nuovi trattamenti e vaccini.
Citazione: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Parole chiave: resistenza antimicrobica, Klebsiella pneumoniae, infezione del flusso sanguigno, sorveglianza genomica, assistenza sanitaria in Thailandia