Clear Sky Science · it
Dye a base di distirrilo-BODIPY sostituiti con piridinio e bromo per la fototerapia mirata ai mitocondri
Illuminare le cellule tumorali dall’interno
La fototerapia fotodinamica è un trattamento oncologico che utilizza farmaci attivabili con la luce per uccidere le cellule tumorali preservando in gran parte i tessuti sani. Questo studio esplora una nuova famiglia di coloranti fluorescenti progettati per indirizzarsi verso le centrali energetiche della cellula — i mitocondri — e, quando illuminati con luce rosso‑profonda, generare specie ossidanti che possono distruggere le cellule cancerose. Il lavoro mette in luce sia le potenzialità sia i limiti dell’ingegnerizzazione di tali coloranti a livello molecolare.
Perché prendere di mira le centrali energetiche della cellula?
I mitocondri sono fondamentali per la produzione di energia e contribuiscono a decidere se una cellula sopravvive o muore. Le cellule tumorali tendono ad avere una membrana mitocondriale più fortemente polarizzata rispetto alle cellule normali, il che le porta ad attrarre molecole cariche positivamente in misura maggiore. I ricercatori hanno sfruttato questa caratteristica legando un gruppo piridinio caricata positivamente a uno scaffold fluorescente noto, il BODIPY. Questa progettazione aiuta a indirizzare i coloranti verso i mitocondri, dove reazioni chimiche indotte dalla luce possono infliggere il massimo danno alle cellule tumorali limitando gli effetti collaterali altrove.
Progettare coloranti fotoattivati più intelligenti
Il team ha creato tre coloranti strettamente imparentati, chiamati PyBHI, PyBMI e PyBBrI, che differiscono principalmente per il numero di atomi di bromo presenti (nessuno, uno o due). Tutti condividono una struttura lunga ed estesa che sposta l’assorbimento e l’emissione verso il vicino infrarosso — una finestra utile in cui la luce può penetrare più in profondità nei tessuti. In teoria, questi coloranti potrebbero usare due diversi percorsi interni per raggiungere uno stato eccitato tripletto che produce ossigeno singoletto reattivo: uno favorito dagli atomi pesanti del bromo e un altro indotto da uno spostamento temporaneo di carica all’interno della molecola. 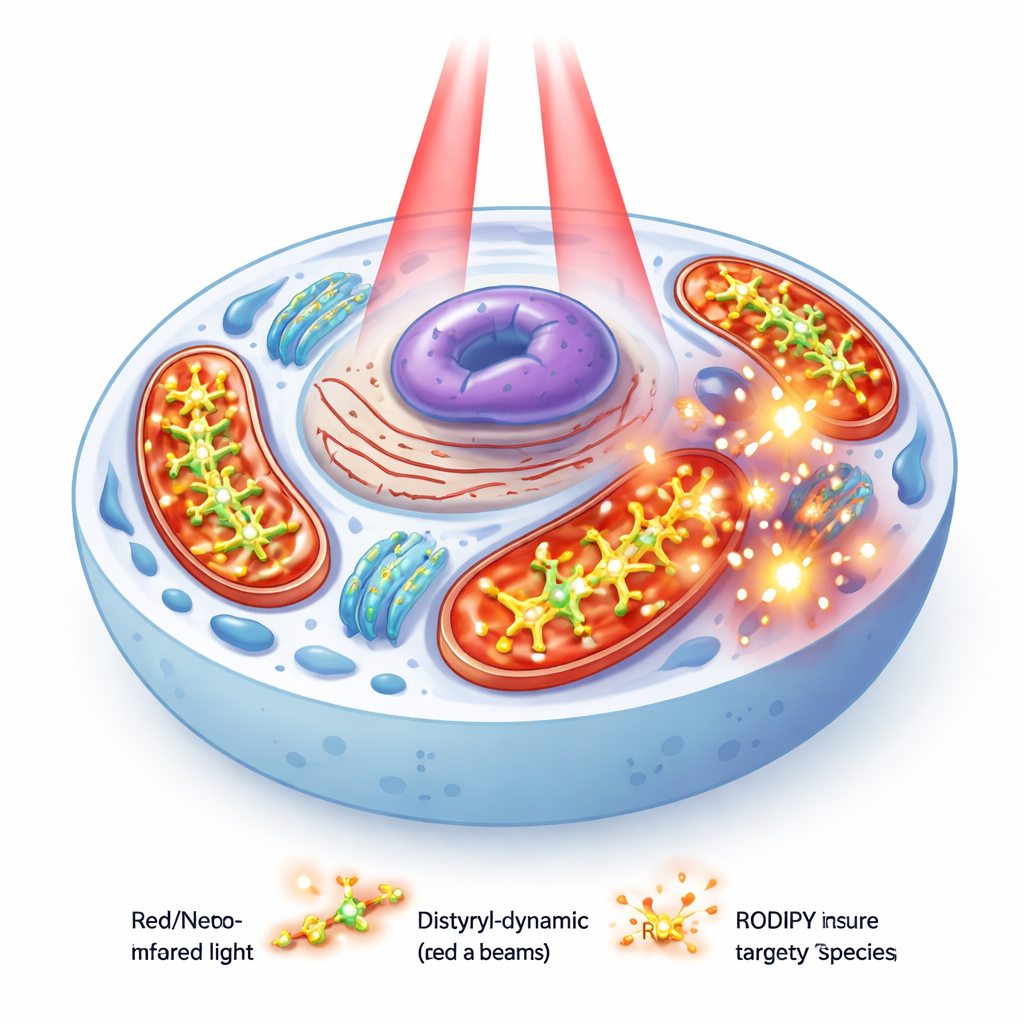
Quando la teoria incontra la realtà sperimentale
Nonostante il progetto elegante, i test dettagliati hanno mostrato che i coloranti non generano ossigeno singoletto con l’efficienza sperata. Usando sonde chimiche che perdono colore reagendo con l’ossigeno singoletto, i ricercatori hanno misurato rese di generazione di ossigeno molto basse per tutti e tre i coloranti, con solo un modesto miglioramento all’aumentare del numero di atomi di bromo. Esperimenti con laser ultraveloci hanno rivelato il perché: dopo l’assorbimento della luce, i coloranti entrano rapidamente in stati a carica spostata che si rilassano per lo più in modo innocuo sotto forma di calore invece di convertirsi nello stato tripletto desiderato. Nelle versioni brominate, gli atomi pesanti aprono comunque una via verso lo stato tripletto, ma questo percorso è molto più lento rispetto alle perdite energetiche concorrenti, limitando l’efficienza complessiva.
Mirare ai mitocondri tumorali nelle cellule vive
La situazione cambia in un contesto biologico. In cellule tumorali umane coltivate di mammella (MCF-7) e cervicali (HeLa), tutti e tre i coloranti sono risultati, tramite microscopia confocale, accumularsi fortemente nei mitocondri, co‑localizzandosi con un marcatore mitocondriale standard. I test di tossicità al buio hanno indicato che i coloranti sono per lo più innocui senza esposizione alla luce. Sotto irradiazione con luce rossa, tuttavia, il colorante dibrominato PyBBrI ha causato una consistente morte delle cellule tumorali, con dosi nell’ordine dei nanomolari che dimezzavano la vitalità cellulare. Gli altri due coloranti sono risultati molto meno efficaci. 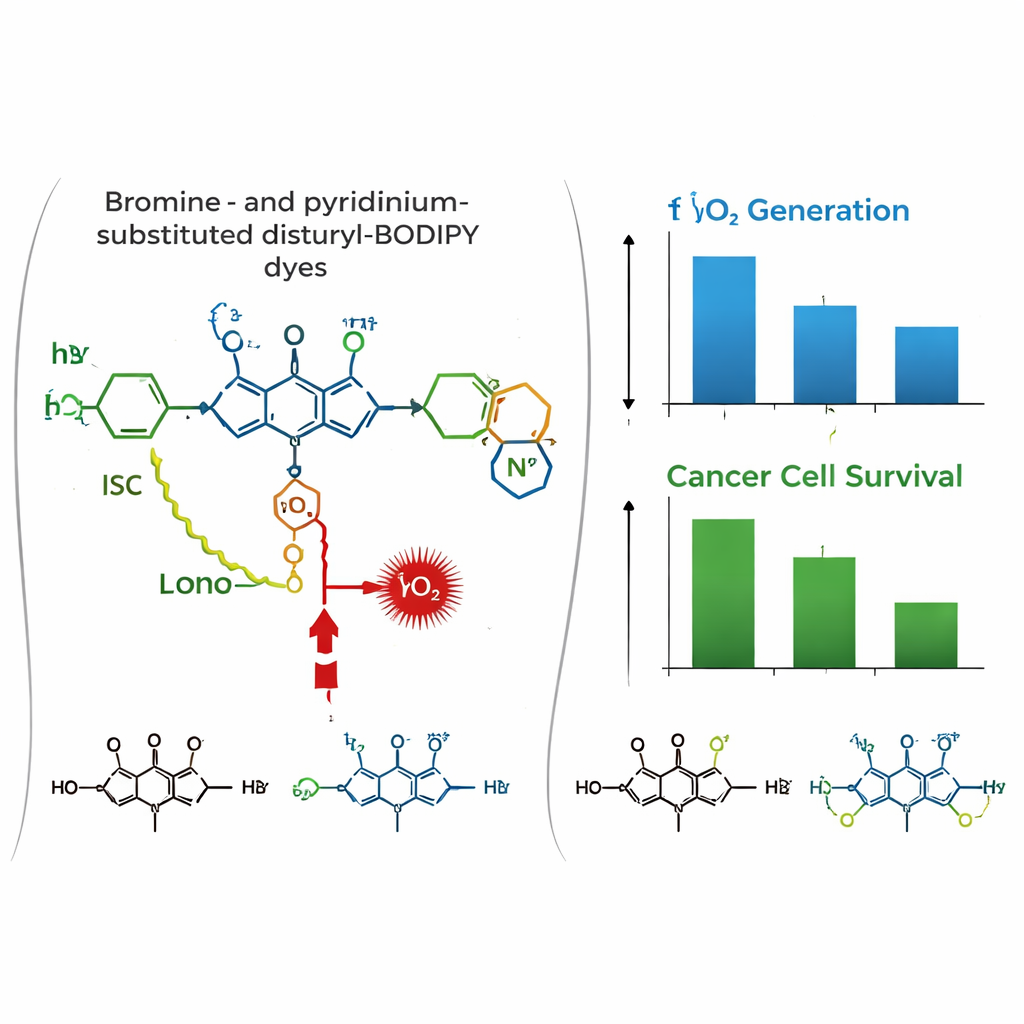
Cosa significa per le terapie oncologiche future
Per un lettore non specialista, il messaggio principale è che piccoli ritocchi chimici possono cambiare radicalmente il comportamento dei farmaci fototattivi e che le loro prestazioni nelle cellule reali possono essere migliori — o peggiori — rispetto alle previsioni basate su misure di base. In questo caso, il colorante più modificato, PyBBrI, ha mostrato solo una produzione modesta di ossigeno reattivo in provetta ma si è rivelato altamente potente contro le cellule tumorali una volta raggiunti i loro mitocondri. Il lavoro sottolinea sia l’importanza di indirizzare i farmaci verso strutture vulnerabili all’interno delle cellule tumorali sia la complessità nel prevedere l’efficienza fotodinamica. Indica la strada verso terapie di nuova generazione mirate ai mitocondri che usano luce nel vicino infrarosso per “attivare” selettivamente la chimica che uccide le cellule esattamente dove serve.
Citazione: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Parole chiave: fototerapia fotodinamica, coloranti mirati ai mitocondri, BODIPY, ossigeno singoletto, cellule tumorali