Clear Sky Science · it
La radiazione γ induce alterazioni subcellulari specifiche per regione dei marcatori della sclerosi laterale amiotrofica e della demenza frontotemporale nel cervello del suino
Perché piccole dosi di radiazione e cervelli di maiale contano
La maggior parte di noi considera la radiazione come qualcosa di puramente dannoso, soprattutto per il cervello. Eppure il nostro mondo è pervaso da bassi livelli di radiazione provenienti da esami medici, voli aerei e dall’ambiente. Nel frattempo, gli scienziati stanno ancora cercando di capire le cause della sclerosi laterale amiotrofica (SLA), la malattia mortale che paralizzò il campione di baseball Lou Gehrig, e della sua stretta cugina, la demenza frontotemporale (DFT), che colpisce comportamento e personalità. Questo studio pone una domanda sorprendentemente speranzosa: potrebbe una singola, modesta dose di radiazione gamma rimodellare sottilmente la chimica cerebrale in modi non interamente dannosi e magari anche protettivi contro i cambiamenti molecolari associati a SLA e DFT?
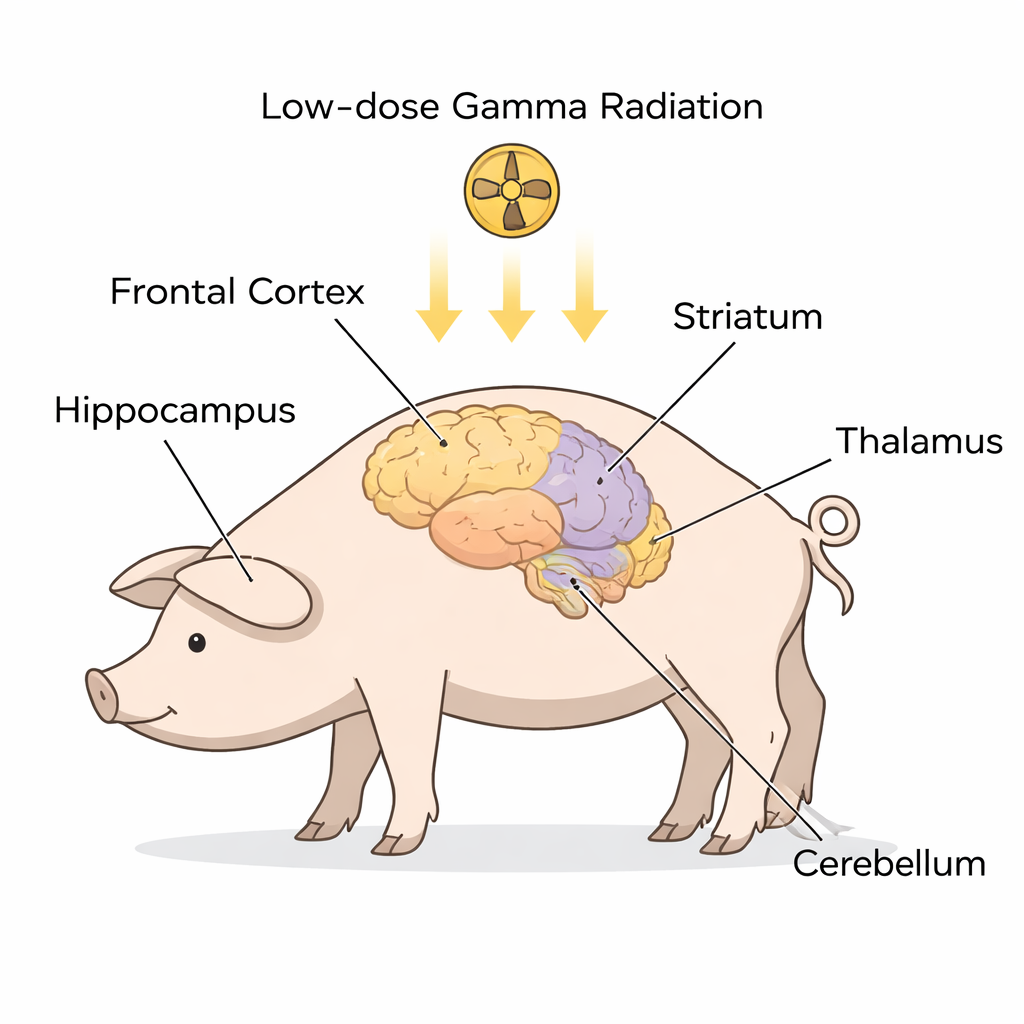
Uno sguardo più attento ai segnali di allarme della SLA nel cervello
Piuttosto che esaminare pazienti già affetti da SLA, i ricercatori hanno lavorato con miniporci Göttingen sani, i cui cervelli sono anatomicamente simili ai nostri. Nove animali hanno ricevuto un’esposizione corporea totale una tantum a radiazione gamma a basso dosaggio, mentre sei sono stati anestetizzati senza essere irradiati e hanno fatto da controlli. Circa un mese dopo, gli scienziati hanno dissezionato cinque regioni cerebrali chiave spesso implicate nella SLA e nella DFT — la corteccia frontale, l’ippocampo, lo striato, il talamo/ipotalamo e il cervelletto. In ciascuna regione hanno separato il contenuto cellulare in due compartimenti principali: il citoplasma (il fluido interno della cellula) e il nucleo (il compartimento che contiene il DNA). Utilizzando una tecnica chiamata Western blot, hanno misurato i livelli di diverse proteine fortemente legate a SLA e SLA‑DFT, tra cui SOD1, FUS, C9orf72, STMN2, ubiquitina, TDP‑43 e una forma modificata detta TDP‑43 fosforilato.
La radiazione lascia alcuni marcatori invariati — e altri spostati
Un risultato rassicurante è stato che i livelli totali di SOD1, una proteina le cui mutazioni causano alcune forme ereditarie di SLA, non sono cambiati in nessuna regione dopo la radiazione. Allo stesso modo, le principali forme di TDP‑43 — la proteina più spesso riscontrata negli ammassi cerebrali associati alla SLA — sono rimaste stabili sia nel nucleo sia nel citoplasma in tutte le regioni. Ma non tutto è rimasto immobile. Il team ha osservato spostamenti specifici per regione e per compartimento in diverse altre proteine. Per esempio, FUS, una proteina che normalmente risiede nel nucleo ma che in SLA può comportarsi in modo anomalo e aggregarsi, è diminuita nel citoplasma del talamo/ipotalamo dopo la radiazione, mentre i suoi livelli nucleari sono aumentati nella corteccia frontale e diminuiti nell’ippocampo. La proteina legata alla SLA C9orf72 non è cambiata nel fluido cellulare ma ha mostrato una diminuzione nei nuclei ippocampali. Anche STMN2, una proteina importante per il mantenimento delle fibre nervose, è calata nei nuclei ippocampali, suggerendo una risposta coordinata tra queste due molecole in quella regione correlata alla memoria.
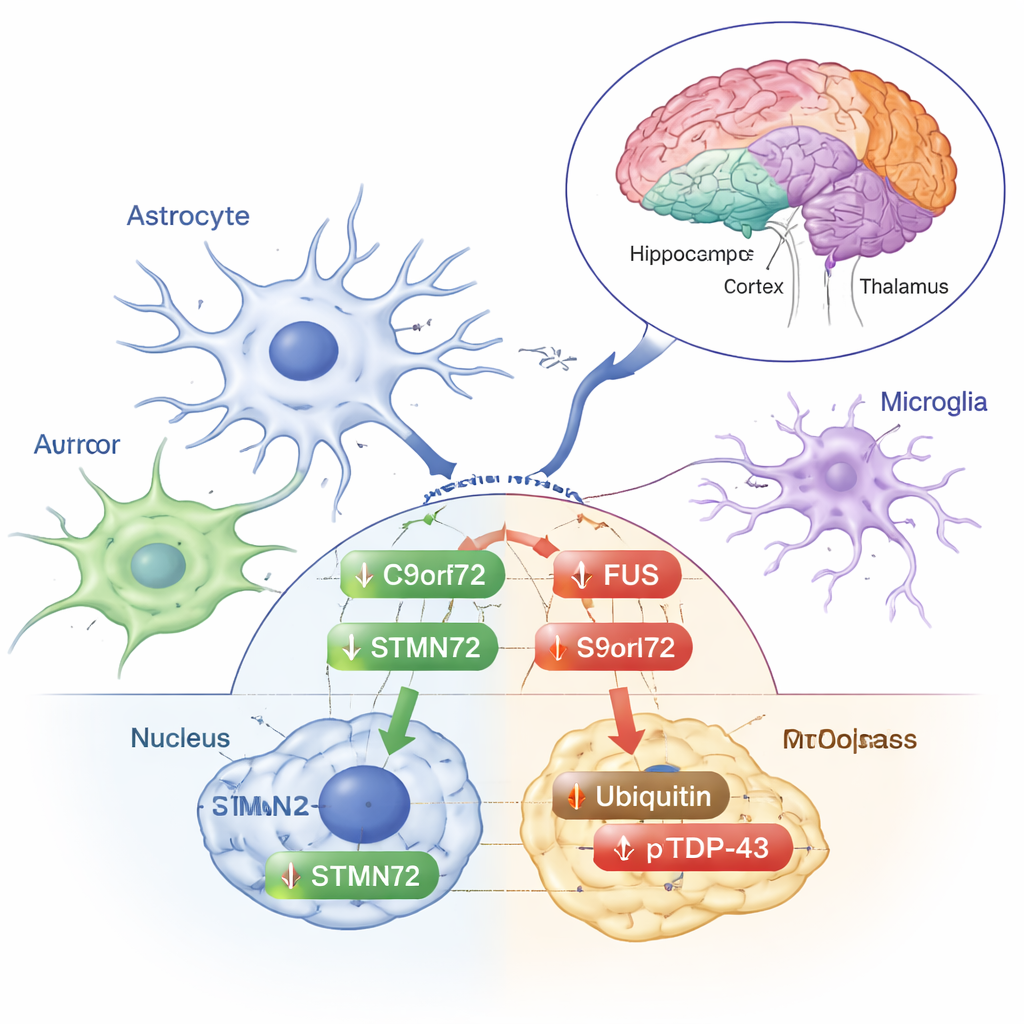
Segnali di stress o protezione precoce?
Altri cambiamenti somigliavano piuttosto a risposte classiche allo stress. L’ubiquitina — il piccolo marcatore che la cellula usa per etichettare le proteine danneggiate da smaltire — è aumentata nella frazione citoplasmatica della corteccia frontale. La forma fosforilata di TDP‑43, spesso arricchita nei depositi anomali osservati in SLA e DFT, è aumentata nel citoplasma della corteccia frontale, dello striato e del talamo/ipotalamo, anche se il TDP‑43 totale non è variato. Questi cambiamenti suggeriscono che la radiazione a basso dosaggio sollecita i meccanismi di gestione proteica del cervello senza innescare i pienamente sviluppati schemi di malripiegamento e aggregazione tipici della malattia. Gli autori sottolineano che queste risposte variano a seconda della regione cerebrale e del fatto che una proteina si trovi dentro o fuori dal nucleo, evidenziando quanto sia finemente tarata la reazione del cervello allo stress.
Cosa potrebbe significare per il rischio di SLA — e possibili benefici
Significa forse che la radiazione a basso dosaggio causa la SLA? I dati vanno contro una risposta semplice affermativa. I ricercatori non hanno osservato la caratteristica mislocalizzazione o accumulo delle principali proteine della SLA, e molti cambiamenti sembrano indicare una regolazione alterata piuttosto che un danno netto. In modo intrigante, questi risultati si allineano con studi precedenti dello stesso gruppo e di altri che suggeriscono che piccole quantità di radiazione possono talvolta scatenare l’“ormesi” — un fenomeno in cui uno stress lieve attiva vie di riparazione e riduce proteine dannose, come quelle legate ad Alzheimer o Parkinson, in modelli animali. Lo studio attuale suggerisce che, almeno a breve termine, una singola bassa dose di radiazione gamma rimodella i marcatori legati alla SLA in modi che potrebbero essere adattativi più che distruttivi.
Grandi interrogativi e speranza cauta
Per i lettori non specialisti, il messaggio chiave è che la relazione tra radiazione e salute cerebrale è più sfumata del semplice “tutta la radiazione è dannosa”. In questo modello animale di grandi dimensioni, l’esposizione a bassa dose di raggi gamma ha prodotto spostamenti sottili e specifici per regione nelle proteine associate a SLA e DFT, senza riprodurre i modelli dannosi osservati nei cervelli dei pazienti. Questi cambiamenti potrebbero riflettere il tentativo del cervello di far fronte e riparare lo stress e, in alcuni casi, potrebbero perfino risultare benefici. Tuttavia, lo studio ha esaminato solo un mese dopo un’unica esposizione, e solo il cervello (non il midollo spinale, dove la SLA colpisce più duramente). Sono necessari studi a lungo termine e con dosi ripetute prima di pensare a una traduzione di questi risultati sull’uomo. Ciononostante, questo lavoro apre una nuova finestra su come la radiazione di livello quotidiano interagisca con le molecole alla base di devastanti malattie neurodegenerative — e solleva la possibilità che, in contesti attentamente controllati, piccole dosi possano un giorno essere sfruttate per stimolare le difese endogene del cervello.
Citazione: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Parole chiave: sclerosi laterale amiotrofica, demenza frontotemporale, radiazione a basso dosaggio, proteine cerebrali, modello miniporco