Clear Sky Science · it
FcIgG-GE11-Melittin come nuovo peptibody mirato su EGFR con potente attività citotossica contro le cellule tumorali
Il veleno d'ape incontra la terapia oncologica di precisione
Molti farmaci promettenti contro il cancro sono semplicemente troppo dannosi per il resto dell'organismo per poter essere usati in sicurezza. Un esempio evidente è la melittina, la tossina principale del veleno d'ape: può distruggere le cellule tumorali, ma può anche danneggiare i globuli rossi e i tessuti sani. Questo studio esplora un espediente intelligente: costruire un “missile guidato” che trasporta la melittina direttamente alle cellule tumorali che esprimono un marcatore di superficie specifico, risparmiando in larga misura le cellule normali.
Perché mirare a un interruttore comune del cancro
Un attore chiave in molti tumori è una molecola chiamata recettore del fattore di crescita epidermico, o EGFR. Questo recettore si trova sulla superficie delle cellule e aiuta a controllarne crescita e sopravvivenza. In diversi tumori — tra cui polmone, colon-retto, prostata e alcuni tumori della testa, del collo e del rene — l'EGFR è sovraespresso, promuovendo divisione cellulare incontrollata. Per questo motivo, i farmaci che si legano all'EGFR sono diventati una classe importante di terapie mirate. Tuttavia, i farmaci EGFR esistenti in genere bloccano i segnali; non provocano attivamente la lisi delle cellule tumorali. I ricercatori si sono chiesti se fosse possibile sfruttare la potente capacità lisi-cellulare della melittina e consegnarla selettivamente alle cellule tumorali ricche di EGFR.
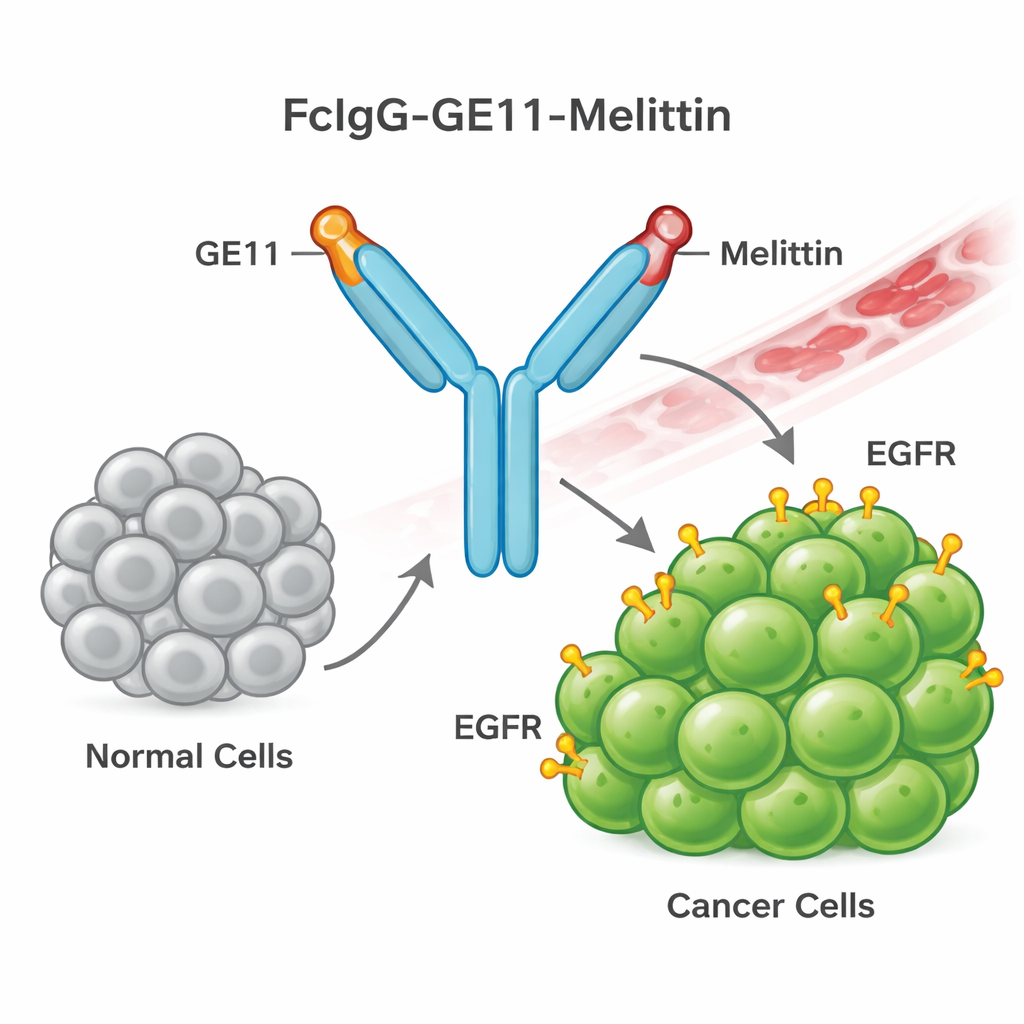
Costruire un’arma guidata con il veleno d'ape
Per farlo, il team ha progettato una nuova proteina di fusione chiamata FcIgG-GE11-Melittin. Essa combina tre componenti: una “coda” di anticorpo (la regione Fc dell'IgG umana) che migliora la stabilità nel circolo e facilita la purificazione; un breve peptide guida chiamato GE11 che riconosce e si lega all'EGFR delle cellule tumorali; e la melittina, il peptide del veleno d'ape in grado di rompere le membrane cellulari. Batteri sono stati ingegnerizzati per produrre questa proteina di fusione in grandi quantità. La proteina è stata quindi ripiegata correttamente e purificata, e i test di laboratorio hanno confermato che formava la struttura dimerica prevista e portava il tag dell'anticorpo umano, indicando che il costrutto era stato costruito correttamente.
Agganciarsi alle cellule tumorali, non a qualunque cellula
La domanda successiva era se questa molecola progettata trovasse davvero e si attaccasse alle cellule tumorali ricche di EGFR. Usando la citometria a flusso, gli autori hanno testato il legame su cellule di carcinoma polmonare A549, note per sovraesprimere EGFR. Le cellule trattate con FcIgG-GE11-Melittin hanno mostrato un forte aumento della fluorescenza, indicando che molte molecole di fusione si erano attaccate alla loro superficie. Un peptibody non correlato, Romiplostim, ha mostrato quasi nessun legame, fungendo da controllo negativo. Il profilo di legame del nuovo costrutto ha corrisposto strettamente a quello del Cetuximab, un noto anticorpo anti-EGFR, a sostegno dell'idea che il componente GE11 stia guidando correttamente la proteina di fusione verso il suo bersaglio.
Uccidere le cellule tumorali risparmiando i globuli rossi
Il team ha quindi testato quanto bene la proteina di fusione potesse uccidere diverse linee cellulari tumorali in coltura. La melittina libera da sola era estremamente potente ma indiscriminata, riducendo drasticamente la sopravvivenza cellulare anche a basse dosi in cellule di polmone (A549), prostata (DU145) e colon-retto (SW480). Al contrario, FcIgG-GE11-Melittin ha mostrato un'azione citotossica dipendente dalla dose, più marcata nelle cellule EGFR-positive, mentre una linea di carcinoma mammario a basso EGFR (MDA-MB-453) era relativamente resistente. Questo schema suggerisce che l'attacco del costrutto dipende dal targeting dell'EGFR più che da un danno casuale alle membrane. Soprattutto, negli esperimenti con globuli rossi umani, la melittina libera ha causato quasi completa emolisi a dosi modeste, mentre la proteina di fusione ha prodotto meno del 5% di emolisi anche a concentrazioni molto elevate. In altre parole, attaccare la melittina al vettore che cerca l'EGFR ha ridotto drasticamente la sua tendenza a far esplodere i globuli rossi.
Cosa potrebbe significare per la cura del cancro in futuro
Nel complesso, il lavoro mostra che accoppiare una tossina potente che distrugge le membrane come la melittina a un sistema di targeting preciso può trasformarla da una sostanza ampiamente tossica in un’arma più selettiva per i tumori. FcIgG-GE11-Melittin si lega saldamente alle cellule tumorali che sovraesprimono EGFR, le uccide in modo controllato e dipendente dalla dose, e mostra un danno minimo ai globuli rossi in laboratorio. Pur richiedendo ulteriori studi su animali e test di sicurezza prima di qualsiasi uso clinico, questo approccio illustra come re-ingegnerizzare tossine naturali in terapie guidate potrebbe aprire nuove strade per trattare i tumori EGFR-positivi in modo più efficace e con meno effetti collaterali.
Citazione: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Parole chiave: terapia oncologica mirata, EGFR, melittina del veleno d'ape, peptibody, veleni selettivi per i tumori