Clear Sky Science · it
TDP-43 citoplasmatico provoca deficit comportamentali precoci senza neurodegenerazione in un modello di C. elegans specifico per i neuroni serotoninergici
Perché i vermi minuscoli contano per le grandi malattie cerebrali
Patologie come la sclerosi laterale amiotrofica (SLA) e la demenza frontotemporale (FTD) privano gradualmente le persone della capacità di muoversi, parlare e della loro personalità. Un sospetto chiave in queste malattie è una proteina chiamata TDP-43, che si aggrega nel posto sbagliato all’interno delle cellule nervose. Questo studio utilizza un verme minuscolo, Caenorhabditis elegans, per osservare cosa succede negli animali viventi quando TDP-43 si sposta fuori dal suo normale sito e finisce nel citoplasma cellulare. Concentrandosi su un piccolo e ben noto insieme di neuroni produttrici di serotonina, i ricercatori mostrano come il comportamento possa alterarsi molto prima che i neuroni muoiano visibilmente—offrendo una finestra sulle fasi più precoci e più trattabili della malattia. 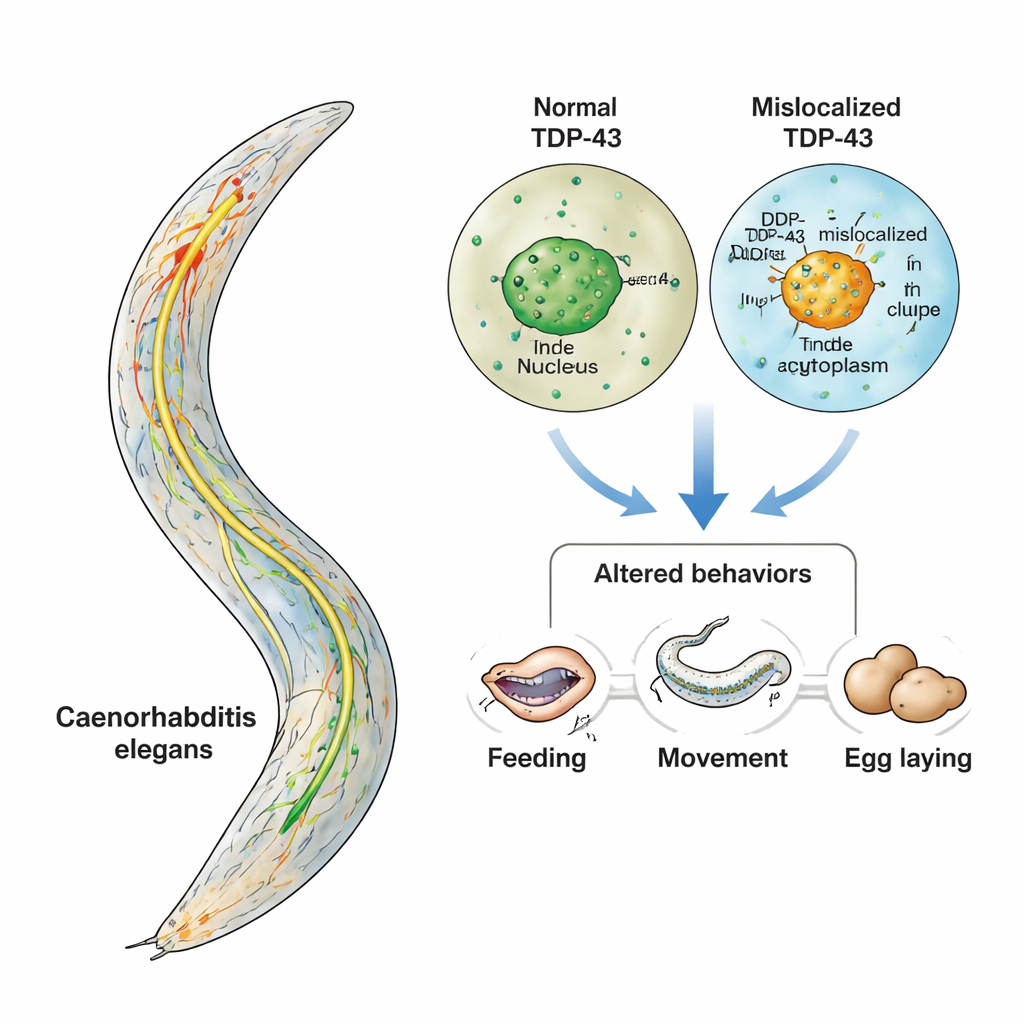
Una proteina che si aggrega e un messaggero chimico
TDP-43 normalmente risiede nel nucleo, dove aiuta a gestire l’RNA, le copie operative delle istruzioni genetiche della cellula. Nella SLA e nella FTD, tuttavia, TDP-43 spesso lascia il nucleo, si accumula nel citoplasma e forma aggregati appiccicosi. Allo stesso tempo, evidenze provenienti da pazienti e modelli murini suggeriscono che la serotonina, un mediatore chimico noto per il suo ruolo nell’umore, sia anch’essa alterata in queste malattie. Poiché la serotonina influenza molti comportamenti—dall’alimentazione al controllo del movimento—gli autori si sono posti una domanda mirata: se TDP-43 è mal localizzato specificamente nei neuroni che producono serotonina, quei neuroni funzionano male in modi che alterano il comportamento, anche prima di degenerare?
Riprogrammare un sistema nervoso semplice
Il gruppo si è rivolto a C. elegans, un verme microscopico il cui sistema nervoso completo di 302 neuroni è stato mappato in dettaglio. Solo tre paia di questi neuroni producono serotonina, e ciascuna coppia controlla un comportamento ben definito: alimentazione (battito faringeo), rallentamento quando si trova cibo, e deposizione delle uova. Usando strumenti genetici, i ricercatori hanno ingegnerizzato vermi in cui solo questi neuroni serotoninergici producevano la TDP-43 umana. Una linea esprimeva la forma normale, localizzata nel nucleo; un’altra esprimeva una versione mutante priva del «tag» che la indirizza al nucleo, costringendo TDP-43 ad accumularsi nel citoplasma. Poiché tutti gli altri neuroni sono rimasti intatti, qualsiasi cambiamento comportamentale poteva essere ricondotto direttamente a problemi in questo singolo e piccolo circuito.
Il comportamento fallisce prima che i neuroni muoiano
In diversi test, i vermi alterati si comportavano in modo anomalo in maniera che rispecchiava da vicino la perdita parziale o grave di serotonina. I vermi con la versione citoplasmatica di TDP-43 mostravano un battito faringeo più lento e ritmico, una minore tendenza a rallentare quando incontravano cibo dopo il digiuno e una ridotta deposizione delle uova. Anche i vermi che esprimevano la TDP-43 normale e nucleare si comportavano peggio rispetto agli animali non modificati, ma non tanto quanto quelli con TDP-43 citoplasmatica, rivelando un chiaro gradiente di compromissione. Fondamentale, quando gli stessi animali sono stati testati in un contesto in cui la serotonina non è necessaria—nuotando in liquido—il loro movimento era normale. Questo ha dimostrato che il nucleo meccanico locomotore era intatto e che i difetti erano specifici per i comportamenti dipendenti dalla serotonina piuttosto che un declino generale dello stato di salute. 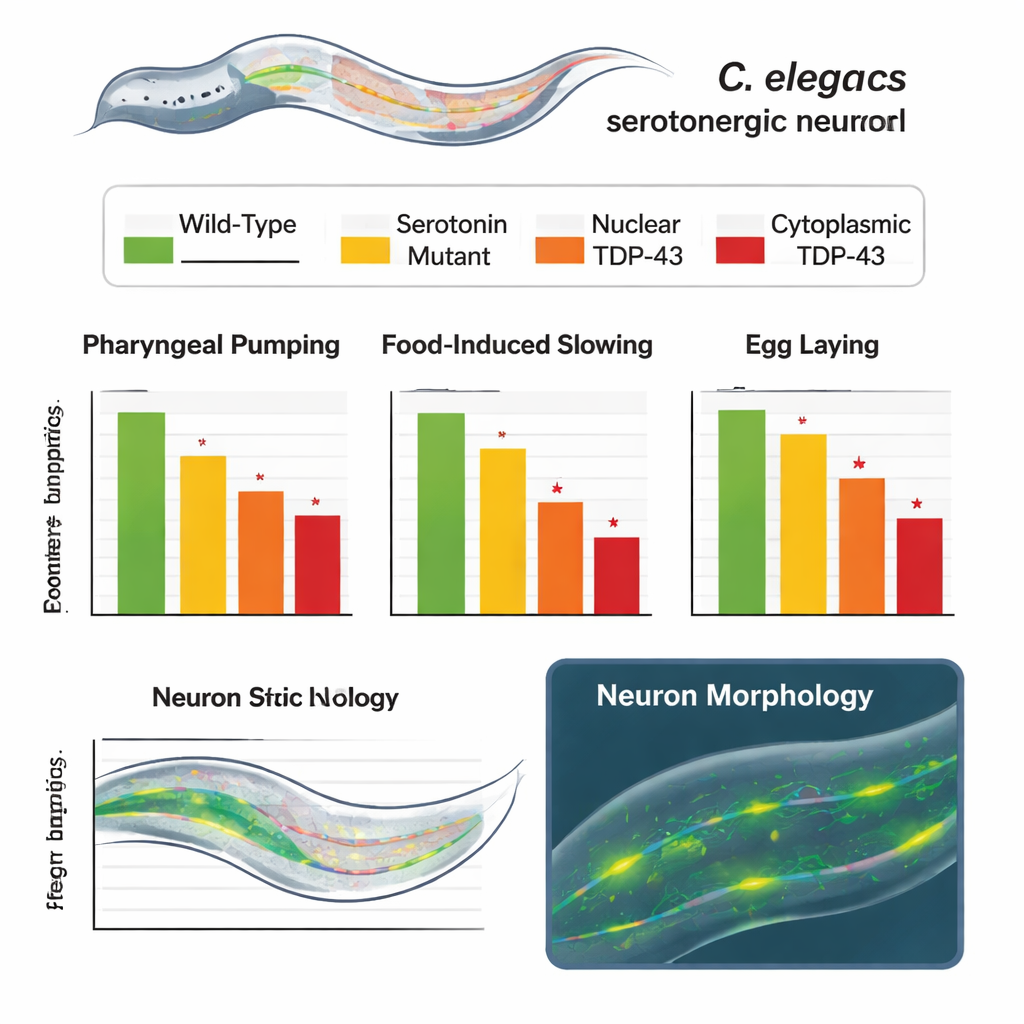
Danno nascosto rivelato da un test farmacologico
Per scoprire se i neuroni interessati fossero ancora vivi e funzionali, i ricercatori hanno usato la fluoxetina, meglio nota come Prozac, un farmaco che potenzia la segnalazione serotoninergica. Nei vermi normali, la fluoxetina aumenta nettamente la deposizione delle uova. Nei vermi ingegnerizzati, il farmaco aumentava ancora la deposizione delle uova, ma la risposta era attenuata—soprattutto in quelli con TDP-43 citoplasmatica. Questo schema suggerisce che i neuroni della serotonina potevano ancora rilasciare segnali, ma lo facevano in modo meno efficace. L’imaging microscopico raccontava una storia simile: i neuroni produttrici di serotonina apparivano strutturalmente normali, senza perdita dei corpi cellulari o distorsioni evidenti nei loro rami, e la loro fluorescenza complessiva—un indicatore dello stato di salute cellulare—corrispondeva a quella dei vermi di controllo.
Segnali precoci e nuove opportunità
Nel complesso, i risultati dipingono un quadro in cui la TDP-43 mal localizzata può perturbare seriamente il funzionamento dei neuroni serotoninergici lasciandoli tuttavia apparentemente intatti alla vista. Nei vermi, il comportamento si altera—alimentazione, adattamento del movimento e riproduzione—prima che si osservi qualsiasi morte neuronale visibile. Ciò rispecchia osservazioni cliniche in cui cambiamenti sottili nel comportamento e nell’umore spesso precedono il restringimento cerebrale evidente nelle malattie neurodegenerative umane. Offrendo un sistema semplice e geneticamente manipolabile in cui i difetti precoci e specifici dei circuiti possono essere misurati con precisione, questo modello di verme potrebbe aiutare gli scienziati a indagare come TDP-43 comprometta la funzione neuronale e a testare terapie volte a salvare i neuroni durante questa finestra vulnerabile, predegenerativa.
Citazione: Lacour, A., Vassallu, F., Romussi, S. et al. Cytoplasmic TDP-43 leads to early behavioral impairments without neurodegeneration in a serotonergic neuron-specific C. elegans model. Sci Rep 16, 6068 (2026). https://doi.org/10.1038/s41598-026-36138-5
Parole chiave: TDP-43, neuroni della serotonina, C. elegans, ALS e FTD, neurodegenerazione