Clear Sky Science · it
Le posizioni R5 e R7 sugli scheletri dei fluorochinoloni guidano la disgregazione dei filamenti di F-actina
Trasformare antibiotici in alleati del cervello
Molti disturbi cerebrali comuni, dall’Alzheimer al morbo di Parkinson, condividono un colpevole nascosto: piccole barre strutturali all’interno dei neuroni che col tempo si bloccano e si irrigidiscono. Queste barre sono costituite da una proteina chiamata actina, normalmente una componente flessibile dello scheletro interno della cellula. Questo studio esplora una possibilità sorprendente: una classe nota di antibiotici, i fluorochinoloni, potrebbe essere riprogettata per separare delicatamente questi aggregati dannosi di actina e potenzialmente contribuire a proteggere il cervello.
Quando lo scheletro cellulare si guasta
Le cellule cerebrali sane rimodellano continuamente il proprio scheletro interno per formare e aggiornare connessioni. I filamenti di actina sono centrali in questo processo, formando e dissolvendosi secondo necessità. Sotto stress, però, l’actina può bloccarsi in aggregati rigidi a forma di asta che ostruiscono la cellula, interrompono il trasporto di carichi vitali e favoriscono l’accumulo di proteine legate a malattia come amiloide e tau. Nel corso degli anni questi aggregati possono maturare in strutture dense note come corpi di Hirano, frequentemente osservate nei cervelli di persone con diverse condizioni neurodegenerative. Poiché i farmaci esistenti che prendono di mira l’actina sono spesso altamente tossici, i ricercatori cercano piccole molecole più sicure che possano allentare questi aggregati senza danneggiare le cellule.
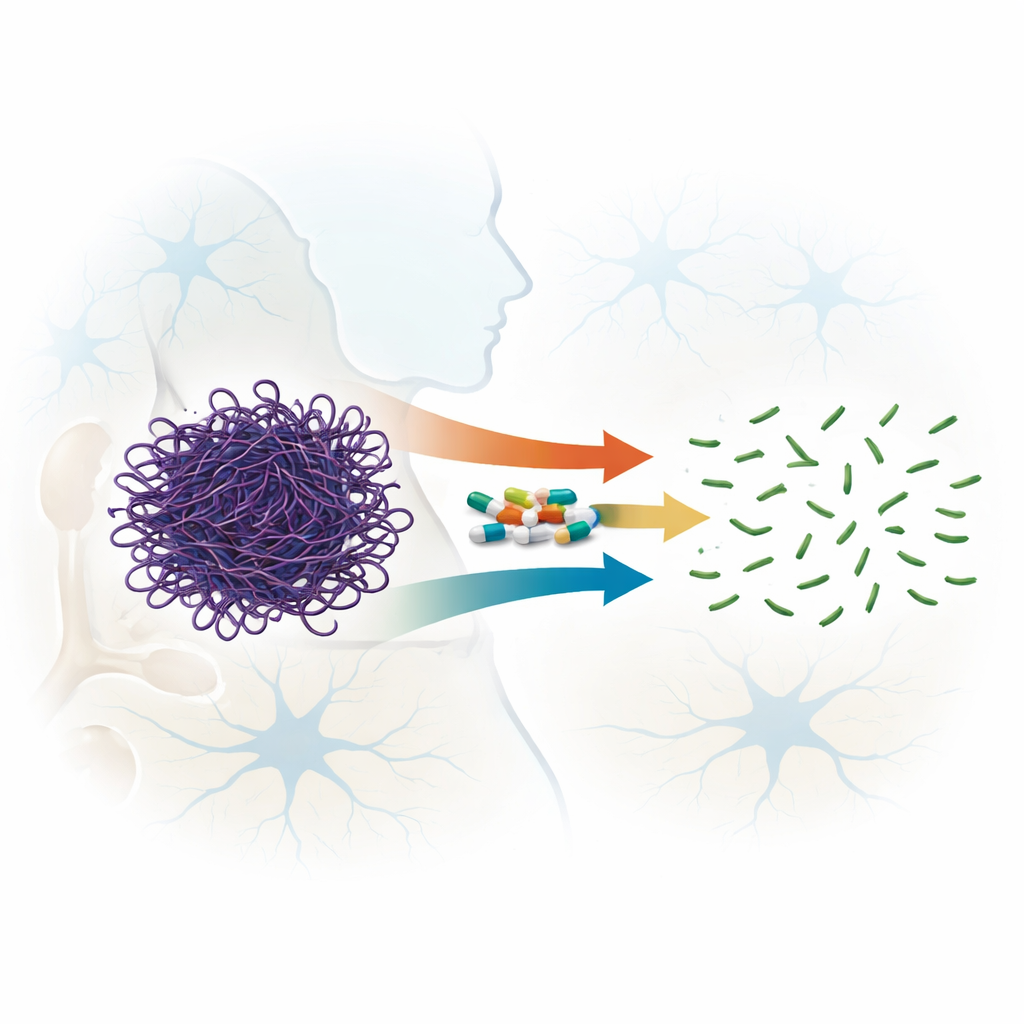
Un talento inaspettato di farmaci familiari
I fluorochinoloni sono antibiotici ad ampio spettro utilizzati in tutto il mondo per trattare le infezioni, e alcuni membri più nuovi di questa famiglia sono in grado di attraversare la barriera ematoencefalica. Indizi precedenti suggerivano che alcuni fluorochinoloni potessero destabilizzare i filamenti di actina. In questo lavoro gli autori hanno confrontato sistematicamente sette composti correlati, appartenenti a quattro generazioni della famiglia, per valutare quanto efficacemente rompessero filamenti di actina già formati piuttosto che limitarsi a impedirne la formazione. Mediante misure di diffusione della luce, microscopia elettronica e filtrazione su gel, hanno dimostrato che tutti i farmaci testati potevano disturbare i filamenti di actina, ma con intensità molto diverse. Due farmaci, lo sparfloxacina (composto di terza generazione) e la moxifloxacina (quarta generazione), si sono distinti per la capacità di tagliare rapidamente e irreversibilmente i filamenti lunghi in frammenti molto più piccoli, anche a rapporti farmaco/proteina relativamente bassi.
Vedere i filamenti spezzarsi
Immagini ad alta risoluzione e test biofisici hanno rivelato come i filamenti cambiano sotto trattamento farmacologico. La microscopia elettronica ha mostrato che l’actina non trattata forma lunghe strisce continue, mentre i fluorochinoloni efficaci le convertono in frammenti corti e dispersi. I membri meno potenti hanno prodotto filamenti piegati e angolati ma non li hanno completamente spezzati. Misurazioni termiche della stabilità proteica hanno confermato questa disgregazione fisica: una volta trattata, l’actina si comportava più come la sua forma libera e non assemblata, con temperature di fusione inferiori, pur mantenendo quasi intatta la sua struttura di base. Ciò suggerisce che i farmaci non denaturano o danneggiano l’actina stessa, ma principalmente indeboliscono il modo in cui le unità si legano tra loro nei filamenti.
Avvicinarsi alla presa molecolare
Per capire perché alcuni fluorochinoloni funzionino meglio di altri, il team ha combinato sofisticati esperimenti di risonanza magnetica nucleare con simulazioni al computer delle interazioni farmaco–proteina. Hanno scoperto che tutti i composti si basano su un “nucleo” ad anello condiviso per contattare l’actina, in particolare in due posizioni su quel nucleo che toccano ripetutamente il filamento. Tuttavia, gruppi chimici aggiuntivi attaccati in siti specifici — indicati come R5 e R7 — influenzano fortemente quanto saldamente e dove ciascuna molecola si leghi. Nei disgregatori più efficaci, queste posizioni portano un gruppo amminico e sistemi ad anello ingombranti che si estendono in una piccola tasca all’interfaccia tra filamenti di actina adiacenti. Lì interferiscono con contatti stabilizzanti chiave, incluso un importante ponte salino che normalmente contribuisce a mantenere uniti i filamenti.
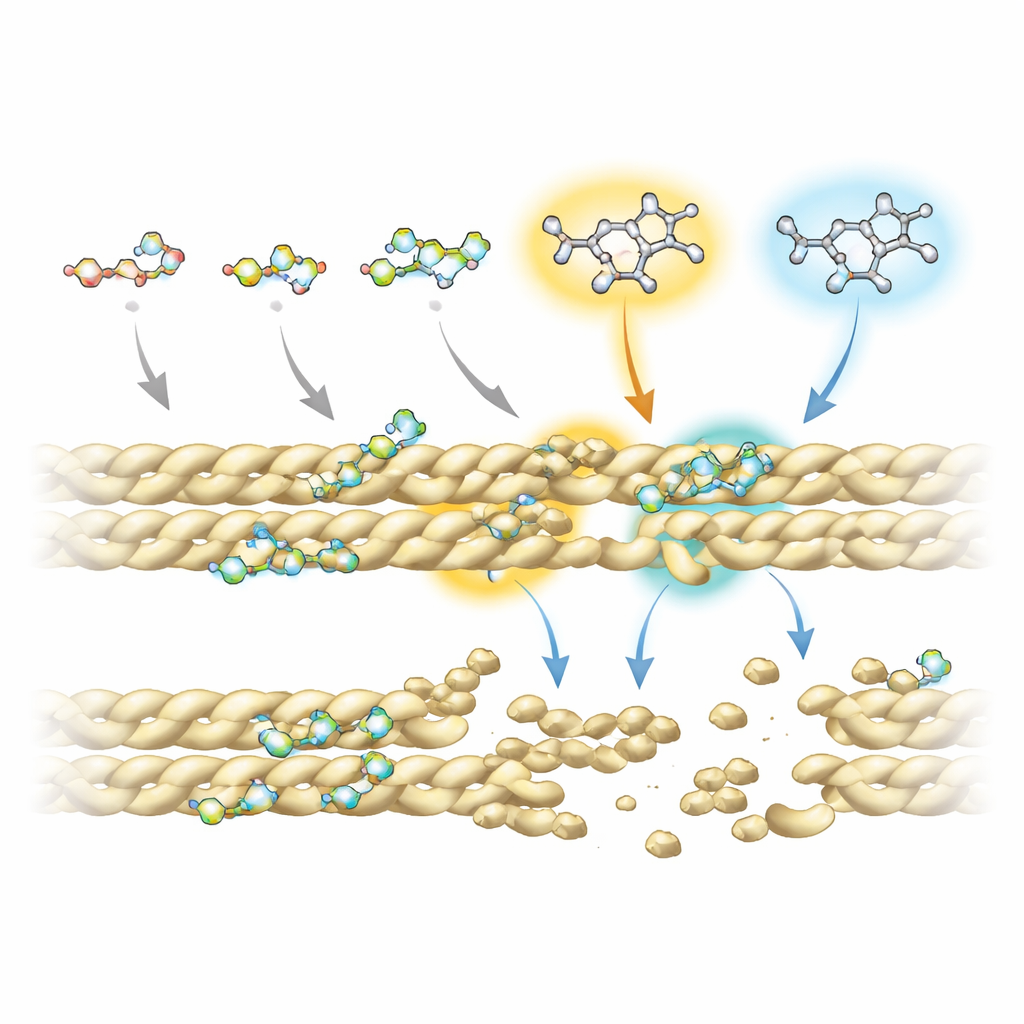
Dalle cellule di lievito alle terapie future
I ricercatori hanno anche testato i farmaci in un ceppo di lievito che accumula naturalmente fasci di actina, imitando alcuni aspetti delle cellule malate. Al microscopio, il lievito non trattato mostrava grandi ammassi brillanti di actina, mentre le cellule esposte ai fluorochinoloni — in particolare sparfloxacina, moxifloxacina e, a dosi più elevate, acido nalidixico — mostravano pattern molto più diffusi e punctati, indicando che i fasci erano stati disgregati. È importante che l’azione dei farmaci apparisse relativamente delicata: indebolivano l’impacchettamento dei filamenti senza deformare grossolanamente la forma sottostante dell’actina, e il loro legame risultava più debole rispetto ai classici veleni dell’actina, riducendo potenzialmente il rischio di effetti collaterali gravi.
Progettare farmaci più intelligenti contro l’actina
Complessivamente, questo studio mostra che piccole modifiche a antibiotici ben noti possono cambiare drasticamente il modo in cui interagiscono con lo scheletro interno della cellula. Identificando le posizioni R5 e R7 come “manopole di controllo” chiave sia per la disgregazione dell’actina sia per la penetrazione cerebrale, gli autori tracciano un progetto per creare nuove molecole ispirate ai fluorochinoloni che smontino selettivamente gli aggregati di actina dannosi. Sebbene questi risultati siano una prova di principio precoce e limitata al laboratorio, sollevano la possibilità che in futuro farmaci derivati da antibiotici familiari possano aiutare a sgomberare lo scheletro tossico nei neuroni e rallentare o prevenire alcune forme di neurodegenerazione.
Citazione: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Parole chiave: aggregati di actina, antibiotici fluorochinolonici, malattie neurodegenerative, riuso di farmaci, citoscheletro