Clear Sky Science · it
Il ruolo dei geni correlati alla senescenza cellulare nel danno da ischemia‑riperfusione e l’identificazione dei loro biomarcatori
Perché il danno cardiaco può peggiorare quando il sangue ritorna
Quando una persona ha un attacco di cuore o si sottopone a un intervento cardiaco, i medici cercano in fretta di ripristinare il flusso di sangue al muscolo cardiaco in sofferenza. Paradossalmente, quel gesto salvavita può però causare danni aggiuntivi — un problema noto come danno da ischemia‑riperfusione. Questo studio esplora perché alcune cellule cardiache rispondono così male al ritorno del sangue, concentrandosi sulla biologia dell’invecchiamento cellulare e identificando un piccolo insieme di geni che potrebbero aiutare i medici a individuare e, in futuro, trattare con maggiore precisione questo danno nascosto.
Quando il soccorso si trasforma in nuovo danno
Il danno da ischemia‑riperfusione si svolge in due atti. Prima, un’arteria coronaria si occlude e il tessuto cardiaco viene privato di ossigeno (ischemia). Poi, quando l’ostruzione viene rimossa e il sangue torna a fluire (riperfusione), un’ondata di molecole reattive e di infiammazione può danneggiare cellule già fragili. Gli strumenti attuali — come l’ECG, le immagini diagnostiche e i test ematici per proteine come la troponina — spesso non rilevano lesioni precoci o lievi e non possono facilmente prevedere chi avrà problemi a lungo termine. Questa lacuna ha spinto i ricercatori a indagare più a fondo, sugli eventi molecolari che avvengono all’interno delle cellule cardiache stesse.
La senescenza cellulare come fattore nascosto
Gli autori si concentrano sulla senescenza cellulare, uno stato in cui le cellule smettono di dividersi in modo permanente e adottano un comportamento da “lampo d’allarme”. Le cellule cardiache senescenti secernono un mix di molecole infiammatorie ed enzimi noto come fenotipo secretorio associato alla senescenza. Questa nube chimica può aggravare la formazione di cicatrici, attirare cellule immunitarie e interferire con la riparazione tessutale, creando un circolo vizioso di danno e disfunzione cronica. Analizzando set di dati pubblici di espressione genica provenienti da cuori di topo esposti a ischemia‑riperfusione e incrociandoli con centinaia di geni legati alla senescenza cellulare, il gruppo ha ridotto la selezione a 26 geni che cambiano marcatamente dopo il danno.
Sei geni che formano un’impronta diagnostica
Per trovare i segnali più informativi tra quei 26 geni, i ricercatori hanno usato diversi metodi di apprendimento automatico. Questi algoritmi cercano combinazioni di geni che meglio distinguono i cuori lesionati da quelli sani. Dopo analisi con regressione logistica, LASSO e macchine a vettori di supporto, sei geni sono emersi come un potente pannello diagnostico: CDKN2B, ID1, STAT3, TERF2, TP53 e ZNF277. Insieme, i loro pattern di attività hanno potuto identificare il danno da ischemia‑riperfusione con elevata accuratezza nei dataset combinati, superando molti marcatori ematici tradizionali nei test interni. Analisi di vie geniche hanno collegato questi marcatori a circuiti di risposta allo stress che coinvolgono danno ossidativo, programmi di morte cellulare e vie di segnalazione ben note come MAPK e PI3K–AKT, tutte implicate nel determinare se una cellula si riprende o scivola in senescenza permanente.
Come il sistema immunitario entra nella storia
Il danno dovuto al ritorno del flusso sanguigno non avviene in isolamento; cellule immunitarie affluiscono rapidamente nel cuore. Stimando l’attività delle cellule immunitarie dagli stessi dati di espressione genica, lo studio ha trovato chiari segni di maggiore partecipazione immunitaria nei cuori lesionati, incluse diverse tipologie di cellule T, cellule B, macrofagi e mastociti. Un gene correlato all’invecchiamento, CDKN2B, ha mostrato una forte correlazione con le cellule T CD4 a “memoria centrale”, mentre TP53 si è correlato con mastociti attivati. Questi legami suggeriscono che le vie legate alla senescenza nelle cellule cardiache e i cambiamenti del sistema immunitario si rinforzano a vicenda: le cellule che invecchiano attirano aiuto immunitario e quelle risposte immunitarie possono, a loro volta, approfondire il danno e la formazione di cicatrici.
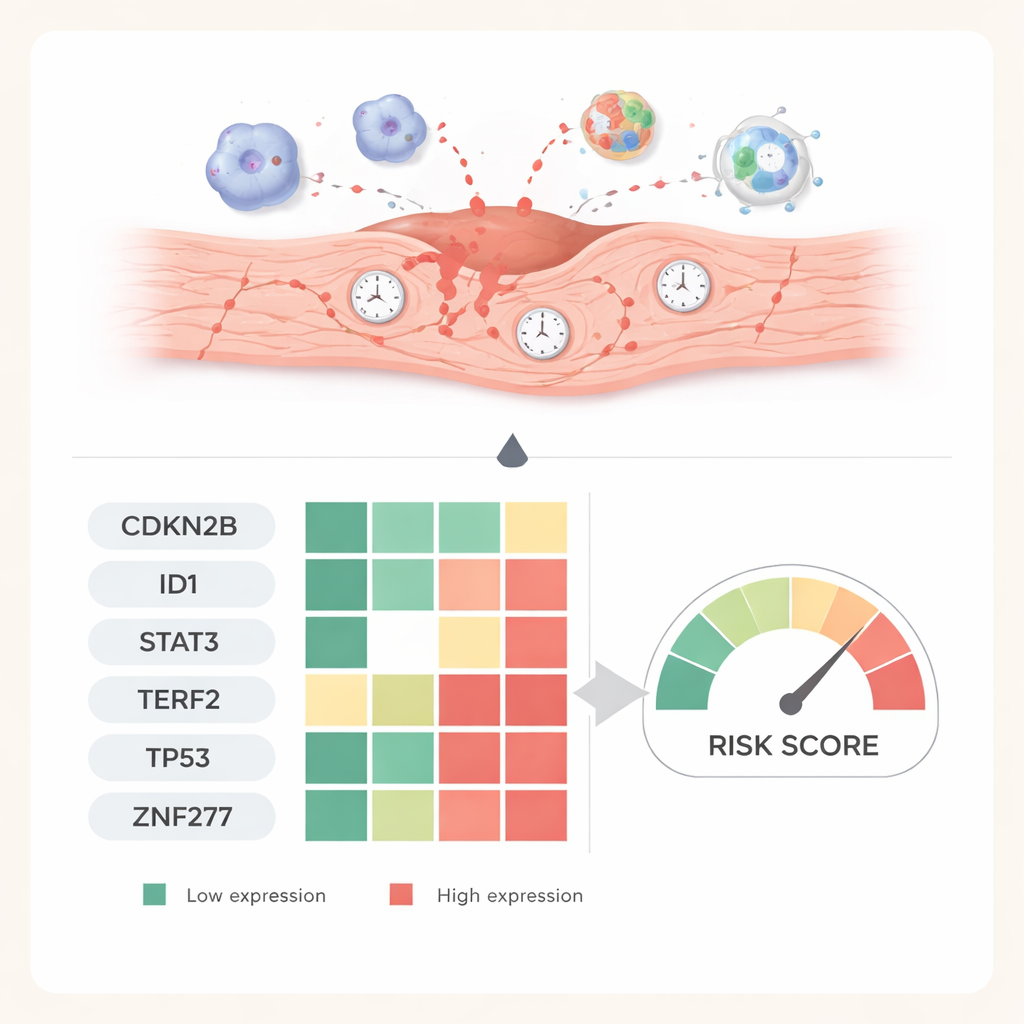
Dalla predizione al computer ai cuori viventi
Per verificare se questi sei geni contano anche al di là degli schermi del computer, i ricercatori hanno creato un modello murino di danno da ischemia‑riperfusione. Hanno misurato l’attività genica in diversi momenti dopo il ripristino del flusso sanguigno e hanno usato colorazioni tissutali per visualizzare le proteine corrispondenti nelle sezioni cardiache. Un gene, CDKN2B, è aumentato costantemente nell’arco di una settimana, suggerendo che contribuisce a fissare le cellule danneggiate in uno stato di senescenza di lunga durata. Altri, tra cui ID1, STAT3, TP53, TERF2 e ZNF277, sono diminuiti bruscamente nelle fasi iniziali per poi recuperare gradualmente, rispecchiando i passaggi tra stress acuto, danno attivo e successiva riparazione. Questi pattern dipendenti dal tempo supportano l’idea che ciascun gene catturi una fase diversa della risposta cardiaca.
Cosa potrebbe significare per i pazienti
Per un lettore non specialista, il messaggio chiave è che lo studio collega il danno correlato all’infarto alla biologia della senescenza cellulare e identifica una “impronta” di sei geni che segnala questo danno in modelli sperimentali. Pur essendo ancora lavoro preclinico basato principalmente su dati murini e banche dati pubbliche, offre una tabella di marcia per nuovi test ematici o tissutali che potrebbero rilevare il danno da ischemia‑riperfusione prima e con maggiore specificità rispetto agli strumenti attuali. A lungo termine, comprendere come questi geni legati all’invecchiamento dirigano infiammazione, fibrosi e riparazione potrebbe aprire la strada a trattamenti che non solo riaprono le arterie bloccate, ma aiutano anche il cuore rianimato a guarire in modo più completo.
Citazione: Sun, L., Liu, H., Jia, T. et al. The role of cellular senescence-related genes in ischemia–reperfusion injury and the identification of their biomarkers. Sci Rep 16, 5211 (2026). https://doi.org/10.1038/s41598-026-36076-2
Parole chiave: danno da ischemia e riperfusione, senescenza cellulare, attacco di cuore, biomarcatori, infiammazione immunitaria