Clear Sky Science · it
Classificazione della gravità della demenza correlata all’Alzheimer da risonanza magnetica mediante ottimizzazione senza derivata di reti neurali convoluzionali
Aiutare i medici a individuare la demenza prima
Con l’invecchiamento delle popolazioni molte famiglie temono la perdita di memoria e la demenza. Le immagini cerebrali possono rivelare cambiamenti precoci legati al morbo di Alzheimer, ma leggere migliaia di scansioni a occhio è lento e difficoltoso, anche per gli esperti. Questo studio presenta uno strumento informatico intelligente che analizza le risonanze magnetiche cerebrali e classifica le persone in quattro livelli di gravità della demenza, dall’assenza di demenza fino a un lieve deficit moderato. Il sistema è progettato per essere estremamente preciso e abbastanza leggero da funzionare sui normali computer ospedalieri, rendendo l’analisi avanzata delle immagini più accessibile.
Un nuovo assistente intelligente per le scansioni cerebrali
I ricercatori si concentrano su un tipo di intelligenza artificiale chiamata rete neurale convoluzionale, o CNN, che eccelle nel riconoscere pattern nelle immagini. Invece di decidere semplicemente se una persona abbia il morbo di Alzheimer, il loro strumento distingue quattro stadi: non demenza, molto lieve, lieve e moderata demenza. Per farlo, il team ha addestrato il modello su grandi raccolte pubbliche di scansioni MRI già etichettate da esperti. L’obiettivo era duplice: raggiungere un’accuratezza prossima alla perfezione e mantenere il modello compatto e veloce, in modo che potesse risultare pratico per l’uso clinico quotidiano e non solo per laboratori di ricerca ben finanziati.
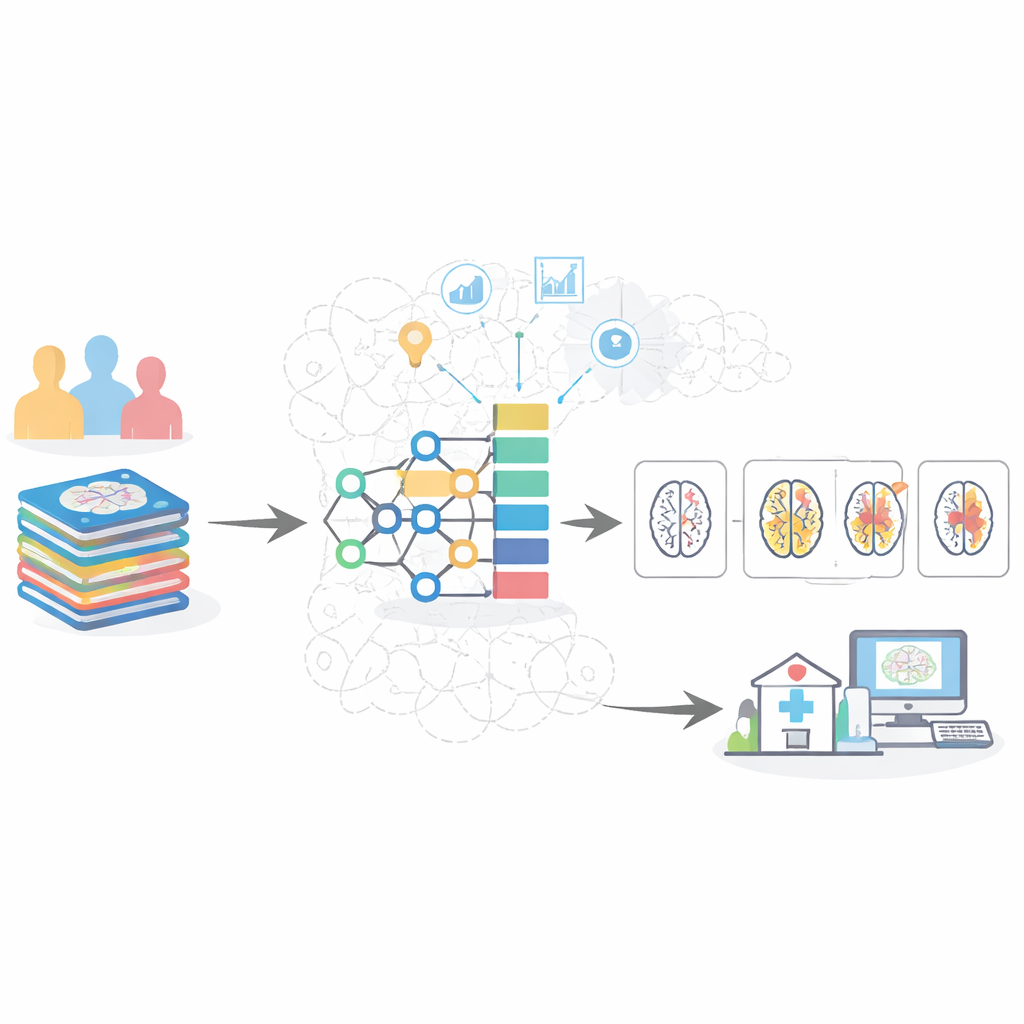
Bilanciare i dati e pulire le immagini
Una sfida chiave nei dati medici è che non tutti gli stadi della malattia sono rappresentati in modo uniforme. In queste raccolte di scansioni cerebrali i casi sani e molto lievi sono comuni, mentre le scansioni di demenza moderata sono molto più rare. I sistemi AI standard tendono quindi a “giocare sul sicuro” sovrapredicendo le classi comuni e trascurando le fasi iniziali o moderate della malattia. Per contrastare questo problema, gli autori hanno usato una strategia in due fasi: hanno prima rimosso le immagini borderline più ambigue e poi generato esempi sintetici realistici per gli stadi sottorappresentati. Parallelamente, hanno preparato con cura ogni fetta MRI applicando filtri, isolando il cervello dai tessuti circostanti e normalizzando luminosità e contrasto in modo che il modello potesse concentrarsi su caratteristiche di rilievo medico, come l’assottigliamento delle strutture profonde della memoria e l’allargamento degli spazi pieni di liquido.
Progettare una rete più piccola e più intelligente
Invece di affidarsi ai metodi tradizionali di addestramento che regolano i parametri seguendo gradienti matematici, il team ha impiegato una famiglia di tecniche di ottimizzazione cosiddette senza derivata. Hanno iniziato con una CNN convenzionale più ampia e poi hanno usato ricerca evolutiva e neural architecture search per far evolvere un design più semplice con soltanto tre strati convoluzionali e molte meno filtri. L’ottimizzazione bayesiana ha messo a punto i parametri di addestramento, mentre il simulated annealing e il pruning hanno rimosso connessioni inutili dopo l’addestramento. Il risultato finale, chiamato DAPA-CNN, ha circa l’85% di parametri aggiustabili in meno rispetto al modello di partenza, occupa circa un quarto della memoria e si addestra in meno dei due terzi del tempo, pur catturando i pattern cruciali nelle scansioni.
Prestazioni quasi perfette e spiegazioni visive chiare
Nonostante le dimensioni ridotte, DAPA-CNN si è dimostrata sorprendentemente accurata. Su un importante dataset sull’Alzheimer ha assegnato correttamente lo stadio di demenza in quasi tutti i casi, con accuratezza e altre misure di performance attorno al 99%. Il modello si è anche generalizzato bene su un dataset multicentrico separato raccolto con scanner diversi, suggerendo robustezza rispetto alle variazioni reali delle immagini. Per rendere il sistema più trasparente per i clinici, gli autori hanno generato mappe di attivazione di classe—sovrapposizioni tipo heatmap che mostrano quali regioni cerebrali hanno influenzato una data decisione. Negli stadi precoci queste mappe enfatizzano aree coinvolte nella memoria note per deteriorarsi per prime nell’Alzheimer; negli stadi successivi si estendono a regioni corticali più ampie, in linea con la comprensione clinica della progressione della malattia.
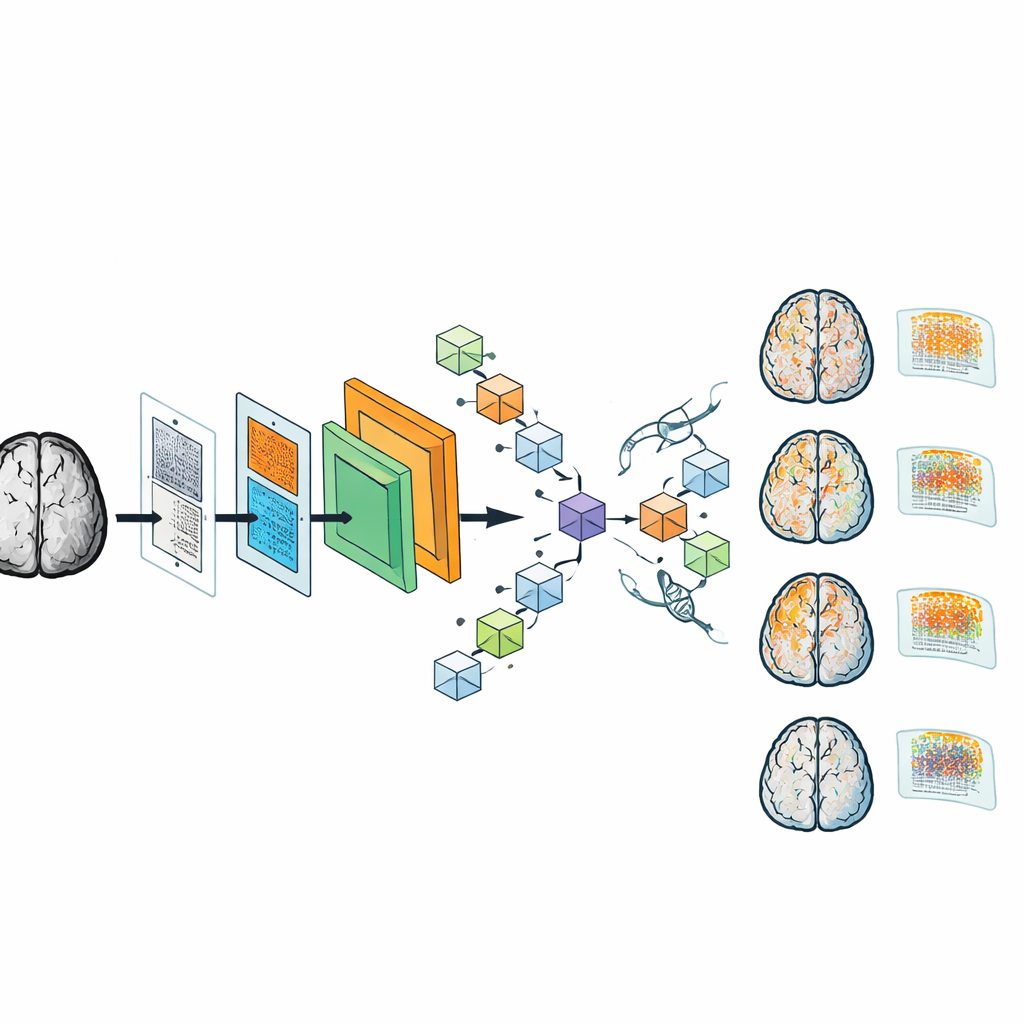
Cosa significa per pazienti e cliniche
Per i non specialisti, il messaggio principale è che lo studio propone uno strumento rapido, compatto e interpretabile per classificare la gravità della demenza dalle risonanze magnetiche di routine. Bilanciando i dati di addestramento e modellando con cura la rete tramite ottimizzazione senza derivata, gli autori hanno creato un modello che può funzionare su hardware modesto offrendo un’accuratezza prossima alla perfezione e mettendo in evidenza le regioni cerebrali alla base delle sue decisioni. Se confermata in futuri trial clinici prospettici, tale tecnologia potrebbe supportare una diagnosi più precoce, una stadiazione più coerente tra gli ospedali e un migliore monitoraggio di come il morbo di Alzheimer modifica il cervello nel tempo.
Citazione: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Parole chiave: morbo di Alzheimer, risonanza cerebrale (MRI), stadiazione della demenza, deep learning, AI per imaging medico