Clear Sky Science · it
L’apprendimento auto-supervisionato su grafi predice associazioni tra RNA non codificanti e malattie
Perché gli RNA nascosti sono importanti per la nostra salute
La maggior parte di noi ha imparato che il compito principale dell’RNA è aiutare a costruire le proteine. Negli ultimi dieci anni, però, gli scienziati hanno scoperto un numero vastissimo di RNA “non codificanti” che non diventano mai proteine ma influenzano comunque il funzionamento delle cellule. Molti di questi molecole sono oggi riconosciute come fattori che possono promuovere o sopprimere tumori e altre malattie complesse. Scoprire quali RNA non codificanti sono collegati a quali malattie potrebbe rivelare nuovi modi per diagnosticare le malattie precocemente o progettare terapie più mirate — ma testare tutte le possibilità in laboratorio sarebbe impossibilmente lento. Questo studio presenta un metodo informatico potente in grado di setacciare grandi reti biologiche e proporre con affidabilità le connessioni RNA–malattia più promettenti da verificare sperimentalmente.
Da rifiuto a ruoli cellulari chiave
Per anni gli RNA non codificanti sono stati liquidati come residui privi di significato dell’attività genica. Oggi sappiamo che famiglie come i microRNA, i long non-coding RNA e gli RNA circolari orchestrano processi vitali, dalla compattazione del DNA all’accensione e spegnimento dei geni fino alla trasmissione di segnali all’interno delle cellule. Poiché occupano molti punti di controllo, anche piccole variazioni in questi RNA possono spostare l’equilibrio verso il cancro o altre patologie. I clinici li stanno già considerando come potenziali biomarcatori e bersagli farmacologici. La sfida è la scala: esistono migliaia di RNA diversi e centinaia di malattie, e gli esperimenti tradizionali per testare ogni collegamento possibile sono costosi e richiedono tempo. Qui entra in gioco la previsione computazionale, che offre un modo per restringere lo spazio di ricerca.
Come leggere una rete biologica
I metodi informatici precedenti cercavano di prevedere i collegamenti RNA–malattia scomponendo grandi tabelle di dati in pezzi più semplici o addestrando modelli di machine learning su esempi noti. Questi approcci sono stati utili, ma spesso ignoravano il modo in cui RNA e malattie sono intessuti in reti. Le moderne “reti neurali su grafi” trattano RNA e malattie come punti connessi da linee, proprio come una rete sociale. Possono imparare pattern su chi è collegato a chi. Tuttavia, la maggior parte di questi metodi grafici richiede molti esempi di addestramento affidabili e numerose caratteristiche di input progettate con cura. Questo li rende sensibili ai dati mancanti, alle misurazioni rumorose e all’overfitting — funzionano bene sui dati noti ma falliscono quando devono prevedere nuove associazioni.
Imparare dai dati stessi
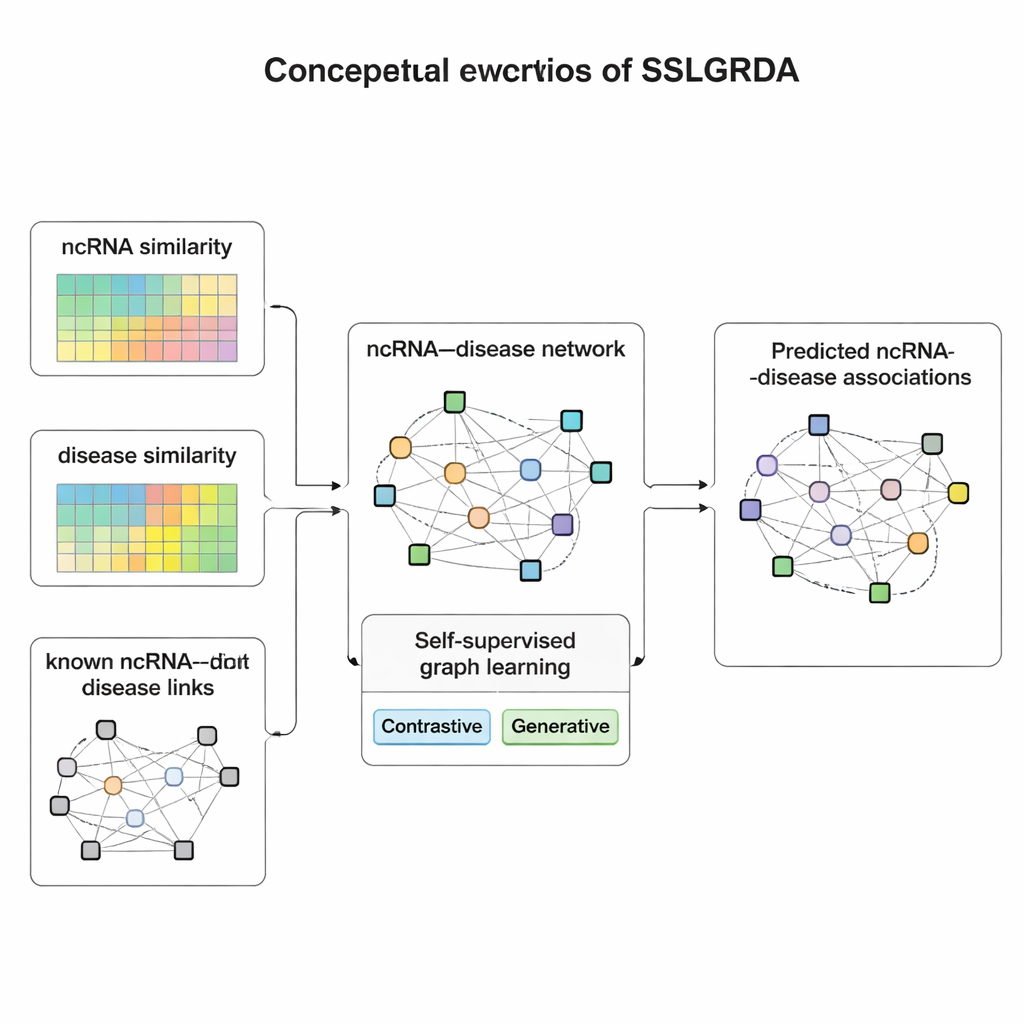
Gli autori presentano SSLGRDA, un nuovo quadro che insegna a un modello basato su grafi a individuare pattern utili senza dipendere pesantemente da dati etichettati. L’idea chiave è l’“apprendimento auto-supervisionato”: invece di indicare quali RNA sono associati a quali malattie, il modello inventa compiti di allenamento autonomi basati unicamente sulla struttura e sugli attributi della rete. I ricercatori costruiscono due tipi di grafi. Uno mantiene RNA e malattie come tipi di nodo distinti collegati da link noti. L’altro li unisce in un’unica grande rete omogenea che include anche informazioni di similarità — quanto sono simili due RNA o due malattie — in modo che elementi scarsamente connessi ottengano vicini di supporto. Su questi grafi, SSLGRDA usa due stili di auto-allenamento. Le strategie contrastive chiedono al modello di riconoscere che diverse “visioni” dello stesso nodo (per esempio, le sue connessioni rispetto ai suoi attributi) dovrebbero produrre rappresentazioni interne simili, separando al contempo i nodi non correlati. Le strategie generative nascondono deliberatamente parti delle caratteristiche di input e sfidano il modello a ricostruirle, incoraggiandolo a catturare strutture più profonde invece di memorizzare il rumore.
Mettere il metodo alla prova
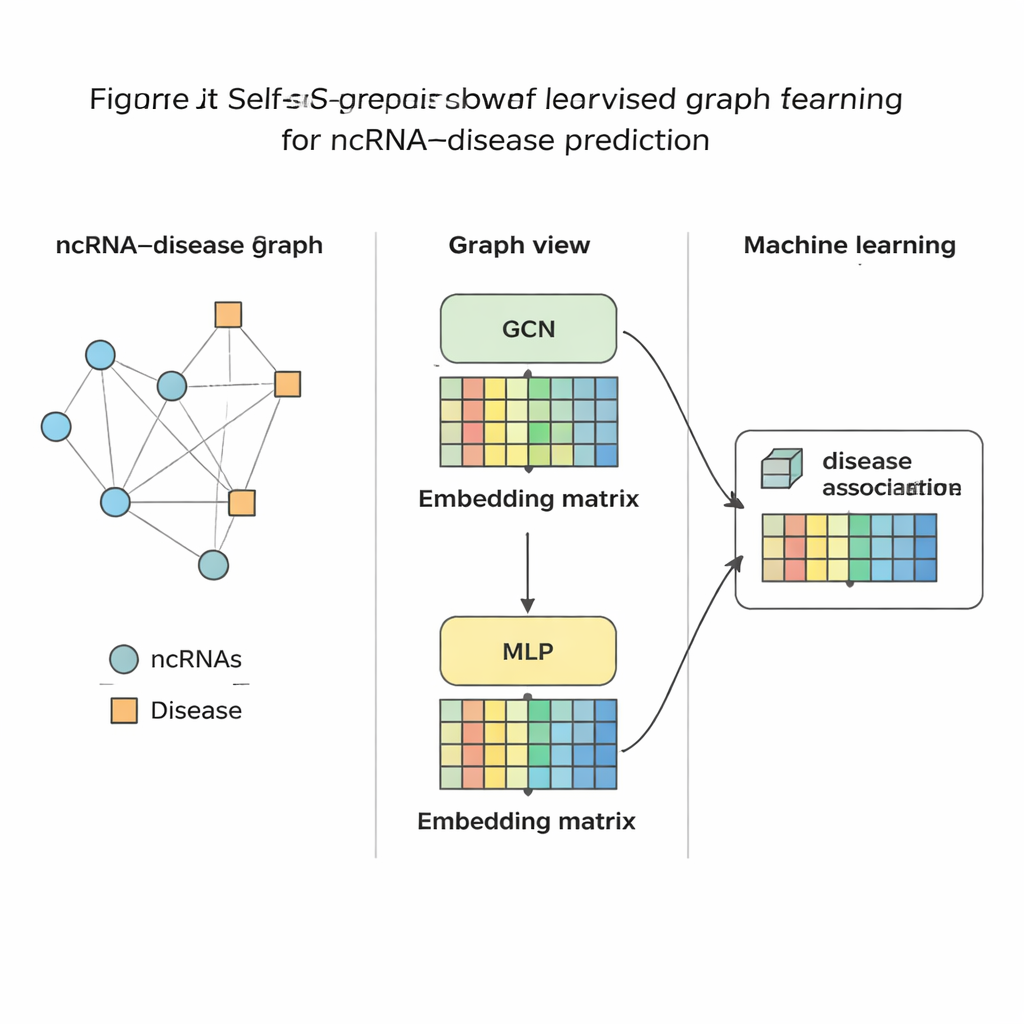
Una volta che SSLGRDA ha distillato ogni RNA e ogni malattia in un’impronta numerica compatta, viene addestrato un classificatore standard di machine learning per giudicare se un loro collegamento sia probabile o meno. Gli autori hanno valutato l’approccio su nove set di dati diversi che coprono tre principali tipi di RNA e centinaia di malattie. In generale, le varianti auto-supervisionate contrastive sul grafo omogeneo (mescolato) hanno ottenuto i migliori risultati, superando una serie di strumenti esistenti, inclusi robusti metodi basati su grafi. Il metodo non solo ha raggiunto una maggiore accuratezza nei test globali, ma ha anche posizionato i partner corretti in cima alle classifiche quando si considerava un singolo RNA o una singola malattia alla volta — cruciale per l’uso pratico in cui un biologo può partire da un singolo cancro e chiedersi quali RNA studiare. Hanno inoltre mostrato che le stesse idee si trasferiscono bene ad altre reti biomediche, come quelle che collegano microbi a malattie o farmaci.
Dalle previsioni a possibili terapie
Per dimostrare il valore pratico, il team ha applicato SSLGRDA per cercare nuovi RNA non codificanti coinvolti nel cancro al seno, nel cancro del colon e in altre condizioni. Molti dei suggerimenti in cima alla classifica sono stati successivamente confermati in database indipendenti o in report scientifici, a supporto della capacità del modello di individuare pattern biologicamente significativi. Per i non specialisti, la conclusione è che questo lavoro fornisce un modo più intelligente per esplorare il groviglio sempre più grande di dati biologici alla ricerca di indizi nascosti sulle malattie. Imparando automaticamente come RNA e malattie si raggruppano e interagiscono, i metodi grafici auto-supervisionati come SSLGRDA possono guidare i ricercatori di laboratorio verso i bersagli più promettenti, accelerando potenzialmente il percorso dai dati grezzi a diagnosi e terapie migliori.
Citazione: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
Parole chiave: RNA non codificanti, associazione con malattie, reti neurali su grafi, apprendimento auto-supervisionato, biologia computazionale